Sastav i struktura atomske jezgre (ukratko)
Mnogo prije pojave pouzdanih podataka o unutarnjoj strukturi svega što postoji, grčki mislioci zamišljali su materiju u obliku najmanjih vatrenih čestica koje su bile u stalnom pokretu. Vjerojatno je ta vizija svjetskog poretka stvari izvedena iz čisto logičkih zaključaka. Unatoč izvjesnoj naivnosti i apsolutnoj neutemeljenosti ove izjave, ispostavilo se da je to istina. Iako su znanstvenici mogli potvrditi hrabru pretpostavku tek dvadeset tri stoljeća kasnije.
Atomska struktura
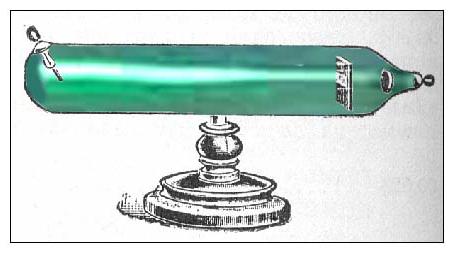
Krajem 19. stoljeća istraživana su svojstva ispusne cijevi kroz koju je struja prolazila. Opažanja su pokazala da se u ovom slučaju emitiraju dvije struje čestica:
- Katodne zrake koje se formiraju u blizini elektroda spojenih na negativni kraj baterije. Katodne zrake su prošle kroz cijev i mogle su proći kroz rupu u pozitivnoj elektrodi, poput struje nabijenih čestica. Opažanja su pokazala da je odnos naboja takve čestice prema njegovoj masi uvijek isti i ne ovisi o vrsti plina.
- Pozitivne zrake. Druga struja čestica ide u suprotnom smjeru i može proći u rupu negativne elektrode. Odstupanja u poljima pokazuju da imaju velike brzine i različite vrijednosti omjera naboj-masa.
Negativne čestice katodnih zraka nazivale su se elektronima. Nakon toga, čestice s istim omjerom naboj-masa nađene su u mnogim procesima. Činilo se da su elektroni univerzalne komponente različitih atoma, koji se vrlo lako odvajaju prilikom bombardiranja iona i atoma.
Čestice koje nose pozitivan naboj izgledale su kao fragmenti atoma nakon gubitka jednog ili više elektrona. Zapravo, pozitivne zrake bile su skupine atoma lišenih negativnih čestica, i kao rezultat toga, imale su pozitivan naboj.
Thompsonov model
Na temelju eksperimenata, utvrđeno je da pozitivne i negativne čestice predstavljaju bit atoma, njegove komponente. Engleski znanstvenik J. Thomson predložio je svoju teoriju. Prema njegovom mišljenju, struktura atoma i atomske jezgre bila je vrsta mase u kojoj su negativni naboj stisnut u pozitivno nabijenu loptu, poput grožđica u torti. Kompenzacija naboja učinila je „cupcake“ električno neutralnim. 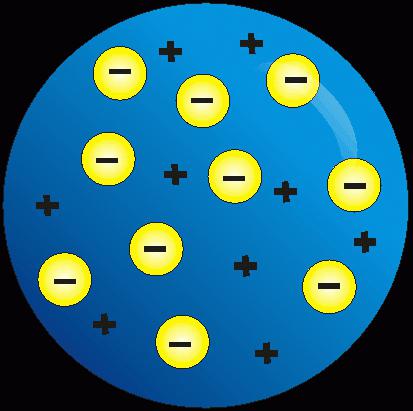
Rutherfordov model
Mladi američki znanstvenik Rutherford, analizirajući tragove preostale nakon alfa čestica, došao je do zaključka da je Thompsonov model nesavršen. Neke alfa čestice su otklonjene pod malim kutovima - 5-10 o . U rijetkim slučajevima alfa čestice su odstupale pod velikim kutom od 60-80 o , au iznimnim slučajevima, kutovi su bili vrlo veliki - 120-150 o . Thompsonov model atoma nije mogao objasniti takvu razliku.
Rutherford predlaže novi model koji objašnjava strukturu atoma i atomske jezgre. Fizika procesa tvrdi da atom mora biti 99% prazan, s malom jezgrom i elektronima koji se okreću oko nje, a koji se kreću u orbitama. 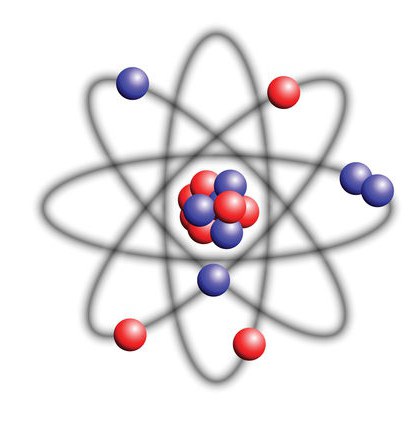
Odstupanja u udarcima, objašnjava činjenica da čestice atoma imaju svoje električni naboj. Pod utjecajem bombardiranja nabijenih čestica, atomski se elementi ponašaju kao obična nabijena tijela u makrokozmosu: čestice s identičnim nabojem odbijaju se i međusobno se privlače suprotnim nabojem.
Stanje atoma
Početkom prošlog stoljeća, kada su lansirani prvi akceleratori elementarnih čestica, sve teorije koje su objasnile strukturu atomske jezgre i sam atom čekali su eksperimentalnu verifikaciju. Do tada su interakcije alfa i beta zraka s atomima već temeljito proučavane. Sve do 1917. smatralo se da su atomi ili stabilni ili radioaktivni. Stabilni atomi ne mogu se razdvojiti, raspad radioaktivnih jezgri ne može se kontrolirati. No Rutherford je uspio pobiti ovo mišljenje.
Prvi proton
Godine 1911. E. Rutherford je iznio ideju da su sve jezgre sastavljene od identičnih elemenata, čija je osnova atom vodika. Na toj ideji, znanstvenik je potisnuo važan zaključak prethodnih istraživanja strukture materije: mase svih kemijskih elemenata podijeljene su bez ostatka masom vodika. Nova pretpostavka otvorila je neviđene mogućnosti, dopuštajući novi pogled na strukturu atomske jezgre. Nuklearne reakcije trebaju potvrditi ili opovrgnuti novu hipotezu.
Pokusi su provedeni 1919. s dušikovim atomima. Bombardirajući ih alfa česticama, Rutherford je postigao iznenađujući rezultat.
Atom N je apsorbirao alfa česticu, zatim se pretvorio u kisikov atom O17 i ispustio jezgru vodika. To je bila prva umjetna transformacija atoma jednog elementa u drugi. Takvo iskustvo usadilo je nadu da struktura atomske jezgre, fizika postojećih procesa dopušta druge nuklearne transformacije.

Znanstvenik je u svojim eksperimentima koristio metodu scintilacije - bljeskalice. S obzirom na frekvenciju bljeskova, izvukao je zaključke o sastavu i strukturi atomske jezgre, o svojstvima proizvedenih čestica, o njihovoj atomskoj masi i rednom broju. Nepoznata čestica se zvala Rutherfordov proton. Imao je sve karakteristike vodikovog atoma, lišen svog jedinog elektrona - jednog pozitivnog naboja i odgovarajuće mase. Tako je dokazano da su proton i jezgra vodika iste čestice.
Godine 1930., kada su izgrađeni i pokrenuti prvi veliki akceleratori, testiran je i dokazan Rutherfordov atomni model: svaki atom vodika sastoji se od jednog elektrona, čiji je položaj nemoguće odrediti, i slobodnog atoma s jednim pozitivnim protonom. Budući da protoni, elektroni i alfa čestice mogu letjeti iz atoma prilikom bombardiranja, znanstvenici su smatrali da su to komponente bilo koje atomske jezgre. No, takav model atomske jezgre izgledao je nestabilan - elektroni su bili preveliki da bi se uklopili u jezgru, osim toga, postojale su ozbiljne poteškoće povezane s kršenjem zakona zamaha i očuvanja energije. Ta dva zakona, kao strogi računovođe, kažu da količina pokreta i mase tijekom bombardiranja nestaju u nepoznatom smjeru. Budući da su ti zakoni općenito prihvaćeni, bilo je potrebno pronaći objašnjenja za takvo curenje.
neutroni
Znanstvenici diljem svijeta postavili su pokuse s ciljem otkrivanja novih sastojaka atomskih jezgri. Tridesetih godina prošlog stoljeća njemački fizičari Becker i Bothe bombardirali su atome berilija alfa česticama. U ovom slučaju, zabilježeno je nepoznato zračenje, za koje je odlučeno da se naziva G-zrake. Detaljne studije opisale su neke od značajki novih zraka: one su se mogle širiti strogo u ravnoj liniji, nisu bile u interakciji s električnim i magnetskim poljima i imale su visoku moć prodiranja. Kasnije su čestice koje tvore ovu vrstu zračenja pronađene u interakciji alfa čestica s drugim elementima - bora, kroma i drugih.
Chadwickova hipoteza
Zatim je James Chadwick, kolega i student Rutherforda, u časopisu Nature dao kratku poruku, koja je kasnije postala poznata. Chadwick je skrenuo pozornost na činjenicu da su proturječja u zakonima o očuvanju lako riješena, pod pretpostavkom da je novo zračenje struja neutralnih čestica, od kojih svaka ima masu približno jednaku masi protona. S obzirom na tu pretpostavku, fizičari su znatno dopunili hipotezu koja objašnjava strukturu atomske jezgre. Ukratko, bit dodavanja svedena je na novu česticu i njezinu ulogu u strukturi atoma. 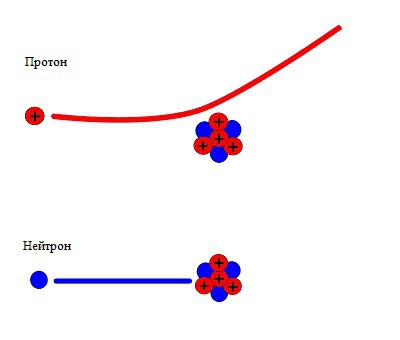
Neutronska svojstva
Detektirana čestica dobila je naziv "neutron". Novootkrivene čestice nisu formirale elektromagnetska polja oko sebe, lako su prolazile kroz tvar bez gubitka energije. U rijetkim sudarima s lakim jezgrama atoma, neutron je u stanju izbiti nukleus iz atoma, izgubiti značajan dio svoje energije. Struktura atomske jezgre pretpostavljala je prisutnost različitog broja neutrona u svakoj tvari. Atomi s istim nuklearnim nabojem, ali s različitim brojem neutrona, nazivaju se izotopima.
Neutroni su poslužili kao izvrsna zamjena za alfa čestice. Trenutno se koriste za proučavanje strukture atomske jezgre. Ukratko, njihovo značenje za znanost ne može se opisati, ali upravo zahvaljujući neutronskom bombardiranju atomskih jezgri fizičari su mogli dobiti izotope gotovo svih poznatih elemenata.
Sastav jezgre atoma
Struktura atomske jezgre danas je kombinacija protona i neutrona koje drže nuklearne sile. Primjerice, jezgra helija je snop dvaju neutrona i dva protona. Svjetlosni elementi imaju gotovo jednak broj protona i neutrona, dok teški elementi imaju mnogo veći broj neutrona. 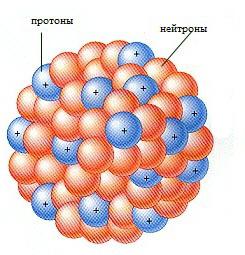 Ovu sliku strukture jezgre potvrđuju eksperimenti na suvremenim velikim ubrzivačima s brzim protonima. Električne sile odbijanja protona uravnotežene su silama jezgre koje djeluju samo u samoj jezgri. Iako priroda nuklearnih sila još nije u potpunosti shvaćen, njihovo postojanje je gotovo dokazano i potpuno objašnjava strukturu atomske jezgre.
Ovu sliku strukture jezgre potvrđuju eksperimenti na suvremenim velikim ubrzivačima s brzim protonima. Električne sile odbijanja protona uravnotežene su silama jezgre koje djeluju samo u samoj jezgri. Iako priroda nuklearnih sila još nije u potpunosti shvaćen, njihovo postojanje je gotovo dokazano i potpuno objašnjava strukturu atomske jezgre.
Odnos mase i energije
Godine 1932. Wilsonova kamera je snimila nevjerojatnu fotografiju koja dokazuje postojanje pozitivno nabijenih čestica masa elektrona. Prije toga, P. Dirac je teoretski predvidio pozitivne elektrone. U kozmičkom zračenju također je otkriven stvarni pozitivni elektron. Novi komad nazvan je pozitron. Kada se sudara sa svojim blizancem - elektronom, dolazi do anihilacije - uzajamnog uništenja dviju čestica. To oslobađa određenu količinu energije.
Prije toga, P. Dirac je teoretski predvidio pozitivne elektrone. U kozmičkom zračenju također je otkriven stvarni pozitivni elektron. Novi komad nazvan je pozitron. Kada se sudara sa svojim blizancem - elektronom, dolazi do anihilacije - uzajamnog uništenja dviju čestica. To oslobađa određenu količinu energije.
Tako je teorija razvijena za makro-svijet bila u potpunosti prikladna za opisivanje ponašanja najmanjih elemenata materije.