Svojstva soli: fizikalna i kemijska
Svakoga dana suočavamo se s solima i ne razmišljamo o ulozi koju igraju u našem životu. Ali bez njih, voda ne bi bila tako ukusna, a hrana ne bi donijela užitak, a biljke ne bi rasle, a život na zemlji ne bi mogao postojati ako u našem svijetu ne bi bilo soli. Dakle, koje su to tvari i koja im svojstva soli čine neophodnima?
Što je sol
U kompoziciji je najbrojnija klasa koja se razlikuje po raznolikosti. это продукт реакции между кислотой и основанием, при которой водородный атом заменяется металлическим. Već u 19. stoljeću kemičar J. Vercelius definirao je sol - to je proizvod reakcije između kiseline i baze u kojoj je vodikov atom zamijenjen metalnim. U vodi se soli obično rastavljaju u metal ili amonij (kation) i kiseli ostatak (anion).

Sol možete dobiti na sljedeće načine:
- interakcijom metala i nemetala, u ovom slučaju će biti bez kisika;
- kada metal reagira s kiselinom, dobiva se sol i otpušta vodik;
- metal može istisnuti drugi metal iz otopine;
- кислотного и основного (еще их называют оксидом неметалла и оксидом металла соответственно); u interakciji dva oksida , kisela i bazična (nazivaju se također ne-metalnim oksidom i metalnim oksidom);
- reakcija metalnog oksida i kiseline proizvodi sol i vodu;
- reakcija između baze i nemetalnog oksida također daje sol i vodu;
- Koristeći reakciju ionske izmjene, različite tvari koje su topive u vodi (baze, kiseline, soli) mogu reagirati, ali reakcija će se nastaviti ako se voda, voda ili slabo topljive (netopljive) soli formiraju u vodi.
Svojstva soli ovise samo o kemijskom sastavu. Ali prvo, pogledajmo njihove razrede.
klasifikacija
Ovisno o sastavu, razlikuju se sljedeće klase soli:
- na sadržaj kisika (bez kisika i bez kisika);
- na interakciji s vodom (topljiva, slabo topljiva i netopljiva).
Takva klasifikacija ne odražava u potpunosti raznolikost tvari. Moderna i najpotpunija klasifikacija, koja odražava ne samo sastav, već i svojstva soli, prikazana je u sljedećoj tablici.
| Sol | |||||
|---|---|---|---|---|---|
| normalan | kiseo | glavni | dvostruki | hibrid | kompleks |
| Vodik je potpuno zamijenjen | Atomi vodika zamijenjeni su metalom ne u potpunosti | Bazne skupine zamijenjene su kiselinskim ostatkom koji nije u potpunosti | Sastoji se od dva metala i jednog kiselinskog ostatka | Sastoji se od jednog metala i dva ostatka kiseline | Složene tvari koje se sastoje od kompleksnog kationa i aniona ili kationa i kompleksnog aniona |
| NaCl | KHSO 4 | FeOHSO3 | KNaSO 4 | CaClBr | [Cu (NH3) 4 ] S04 |
Fizička svojstva
Koliko god široka bila klasa tih tvari, moguće je izdvojiti opća fizikalna svojstva soli. To su tvari ne-molekularne strukture, s ionskom kristalnom rešetkom.
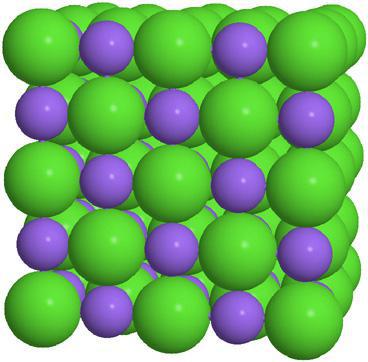
Vrlo visoka tališta i vrelišta. Pod normalnim uvjetima, sve soli ne provode električnu energiju, ali većina njih je savršeno vodljiva u otopini.
Boja može biti vrlo različita, ovisi o metalnom ionu, koji je njegov dio. Željezni sulfat (FeSO 4 ) je zelen, željezni klorid (FeCl3) je tamno crven, a kalijev kromat (K 2 CrO 4 ) je lijepa svijetlo žuta boja. Ali većina soli je i dalje bezbojna ili bijela.

Topljivost u vodi također varira i ovisi o sastavu iona. U principu, sva fizička svojstva soli imaju svojstvo. Oni ovise o tome koji ion metala i koji ostatak kiseline je uključen u pripravak. Nastavljamo razmatrati sol.
Kemijska svojstva soli
I ovdje je važna značajka. Osim fizičkih, kemijska svojstva soli ovise o njihovom sastavu. I na kojoj klasi pripadaju.

No, opća svojstva soli još uvijek se mogu razlikovati:
- mnogi od njih se pri zagrijavanju razgrađuju u dva oksida: kiseli i bazični, bez kisika - metal i nemetali;
- soli međusobno djeluju s drugim kiselinama, ali se reakcija odvija samo ako sol sadrži kiseli ostatak slabe ili hlapljive kiseline ili je rezultat netopljiva sol;
- interakcija s alkalijama je moguća ako kation tvori netopljivu bazu;
- reakcija je moguća između dvije različite soli, ali samo ako se jedna od novoformiranih soli ne otopi u vodi;
- može doći do reakcije s metalom, ali to je moguće samo ako uzmemo metal koji se nalazi desno od raspona napona od metala sadržanog u soli.
O kemijskim svojstvima normalnih soli govori se gore, dok ostale klase reagiraju sa supstancama na malo drugačiji način. Ali razlika je samo na proizvodima u trgovini. U osnovi, sačuvana su sva kemijska svojstva soli, kao i zahtjevi za reakcije.