Redoks potencijal: izračun i mjerenje
Redoks potencijal (ORP) je parametar koji opisuje razinu oksidacije (oksidacije) i redukciju tvari. Drugim riječima, to je sposobnost darovanja ili primanja elektrona kao posljedice interakcije kemijskih elemenata, ovisno o prirodi procesa i uvjetima reakcija.

Kratak opis
Redox potencijal - koncept koji u većoj mjeri odražava sposobnost nego udio (aktivnost). Energetski potencijal je energija koja se akumulira i spremna je za uporabu u bilo koje vrijeme. U trenutku kada se koriste svi kemijski spojevi koji se mogu podvrgnuti oksidaciji i redukciji, sustav dolazi u stanje ravnoteže. Najčešće, u takvim slučajevima, ostaje određena suvišna energija, koja formira redukcijski ili oksidacijski potencijal otopine.
Formiranje hrđe je tipičan primjer procesa oksidacije / redukcije. Elementi uključeni u ovaj proces prolaze kroz kemijske promjene. Kisik se kombinira s željezom u obliku željeznog oksida (poznatije kao rđa): željezo se podvrgava oksidaciji, a kisik se smanjuje. Kao rezultat toga, redoks potencijal "Fe / O 2 " sustava postaje ravnoteža.

ORP voda
Čista voda za piće vrlo je važan čimbenik u životu, što se često zaboravlja. Nažalost, postoji vrlo malo apsolutno čistih izvora pitke vode za život, koji se proizvode u industrijskim razmjerima kako bi se osigurala naselja. Stoga se voda koja ulazi u sustav vodoopskrbe mora očistiti i dezinficirati. Kako se ispostavilo, možete koristiti svojstva ORP-a.
Redoks potencijal vode mjeri se u minivoltima (mV). Ovaj parametar ukazuje na aktivnost dezinficijensa, a ne na njegovu koncentraciju, izraženu u ppm. Kemijski spojevi - klor, brom, vodikov peroksid, peroctena kiselina ili ozon - vrlo su učinkovita sredstva za oksidaciju (ali ne uvijek sigurna).
Oni su sposobni oksidirati ("selektirati") elektrone iz drugih kemijskih spojeva i stoga su izvrsni dezinficijensi. Dezinfekcijskim sredstvom uzrokuje promjene u kemijskom stanju patogena, štetnih algi i drugih organskih tvari. U praksi to znači da dekontaminirana voda s prikladnom razinom pH ne samo da može uništiti štetne bakterije, već se i od njih očistiti.
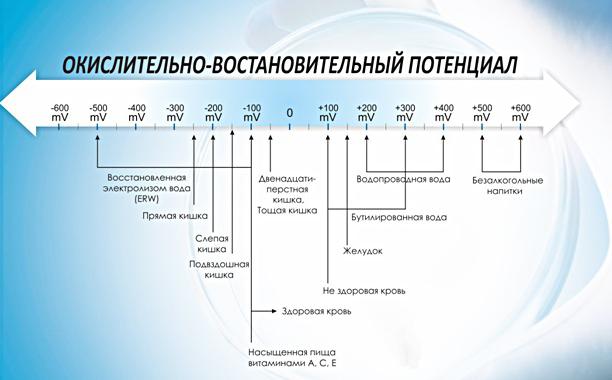
Sigurnosni standardi
Godine 1972. Svjetska zdravstvena organizacija (WHO) u Pravilniku o standardima za pitku vodu utvrdila je da se uz AFP od 650 mV voda smatra dezinficiranom, a inaktivacija virusa javlja se gotovo trenutno. Istraživanja su pokazala da ako je redoks potencijal 650 mV, bakterija E. coli se odmah uništi ili u roku od nekoliko sekundi. Za uništavanje otpornijih mikroorganizama, kao što su Listeria, Salmonella, kvasac i gljivice, potrebno je da ORP bude 750 mV ili više.
Kako mjeriti ORP
U praksi se mjerenje redoks potencijala provodi posebnim uređajima. Princip rada uređaja za registriranje ORP-a temelji se na mjerenju napona (u minivoltima, mV) u električnom krugu koji formira srebrna elektroda (negativni pol) i platinska trakasta elektroda (pozitivni pol). Mogu se koristiti i drugi materijali, kao što su grafit i stakleni ugljik. Elektrode uređaja se stavljaju u vodenu otopinu, a zatim se uzimaju očitanja.
Mjeri se vrlo mali napon (mV), koji nastaje kada se metal stavi u vodu koja sadrži oksidirajuće i reducirajuće tvari. Ove vrijednosti naprezanja karakteriziraju potencijal oksidanata sadržanih u tekućini.

Moguća ograničenja
Nije moguće točno izmjeriti standardni redoks potencijal, stoga se u praksi ORP vrijednost ispitivanog redoks para mjeri u odnosu na bilo koju standardnu polu-reakciju usporedbe i elektrodu stvorenu na njenoj bazi (referentna elektroda). Standardna polu-reakcija mora biti reverzibilna, a referentna elektroda mora imati stalan i ponovljiv potencijal i imati prilično jednostavnu strukturu.
Potencijal Redox elektrode
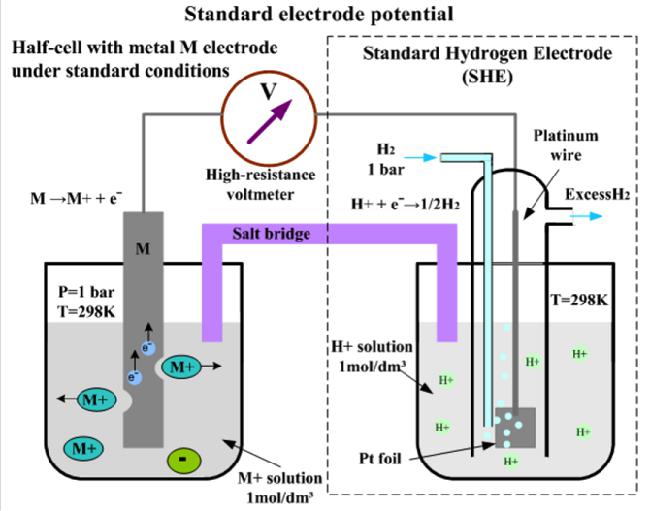
Standardna vodikova elektroda koja se sastoji od platinske trake prekrivene slojem fine platine (platina crna) i uronjena u otopinu soli, prihvaća znanstvena zajednica kao univerzalna referentna elektroda za mjerenje ORP. (sumporna) kiselina s aktivnošću iona kemijskog elementa vodika, jednako jednom: a H + = 1 .
Platina se ispire plinovitim vodikom pod tlakom od 101,3 kPa (ili 1 atm), koji se sorbira na poroznoj površini platine crne boje. Označava se standardna vodikova elektroda: Pt (H2) (p = 1 atm) HCl ( aH + = 1) .
Na površini takve reverzibilne elektrode dolazi do pola reakcije: 2N + + 2 ↔ N 2 ↑ . Potencijal, koji se uobičajeno prihvaća na nuli pri bilo kojoj temperaturi: E od SHE = 0 . Treba napomenuti da SHE nije redoks elektroda, već se odnosi na takozvane elektrode prve vrste. Njihov potencijal ovisi o aktivnosti određenih kationa - u prikazanom primjeru, o aktivnosti kationa vodika.
Redoks reakcije
IAD se naziva reakcija s promjenom stupnja oksidacije tvari koje reagiraju. S ovom promjenom oksidacijska stanja pojavljuje se s vezanjem / oslobađanjem elektrona. Procesi dodavanja i trzaja elektrona znanstvenici smatraju pola reakcija redukcije i oksidacije, odnosno:
- aOK 1 + ne V sOc 1 (oporavak);
- bBoc 2 - ne O dOk 2 (oksidacija).
U svakoj polovici reakcije element s višim stupnjem oksidacije naziva se oksidirani oblik (OK), au nižem stupnju oksidacije reducirani oblik (Boc). Oksidirani / reducirani oblici tvari su konjugirani redoks par koji se naziva redoks par. U redoks paru, oksidirani oblik (OK) je akceptor elektrona, reducirani oblik (Boc) je vrsta donora elektrona. Redukcija / oksidacijska polu-reakcija nije moguća odvojeno - ako je prisutan donor elektrona, tada mora biti prisutan i akceptor.
Standardni ORP
Ako se potencijal ispitivanog redoks para mjeri u standardiziranim uvjetima, temperatura je 25 ᵒ S (298 K), tlak je 1 atm (101,3 kPa), a aktivnost oksidiranih i reduciranih oblika jednaka je jednom ( ok = sun = 1 mol / l ) naziva se "standardni redoks potencijal" i označava se kao: E 0 cca / Vos .
Tablica potencijala
Standardni redoks potencijalni skupovi redoks parova znanstvenici su mjerili u praksi. Njihove vrijednosti u voltima prikazane su tablicom redoks potencijala:
OB par (OK / VOS) | E 0 Ok / Vos | OB par (OK / VOS) | E 0 Ok / Vos |
2H + / Hz | 0.00 | F 2 / 2F - | 2.28 |
S0 / H2S | -0,14 | MnO4- / Mn2 + | 1.51 |
Fe 2+ / Fe 0 | -0,47 | Cl 2 / 2Cl - | 1.36 |
Zn2 + / Zn0 | -0,76 | Fe3 + / Fe2 + | 0.77 |
Al3 + / Al0 | -1,61 | I 2 / 2I - | 0,54 |
Mg 2+ / Mg 0 | -2,07 | Sn 4+ / Sn 2+ | 0.15 |
Vrijednosti dekodiranja
Što je veći redoks potencijal E 0 OK / Boc , to je oblik više oksidiran, te u skladu s tim reducirani oblik ima slabiju redukcijsku funkciju. I obrnuto, što je manji E 0 Ok / Vos , to je jači obnovljeni oblik.
Pozitivan znak potencijala ukazuje na spontanu reakciju redukcije u tandemu s SHE, a negativna na spontanu oksidacijsku reakciju. Potencijali jakih oksidacijskih sredstava uvijek će biti pozitivni, a jaki redukcijski agensi će biti negativni.
Tablica redoks potencijala pokazuje da molekularni fluor ima najveća oksidativna svojstva, a metalik magnezij ima najveća redukcijska svojstva. u ove ione Fluor i magnezij praktički nemaju reducirajuća i oksidirajuća svojstva.
Nernstova jednadžba
Potencijal sustava ovisi o omjerima koncentracija reduciranih i oksidiranih oblika tvari uključenih u interakciju, temperature okoline, svojstava otapala, pH otopine i drugih čimbenika. Izračun redoks potencijala, izražen ovisnošću potencijala o sastavu otopine, pokazuje Nernstovu jednadžbu:
E Ok / Boc = E 0 Ok / Boc + (RT / nF) × ln (aOk / aBoc), gdje
- E Ok / Vos - realna AFP polu reakcija (redoks parovi).
- E 0 Ok / Vos - standardna ORP polu reakcija (redoks parovi).
- n je broj elektrona OB reakcije.
- R = 8,314 J / mol x K (molarna konstanta plina).
- F = 96500 C / mol (Faradayev broj).
- T je apsolutna temperatura (u K).
Oporavak i oksidacija
Redoks reakcije su određene stupnjem oksidacije i redukcije. Oksidacija se odnosi na procese kada atomi, molekule ili ioni doniraju elektrone. I oporavak - kada atomi, molekule ili ioni dobivaju elektrone.
Prema tome, oksidanti su tvari koje vežu elektrone (O2, halogene, HNO3, KMnO4) i redukcijska sredstva koja daruju elektrone drugim atomima tijekom redoks procesa (H2, metali, HI). Davanje elektrona drugima, sami redukcijski agensi se oksidiraju, a oksidirajuća sredstva, uzimajući elektrone iz drugih sudionika u reakciji, reduciraju se: 2FeCl2 + Cl2 → 2FeCl3 .
Stanje oksidacije
To je naboj koji bi atom u kemijskom spoju imao ako bi elektroni svake kemijske veze koju su stvorili bili potpuno pomaknuti na više elektronegativni atom. Na primjer:
- FeCl2: Fe + 2 , 2Cl- 1 ;
- NaH: Na + l , H- 1 ;
- CCI4: C + 4,4Cl- 1 ;
- CH4: C- 4 , 4H + 1 .
OVR može uključivati djelomične ili potpune prijelaze elektrona, stupanj oksidacije elemenata se mijenja. Primjenjuju se sljedeća pravila:
- U jednostavnoj tvari, oksidacijsko stanje atoma će biti nula (Cl 2 : 2 ClO).
- Stupanj oksidacije atoma iz sastava molekule je također nula.
- Stupanj oksidacije atoma kompleksnog iona bit će jednak naboju iona.
Određivanje redoks potencijala tla
AFP izravno utječe na strukturu tla. Za mjerenje, elektroda se zaglavi u mokro tlo, a vrijednost u mV (milivolti) određuje se na posebnom uređaju. Istovremeno se u tlima manifestiraju mnogi procesi i redoks reakcije transformacija aktivnih kemijskih elemenata: organske tvari, mangana, željeza, sumpora i dušika.
Odlučujući utjecaj na stanje tla vrši kisik u dva oblika: otopljen u vlazi zemlje i atmosferski. Oni su u ravnoteži. Na redoks procesima također se smanjuju tvari mikroorganizama. Glavni čimbenici koji određuju fokus i intenzitet AFP su:
- Stupanj vlage u tlu.
- Aktivnost mikroflore.
- Aeracija tla.
- Sadržaj organske tvari.
Visoke razine AFP karakteriziraju automorfna tla:
- Serozem - 350-450 mV.
- Černozemi - 400-600 mV.
- Podzol - 550-750 mV.
Kada se potencijal navodnjavanja smanji.
ORP vina
U proizvodnji vina, njegova važna karakteristika je redoks (redox) potencijal. Kontroliranjem redoks potencijala moguće je regulirati ili barem razumjeti značenje procesa "bijesnih" tijekom zrenja vinskih materijala. To su procesi reakcije fermentacije, redukcije i oksidacije.
Nakon kontakta s kisikom, samo-oksidirajući sustavi se mijenjaju, što rezultira povećanim potencijalom. Prema tome, što je dulji stupanj prozračivanja vinskog materijala, to je veći njegov redoks potencijal. Ako je pristup zraku zaustavljen, potencijal se postupno smanjuje, dosežući određene vrijednosti, nazvane graničnim potencijalom. Po pravilu, gazirana vina imaju pokazatelje od 350-500 mV, vina koja dozrijevaju bez zraka - 100-150 mV. Što je dulje vrijeme prošlo od punjenja alkoholnog pića u boce, to će biti manji potencijal. Potrebno je otvoriti bocu ili tresti, a koeficijent mV dramatično će se povećati.
ORP na kozmičkoj skali
Normalni redoks potencijal povijesno je bio odlučujući čimbenik u geološkoj evoluciji Zemlje i drugih kozmičkih tijela. Glavni oksidans u geološkim sustavima je kisik. Isparljivost kisika (fO 2 ) je mjera oksidacije prirodnih sustava, bez obzira na prisutnost ili odsutnost plinske faze koja u njima sadrži slobodni kisik. Nestabilnost kisika kontrolira ponašanje mnogih elemenata u procesima kondenzacije protoplanetarnog oblaka, pri nagomilavanju planeta i stvaranju njihovih metalnih jezgri. To znanje pomaže u predviđanju prisutnosti minerala.
Korištenje AFP-a u praksi
Mjerenje ORP omogućuje određivanje učinkovitosti dezinfekcije vode, bez obzira na vrstu korištenog oksidanta ili mješavinu dezinfekcijskih spojeva i drugih čimbenika. Rezultat mjerenja pokazuje je li postupak dezinfekcije stvarno učinkovit. Mjerenje vode ORP može se provesti u bilo kojoj točki sustava, čime se određuje čistoća izvora vode, cijevi, kao i vodovodne instalacije.
Redoks potencijal na svakom kraju sustava trebao bi biti veći od 650 mV. Ako je ORP izmjeren na kraju sustava manji nego na početku sustava, to znači da sustav vodoopskrbe nije dobro očišćen.
Upotreba ORP-a omogućuje pronalaženje optimalne ravnoteže između pH i sadržaja nevezanog klora. točnost mjerni instrumenti Omogućuje smanjenje razine klora na razinu u kojoj nema opasnosti od korozije. Na primjer, ako je ORP 850 mV, treba smanjiti razinu klora, a u slučaju kada je vrijednost 600 mV, treba provjeriti pH i nevezani klor, te u skladu s tim prilagoditi smanjenjem pH ili povećanjem prisutnosti klora.
ORP tehnologija se koristi u područjima kao što su obrada vode (prije i poslije potrošnje), obrada metala, dezinfekcija svježeg povrća i voća, ozoniranje vode (komercijalni akvariji, dezinfekcija vode), proizvodnja vina, proizvodnja bjelila, klaonice na farmama peradi, papirna industrija (izbjeljivanje pulpa), bazeni, SPA. Temperatura vode ne utječe na vrijednost ORP-a.

