Prvi zakon termodinamike za prosječnu osobu.
Sva ljudska aktivnost temelji se na potrošnji energije. Bez energije je teško zamisliti aktivnost organizma, funkcioniranje svih dobara za ljude. Važno je kako unutar osobe tako i za njegovu vanjsku egzistenciju. Različite industrije ne mogu samostalno raditi jer zahtijevaju energiju. Prijevoz robe, grijanje prostora, sinteza novih tvari u tijelu tijela - sve je to zbog sposobnosti proizvodnje.
Mjesto energije u termodinamici
Da bi se odredilo mjesto energije u ovoj grani znanosti, treba saznati što točno podrazumijeva termin "termodinamika". To je područje fizike u kojem se dubinski proučavaju procesi pretvorbe energije. Svatko zna da je energija predstavljena u nekoliko oblika: ona može biti kemijska, električna, toplinska, mehanička i svjetlosna. Ova grana znanosti ima čak svoje vlastite zakone i principe, primjerice prvi zakon termodinamike, kao i neke druge. Na temelju toga, može se reći da ovo područje znanja ne bi postojalo da svojstva gore opisane fizikalne veličine nisu poznata.
Kako se transformira energija?

Mnogi ljudi ne razumiju činjenicu prijenosa energije iz jednog stanja u drugo. Ali u svakodnevnom životu tako često koristimo prolaznu energiju da više ne iznosimo odakle dolazi. Primjerice, kad svakodnevno ulazimo u automobil, ne mislimo da u trenutku vožnje kemijska energija ide u električnu energiju. U elektromotoru se početna električna energija pretvara u mehaničku energiju, a u parnoj turbini toplina se pretvara u mehaničku fizičku veličinu. Uz sve to postoje određeni kvantitativni omjeri različitih oblika energije. No, tijekom procesa transformacije javljaju se neki kvantitativni gubici: potrošnja korisne energije uvijek je veća od njezine proizvodnje. Ova pojava se lako objašnjava: transformacija ne može bez trenja, tijekom koje dio energije postaje toplina i raspršuje se u prostoru. Ispada da se taj dio više ne može koristiti kao korisna količina. Prema tome, svaka pretvorba nije bez gubitaka.
Prvi zakon termodinamike
Proučavajući proces pretvorbe energije, znanstvenici su otkrili dva temeljna zakona. Ovaj članak će biti posvećen prvom od njih. Ovaj zakon termodinamike kaže: za svaku promjenu - kemijsku ili fizičku - količina energije ostaje konstantna. Na drugi način, također se naziva zakon o uštedi energije. Iz ove definicije slijedi da se energija ne pojavljuje iznenada i jednostavno ne nestaje. Ako u procesu bilo koje aktivnosti prelazi u različite oblike, od jednog do drugog, tada se njegov ukupni broj ne mijenja. Drugim riječima, energija se ne stvara ili uništava, što odražava prvi zakon termodinamike. Definicija u različitim izvorima može varirati, ali bit ostaje ista.

Povijest otkrića ovog zakona
Počinje svoj zakon od sredine XIX stoljeća. Njemački liječnik Mayer, promatrajući kako se mijenja boja ljudske krvi u tropima, razmišljao je o odnosu između takvih fizičkih pojmova kao što su toplina i energija. S druge strane, poznati znanstvenik Joule skrenuo je pozornost na razvoj Meier, nešto dodano na njegov dio. Sve podatke o ovom zakonu ujedinio je još jedan njemački liječnik, Helmholtz, kada je proučavao fizičke osnove organa opažanja - ljudskog sluha i vida. On je taj zakon formulirao na takav način da ga cijeli svijet poznaje danas.
Vrste razmjene energije
Toplina koja se javlja kada se jedna vrsta energije prenosi na drugu utječe na promjenu unutarnje energije objekta. Kada se promijeni, pojavljuje se protivljenje radu vanjskih sila koje utječu na ovaj objekt. Unutarnja energija može biti kinetička (to je kretanje atoma objekta), potencijal (pohranjen je u kemijskim vezama između atoma), gravitacijska energija cijelog sustava (tj. Učinak na objekt) gravitacijske sile koji se manifestiraju unutar). Na temelju tih vrsta znanstvenici su identificirali određene vrste razmjene energije.
- Prvi se obično smatra predizoliranim sustavima - nema razmjene energije i drugih elemenata određenog sustava.
- Drugi tip su zatvoreni sustavi, karakterizirani nedostatkom razmjene elemenata sustava, ali se u neznatnoj mjeri izmjenjuje energija.
- Otvoreni sustavi (treći tip razmjene) karakteriziraju razmjena i energija te njihovi elementi.
pojam unutarnja energija u termodinamici
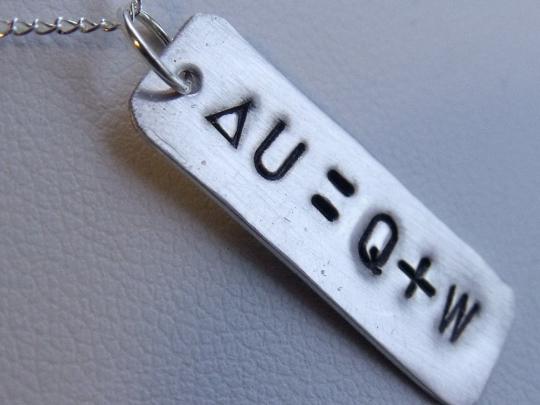
Unutarnja energija objekta ili sustava u termodinamici igra gotovo ključnu ulogu. Zapravo, ovo je složena kombinacija nekoliko tokova aktivnosti molekula i atoma. Sastoji se od vrsta kao što su energija rotacije i kretanje naprijed molekula, energija gibanja atoma i skupina atoma, koja se nalazi unutar molekula i emitira se kad te čestice osciliraju. Nuklearna energija atoma i energija interakcije između molekula također su povezane s unutarnjom energijom objekta. U NR ovisi o početnom stanju objekta i konačnim pokazateljima njegovog stanja. Ta je energija kontinuirana, kao prvi zakon termodinamike. Može se lako izračunati pomoću sljedeće formule: toplina dodana sustavu, minus rad koji obavlja ovaj sustav. Ovdje ne govorimo o prirodi procesa promjene unutarnje energije, čak ni o konačnom stanju ravnoteže, jer to već određuje drugi zakon termodinamike.
Odnos topline i unutarnje energije
Ti su pojmovi vrlo usko povezani. Pretpostavlja se da je toplina dio unutarnje energije sustava. Shvatit ćemo što je vrućina. Sam subjekt nema takav u uobičajenom smislu te riječi. Može se reći da je toplina energija koja prolazi od objekta koji ima visoku temperaturu do objekta s temperaturom nižom od one prve.

Drugim riječima, to je dio unutarnje energije objekta, koji se iz nje prenosi, jer ima više temperaturne pokazatelje. Takav prijenos u fizici i kemiji naziva se grijanje.
Prvi zakon termodinamike, kemija
Ovaj je zakon od temeljne važnosti ne samo za fizičke pokuse, proučavanje pojava i otkrivanje novih procesa, već i za drugu znanost - kemiju - i srodne industrije. Proučavanjem postojanja i prijenosa energije u različite oblike iz perspektive kemijskih reakcija tijela ili objekta otvara se horizont zanimljivih istraživanja i uzoraka u bioenergetskoj ravnini.

Mnogi smatraju da je prvi zakon termodinamike udaljen od života obične osobe, da su molekule i atomi podložni samo razumijevanju malog broja posvećenih ljudi. Ali ovo je daleko od slučaja. Osnova života svakog živog organizma je metabolizam, koji se ne može dogoditi bez transformacije energije. Stoga su kemijski procesi pretvorbe energije u ljudskom tijelu od posebnog interesa ne samo za fizičare, već i za dijetetičare i sportske instruktore. Uostalom, znajući sve značajke ovog procesa, možete uspješno pomoći ljudima da se riješe viška kilograma, kao i da se brinu o sebi uz pomoć pravilno sastavljenog jelovnika koji se sastoji od zdrave hrane.