Vanadij: svojstva, atomska masa, formula, primjena
Vanadij je kemijski element označen simbolom "V". Atomska masa vanadija je 50.9415 a. m., atomski broj - 23. To je čvrsti srebrno-sivi, kovan i topiv metal, koji se rijetko nalazi u prirodi. Dio je više od 60 minerala i može se čak nalaziti u fosilnim gorivima.

Neprepoznato otkriće
Metoda vanadija prvi je put otkrio meksički mineralog španjolskog podrijetla, Andres Manuel Del Rio, 1801. godine. Istraživač je uklonio novi element iz uzorka smeđe olovne rude koja se kopa u Meksiku. Kako se ispostavilo, metalne soli imaju veliku raznolikost boja, tako da ga je Del Rio prvobitno nazvao "panchromium" (od grčkog "παγχρώμιο" - "višebojan").
Kasnije je mineralog preimenovan u element erythronium (iz grčkog “ερυθρός” - “crveni”), jer je većina soli dobila crvenu nijansu kada se zagrijava. Čini se da se nevjerojatna sreća nasmiješila malo poznatom znanstveniku u Europi. Otkriće novog kemijskog elementa vanadija obećao, ako ne i slavu, onda barem priznanje od strane kolega. Međutim, zbog nedostatka važnog autoriteta u znanstvenom svijetu, postignuće Meksika je ignorirano.
Godine 1805. francuski kemičar Hippolytus Victor Colle-Dekotils sugerirao je da je novi element koji je istraživao Del Rio bio samo uzorak kromata olova s nečistoćama. Na kraju, meksički istraživač, kako ne bi potpuno izgubio lice pred znanstvenim bratstvom, prihvatio je odobrenje Colle-Decotyle i odbio ga otvoriti. Međutim, njegovo postignuće nije potonulo u zaborav. Danas je Andrés Manuel Del Río prepoznat kao otkrivač rijetkog metala.
ponovno otkriće
Godine 1831. Šveđanin Nils Gabriel Sefström ponovno je otkrio kemijski element vanadij u oksidu koji je dobio kada je radio s željeznom rudom. Kao svoju oznaku, znanstvenik je odabrao slovo "V", koje još nije dodijeljeno nijednom elementu. Sefström je novi metal nazvao zbog svoje lijepe i bogate boje u čast nordijske boginje ljepote Vanadis.
Vijest je izazvala pojačano zanimanje za znanstvenu zajednicu. Odmah se sjetio rada meksičkog minerologa. U istom 1831. Friedrich Wöhler ponovno je provjerio i potvrdio prethodno otkriće Del Rioa. A geolog George William Featherstonhup čak je predložio nazivanje metala "Rionium" u čast otkrivaču, ali inicijativa nije podržana.

nedostižan
Izolacija metala vanadija u čistom obliku pokazala se teškom. Prije toga znanstvenici su radili samo s njegovim solima. Zato su nepoznata prava svojstva vanadija. Godine 1831. Berzelius je izvijestio da je primio metaliziranu tvar, ali Henry Enfield Roscoe je dokazao da je Berzelius zapravo proizvodio vanadij nitrid (VN). Konačno, Roscoe je proizveo metal 1867. reducirajući vanadij klorid (VCl2) pod djelovanjem vodika. Od 1927. dobiva se čisti vanadij redukcijom vanadijevog pentoksida uz sudjelovanje kalcija.
Prva serijska industrijska uporaba elementa datira iz 1905. Metal je dodan čeličnoj leguri za proizvodnju šasija trkaćih automobila, a kasnije - u modelu Ford T. Karakteristike Vanadija mogu smanjiti težinu konstrukcije, a povećati zateznu čvrstoću. Usput rečeno, njemački kemičar Martin Khenze otkrio je 1911. godine vanadij u krvnim stanicama (ili koelomijskim stanicama) morskih stanovnika - uličice.

Fizička svojstva
Vanadij je duktilno sivo-plavi metal srednje tvrdoće sa čeličnim sjajem i gustoćom od 6,11 g / cm3. Neki izvori opisuju materijal kao mekan, imajući u vidu njegovu visoku plastičnost. Kristalna struktura elementa složenija je od većine metala i čelika.
Vanadij ima dobru otpornost na koroziju, alkalije, sumpor i klorovodična kiselina. On oksidira na zraku na temperaturi od oko 660 ° C (933K, 1220 ° F), iako se pasivizacija oksida događa čak i na sobnoj temperaturi. Taj se materijal topi kada temperatura dosegne 1920 ° C, a vrije na 3400 ° C.
Kemijska svojstva
Vanadij pod utjecajem kisika tvori četiri tipa oksida:
boja | gustoća | vrenje | taljenje | |
VO (II) | crna | 5,76 g / cm3 | 3100 ° C | 1830 ° C |
V 2 O 3 (III) | crna | 4.87 g / cm3 | 3000 ° C | 1967 ° C |
VO 2 (IV) | Mornarsko plavo | 4.65 g / cm3 | 2700 ° C | 1542 ° C |
V 2 O 5 (V) | narančasta | 3,357 g / cm3 | 2030 ° C | 670 ° C |
Spojevi vanadija tipa (II) su reducensi, a spojevi tipa (V) su oksidirajuća sredstva. Spojevi (IV) često postoje kao derivati vanadilnog kationa.
oksid
Najvažniji komercijalno važan spoj je vanadijev pentoksid. To je smeđe-žuta krutina, iako je kada je svježe upakirana iz vodene otopine, njena boja je tamno narančasta.

Oksid se koristi kao katalizator za dobivanje sumporne kiseline. Ovaj spoj oksidira sumporni dioksid (SO2) u trioksid (SO3). U ovoj redoks reakciji sumpor se oksidira od +4 do +6, a vanadij se smanjuje od +5 do +4. Formula za vanadij je sljedeća:
V2O5 + SO2 → 2VO2 + SO3
Katalizator se regenerira oksidacijom kisika:
2VO 2 + O 2 → V 2 O 5
Slični oksidacijski procesi koriste se u proizvodnji anhidrida maleinske kiseline, ftalnog anhidrida i nekoliko drugih skupnih organskih spojeva.
Ovaj oksid se također koristi u pripravi ferrovanadija. Zagrijava se željezom i ferosilicijom uz dodatak vapna. Kada se koristi aluminij, legura željezo-vanadij se proizvodi zajedno s aluminijevim oksidom kao nusprodukt. Zbog visokog koeficijenta toplinskog otpora, vanadijev oksid (V) se koristi kao detektorski materijal u bolometrima i mikrobolometarskim nizovima u uređajima za toplinsko snimanje.
karakteristike
Rijetki metal ima sljedeće karakteristike:
- Kristalna struktura: kubični u središtu tijela.
- Provodljivost zvuka: 4560 m / s (na 20 ° C).
- Valencija valadija: V (rijetko IV, III, II).
- Toplinsko širenje: 8,4 μm / (m · K) (na 25 ° C).
- Toplinska provodljivost: 30,7 W / (m · K).
- Električni otpor: 197 nm · m (pri 20 ° C).
- Magnetizam: paramagnetski.
- Magnetska osjetljivost: + 255 · 10 -6 cm3 / mol (298K).
- Modul elastičnosti: 128 GPa.
- Modul smicanja: 47 GPa.
- Skupni modul elastičnosti: 160 GPa.
- Poissonov omjer: 0,37.
- Tvrdoća Mohsa: 6.7.
- Tvrdoća po Vickersu: 628-640 MPa.
- Tvrdoća po Brinellu: 600-742 MPa.
- Kategorija predmeta: prijelazni metal.
- Elektronička konfiguracija: 3d 3 4s 2 .
- Toplina topljenja: 21,5 kJ / mol.
- Toplina isparavanja: 444 kJ / mol.
- Molarni toplinski kapacitet: 24,89 J / (mol · K).
Vanadij u periodnom sustavu nalazi se u 5. skupini (podgrupa vanadija), četvrto razdoblje, d-blok.
širenje
Vanadij u skali svemira je oko 0,0001% ukupnog volumena tvari. Često se širi poput bakra i cinka. Metal se nalazi u spektralnom sjaju Sunca i drugih zvijezda.
Element je 20. najčešći u kori. Kristal vanadij u kristalnom obliku je vrlo rijedak, ali spojevi ovog materijala nalaze se u 65 različitih minerala. Ekonomski značajni od njih su patronit (VS 4 ), vanadinit (Pb 5 (VO 4 ) 3 Cl) i karnotit (K2 (UO2) 2 (VO 4 ) 2 · 3 H 2 O).
Vanadil ioni su obilno raspoređeni u morskoj vodi i imaju prosječnu koncentraciju od 30 nMa. Neki izvori mineralne vode također sadrže te ione u visokim koncentracijama. Primjerice, izvori u blizini planine Fuji sadrže do 54 µg / l.
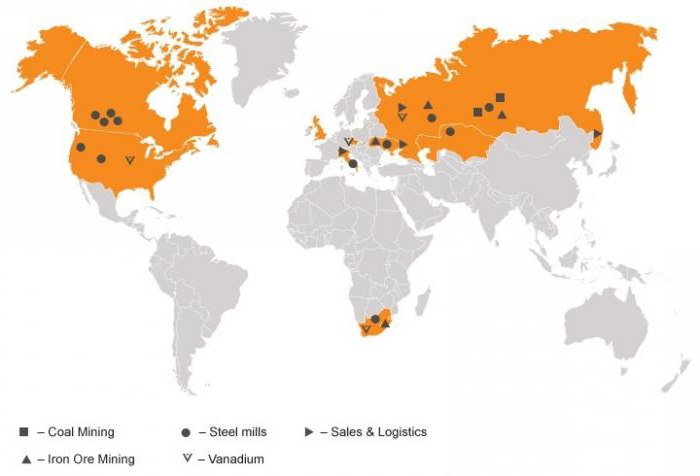
vađenje
Veći dio ovog rijetkog metala dobiven je od vanadijevog magnetita koji se nalazi u ultrabazičnim magmatskim gabrovoj stijeni. Sirovine se uglavnom kopaju u Južnoj Africi, sjeverozapadnoj Kini i istočnoj Rusiji. Ove su zemlje u 2013. proizvele više od 97% ukupnog vanadija (79.000 tona).
Metal je također prisutan u boksitu i depozitima sirove nafte, ugljena, uljnih škriljaca i katranskog pijeska. U sirovom ulju zabilježene su koncentracije do 1200 ppm. Zbog oksidativnih svojstava vanadija (nekih njegovih oksida) nakon sagorijevanja takvih naftnih proizvoda, ostaci elementa mogu uzrokovati koroziju u motorima i kotlovima.
Procjenjuje se da se oko 110.000 tona tvari godišnje ispušta u atmosferu spaljivanjem fosilnih goriva. Danas se razvijaju tehnologije za vađenje vrijednih tvari iz ugljikovodika.
proizvodnja
Vanadij se uglavnom koristi kao dodatak čeličnim legurama koje se nazivaju ferolegure. Ferrovanadij se dobiva izravno redukcijom smjese vanadijevog oksida s valencijom (V), željezovim oksidima i čistim željezom u električnoj peći.
Metali se dobivaju višestupanjskim postupkom, koji započinje sagorijevanjem drobljene vanadijeve magnetitne rude dodatkom natrijevog klorida (NaCl) ili natrijevog karbonata (Na2C03) pri temperaturi od oko 850 ° C, čime se dobiva natrijev metavanadat (NaVO 3 ). Vodeni ekstrakt ove tvari zakiseljen je kako bi se dobila polivanadatna sol, koja je reducirana metalom kalcija. Kao alternativa maloj proizvodnji, vanadijev pentoksid se reducira vodikom ili magnezijem.
Koriste se i mnoge druge metode, u kojima se vanadij proizvodi kao nusproizvod drugih procesa. Njeno čišćenje moguće je metodom jodida koju su razvili Anton Edouard van Arkel i Jan Hendrik de Bohr 1925. To podrazumijeva stvaranje vanadij (III) jodida i njegovo naknadno razlaganje u čisti metal:
2 V + 3I 2 VI 2 VI 3
Japanci su izmislili prilično egzotičan način dobivanja ovog elementa. Uzgajaju se na podvodnim plantažama (tip akorda), koje apsorbiraju vanadij iz morske vode. Zatim se skupljaju i spaljuju. Vrijedan metal se izdvaja iz oblikovanog pepela. Usput, njegova koncentracija u ovom slučaju je mnogo veća nego u najbogatijim depozitima.

legure
Što su legure vanadija? Približno 85% proizvedenog rijetkog metala koristi se za proizvodnju ferovanadija ili kao dodatak čeliku. Početkom 20. stoljeća ustanovljeno je da čak i mala količina vanadija značajno povećava čvrstoću čelika. Ovaj element formira stabilne nitride i karbide, što dovodi do poboljšanja performansi čelika i legura.
Od tada se vanadij koristi u osovinama, okvirima, koljenastim vratilima, zupčanicima i drugim važnim komponentama vozila na kotačima. Postoje dvije skupine legura:
- Visok sadržaj ugljika od 0,15% do 0,25% vanadija.
- Brzo rezanje alatni čelici (HSS) sadržaj od 1% do 5% ovog elementa.
Kod HSS čelika može se postići tvrdoća veća od HRC 60. Koriste se u kirurški instrumenti. U metalurgiji praha, legure mogu sadržavati do 18% vanadija. Visok sadržaj karbida u tim legurama značajno povećava otpornost na trošenje. Oni prave alate i noževe.
Zbog svojih svojstava vanadij stabilizira beta oblik titana, povećava njegovu čvrstoću i stabilnost temperature. Pomiješan s aluminijem u titanovim legurama, koristi se u mlaznim motorima, brzim zrakoplovima i zubnim implantatima. Najčešća legura bešavnih cijevi je titan 3 / 2.5, koja sadrži 2,5% vanadija. Ovi su materijali široko rasprostranjeni u zrakoplovnoj, obrambenoj i biciklističkoj industriji. Još jedna uobičajena legura, proizvedena uglavnom u listovima, je titan 6AL-4V, gdje 6% aluminija i 4% vanadija.
Nekoliko legura vanadija pokazuje supravodljiva svojstva. Prvi fazni supravodič A15 je V3 Si vanadijski spoj, koji je dobiven 1952. Vonadij-galijeva vrpca koristi se u supravodljivim magnetima. Struktura supravodljive faze A15 V 3 Ga slična je strukturi uobičajenih supravodiča: stannida triniobija (Nb 3 Sn) i niobij-titana (Nb3 Ti).
Nedavno su znanstvenici otkrili da je u srednjem vijeku nekim uzorcima damasta i damasta čelika dodana mala količina vanadija (od 40 do 270 dijelova na milijun). To je poboljšalo svojstva lopatica. Međutim, nejasno je gdje i kako je miniran rijetki metal. Možda je bio dio nekih ruda.
primjena
Osim metalurgije, vanadij se koristi i za druge zadatke. Poprečni presjek hvatanja toplinskog neutrona i kratkog poluživota izotopa proizvedenih hvatanjem neutrona čine ovaj metal prikladnim materijalom za uporabu unutar fuzijskog reaktora.
Najčešći vanadijev oksid, pentoksid V 2 O 5, koristi se kao katalizator u proizvodnji sumporna kiselina i kao oksidacijsko sredstvo u proizvodnji anhidrida maleinske kiseline. Vanadijev oksid se koristi u proizvodnji keramičkih proizvoda.
Metal je važna komponenta mješovitih metalnih oksidnih katalizatora koji se koriste u oksidaciji propana i propilena u akroleinu, akrilnoj kiselini ili amoksidaciji propilena u akrilonitril. Drugi vanadij oksid - dioksid VO2 - koristi se u proizvodnji staklenih premaza koji blokiraju infracrveno zračenje na određenoj temperaturi.
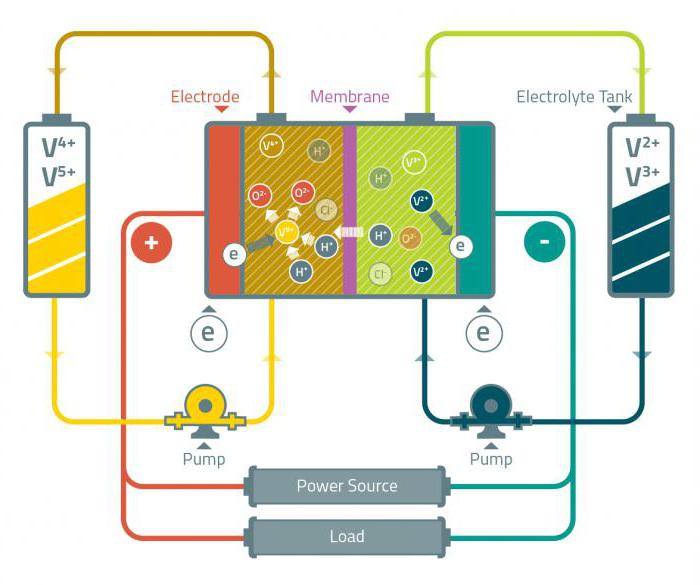
Vanadijska redoks baterija je galvanska ćelija koja se sastoji od vodenih iona vanadija u različitim oksidacijskim stanjima. Baterije ove vrste prvi su put predložene tridesetih godina prošlog stoljeća, a komercijalna uporaba počela je 1980-ih. Vanadat se može koristiti za zaštitu čelika od korozije.
Vanadij je važan za ljudsko zdravlje. Pomaže regulirati metabolizam ugljika i lipida, uključen je u proizvodnju energije. Dnevno se preporučuje konzumiranje 6-63 mcg (WHO podataka) tvari iz hrane. Dovoljno je kod žitarica, mahunarki, povrća, ljekovitog bilja, voća.