Što je barijev sulfat? Kako dobiti barijev sulfat?
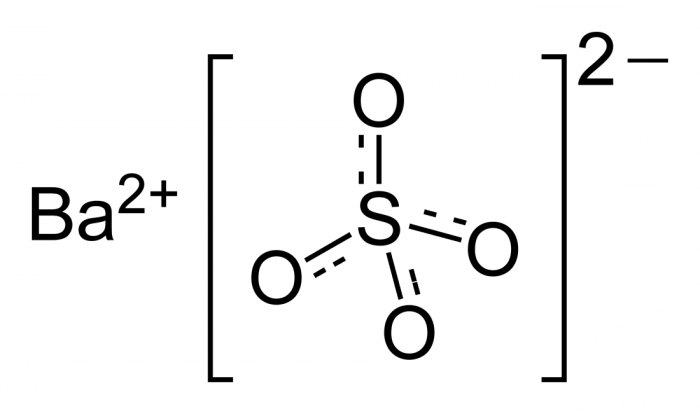
Barijev sulfat je anorganska tvar s kemijskom formulom BaSO 4 . To je bijeli prah, bez mirisa, netopljiv u vodi. Njezina bjelina i neprozirnost, kao i visoka gustoća određuju glavna područja primjene.
Povijest naslova
Barij se odnosi na zemnoalkalijske metale. Potonji su tako nazvani jer, prema D.I. Mendeleevu, njihovi spojevi tvore neotopljivu masu Zemlje, a oksidi "imaju zemljani izgled". Barij se prirodno nalazi u obliku minerala barita, koji je barij sulfat s raznim nečistoćama.
Prvi su ga otkrili švedski kemičari Scheele i Gan 1774. kao dio takozvanog teškog sparija. Odatle i naziv minerala (od grčkog. "Baris" - težak), a zatim i sam metal, kada ga je 1808. godine izolirao u svom čistom obliku Humphry Devi.
Fizička svojstva
Budući da je BaSO 4 sol sumporne kiseline, njena fizička svojstva djelomično su određena samim metalom, koji je mekan, kemijski aktivan i srebrno bijeli. Prirodni barit je bezbojan (ponekad bijeli) i proziran. Kemijski čisti BaSO4 ima boju od bijele do blijedožute boje, nije zapaljiva, s točkom taljenja od 1580 ° C.

Kolika je masa barijevog sulfata? Njegova molarna masa je 233,43 g / mol. Ima neuobičajeno visoku specifičnu težinu - od 4,25 do 4,50 g / cm3. S obzirom na netopljivost u vodi, visoka gustoća čini ga nezamjenjivim kao punilo za tekućine za bušenje vode.
Kemijska svojstva
BaSO 4 je jedan od najslabije topljivih spojeva u vodi. Može se dobiti iz dvije vrlo topljive soli. Uzeti vodenu otopinu natrijevog sulfata - Na2S04. njegov molekula u vodi disocira na tri iona: dva Na + i jedan SO 4 2- .
Na 2 SO 4 → 2Na + + SO 4 2- 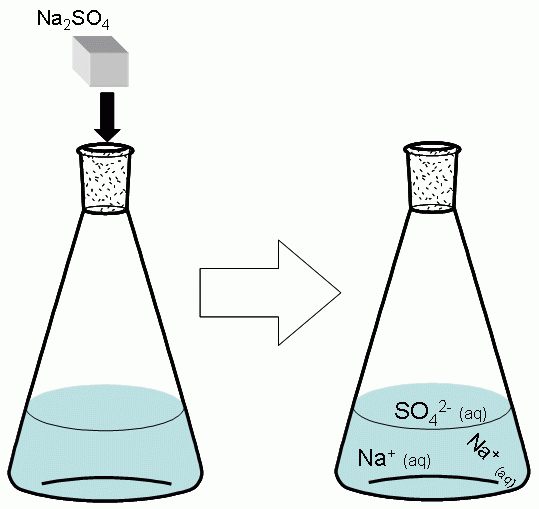
Uzmite također i vodenu otopinu barijevog klorida - BaCl 2 , čija se molekula disocira na tri iona: jedan Ba 2+ i dva Cl - ,
BaCl2 → Ba 2+ + 2Cl -
Miješa se vodena otopina sulfata i smjesa koja sadrži klorid. Barijev sulfat nastaje kao posljedica kombiniranja u jednu molekulu dva iona s istom veličinom i suprotno u naboju signala.
Ba 2+ + SO 4 2- → BaSO 4
U nastavku možete vidjeti potpunu jednadžbu ove reakcije (tzv. Molekularnu).
Na2S04 + BaCl2 → 2NaCl + BaSO4 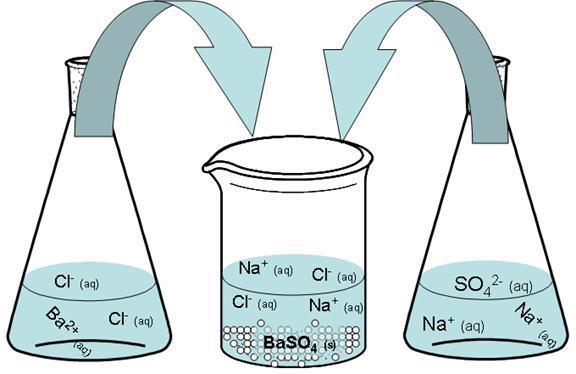
Rezultat je netopljivi talog barijevog sulfata.
Roba Barite
U praksi, sirovina za dobivanje tržišnog barijevog sulfata, namijenjena za uporabu u bušotinama za bušenje naftnih i plinskih bušotina, u pravilu je mineralni barit.
Pojam "primarni" barit odnosi se na robne proizvode koji uključuju sirovinu (dobivenu iz rudnika i kamenoloma), kao i jednostavne proizvode za obogaćivanje metodama kao što su pranje, taloženje, odvajanje u teškim medijima, flotacija. Veći dio sirovog barita zahtijeva njegovo dovođenje na minimalnu čistoću i gustoću. Mineralni materijal koji se koristi kao punilo je smrvljen i prosijan do ujednačene veličine tako da najmanje 97% njegovih čestica ima veličinu do 75 mikrona, a ne više od 30% manje od 6 mikrona. Primarni barit također treba biti dovoljno gust, tako da njegova specifična težina iznosi 4,2 g / cm3 ili više, ali u isto vrijeme dovoljno mekana da ne bi oštetila ležajeve.
Priprema kemijski čistog proizvoda
Mineralni barit je često kontaminiran raznim nečistoćama, uglavnom željeznim oksidima, koji ga boje u različitim bojama. Obrađuje se karbotermnom metodom (grijanje koksom). Rezultat je barijev sulfid.
BaSO 4 + 4 S → BaS + 4 SO
Potonji je, za razliku od sulfata, topiv u vodi i lako reagira s kisikom, halogenima i kiselinama.
BaS + H2S04 → BaS04 + H2S
Da biste dobili proizvod visoke čistoće, koristite sumporna kiselina. Barijev sulfat, koji je nastao ovim procesom, često se naziva blanfix, koji na francuskom znači "fiksni bijeli". Često se nalazi u potrošačkim proizvodima, kao što su boje.

U laboratorijskim uvjetima, barij sulfat nastaje kombiniranjem barijevih iona i sulfatnih iona u otopini (vidi gore). Budući da je sulfat najmanje toksična barijeva sol zbog svoje netopljivosti, otpad koji sadrži njegove druge soli ponekad se tretira natrijev sulfat vezati sav barij, koji je vrlo toksičan.
Od sulfata do hidroksida i natrag
Povijesno gledano, barit se koristi za proizvodnju barijevog hidroksida Ba (OH) 2 , koji je potreban za rafiniranje šećera. To je općenito vrlo zanimljiv i široko korišten spoj u industriji. Lako se otapa u vodi, tvori otopinu poznatu kao baritna voda. Prikladno je koristiti za vezanje sulfatnih iona u različitim pripravcima stvaranjem netopljivog BaS04.
Vidjeli smo gore da kada se zagrijava u prisutnosti koksa iz sulfata, lako je dobiti vodotopivi barijev sulfid - BaS. Potonji, u dodiru s vrućom vodom, tvori hidroksid.
BaS + 2H20 → Ba (OH) 2 + H2S
Barijev hidroksid i natrijev sulfat, uzeti u otopini, kada se promiješaju, daju netopljivi talog barijevog sulfata i natrijev kaustik.
Ba (OH) 2 + Na2S04 = BaS04 + 2NaOH

Pokazalo se da se prirodni barijev sulfat (barit) industrijski najprije pretvara u barijev hidroksid, a zatim služi za dobivanje istog sulfata tijekom pročišćavanja različitih sustava soli iz sulfatnih iona. Na isti način, reakcija će se odvijati pri čišćenju od SO 4 iona - otopine bakrenog sulfata. Ako napravite mješavinu barijevog hidroksida + bakrovog sulfata, rezultat je bakrov hidroksid i netopljivi barijev sulfat.
CuS04 + Ba (OH) 2 → Cu (OH) 2 + BaS04
Čak iu samoj reakciji sa sumpornom kiselinom, njegovi sulfatni ioni bit će potpuno vezani barijem.
Koristiti u isplaci
Oko 80% svjetske proizvodnje pročišćenog i mljevenog barita barijevim sulfatom troši se kao sastavni dio bušotinskih fluida u stvaranju naftnih i plinskih bušotina. Dodatak povećava gustoću tekućine koja se ubrizgava u bušotinu, s ciljem bolje otpornosti na visoki formacijski tlak i sprečavanje izbijanja.
Kada se bušotina izbuši, bit prolazi kroz drugačiju formaciju, od kojih svaka ima svoje karakteristike. Što je veća dubina, veći postotak barita mora biti prisutan u strukturi otopine. Dodatna prednost je da je barijev sulfat nemagnetna tvar, tako da ne interferira s različitim mjerenjima u bušotini s elektroničkim uređajima.
Industrija boja i papira
Većina sintetičkih BaSO 4 se koristi kao sastojak bijelog pigmenta za boje. Tako se blanc fiksiran u smjesi s titanovim dioksidom (TiO2) prodaje kao bijela uljana boja koja se koristi u bojanju.
Kombinacija BaSO 4 i ZnS (cinkov sulfid) proizvodi anorganski pigment nazvan litopon. Koristi se kao premaz za određene stupnjeve fotografskog papira.
U novije vrijeme, barijev sulfat se koristi za posvjetljivanje papira dizajniranog za inkjet pisače.
Primjena u kemijskoj industriji i obojenoj metalurgiji
U proizvodnji polipropilena i polistirena BaSO 4 koristi se kao punilo u omjeru do 70%. Ima učinak povećanja otpornosti plastike na kiseline i lužine, a također im daje neprozirnost.
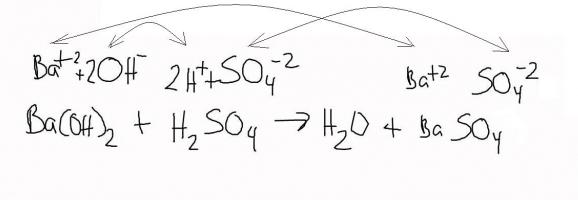
Također se koristi za proizvodnju drugih spojeva barija, posebice karbonata, koji se koristi za proizvodnju LED stakla za televizijske i računalne zaslone (povijesno u katodnim cijevima).
Kalupi koji se koriste u lijevanju metala često premazuju barij sulfatom kako bi se spriječilo prianjanje na rastaljeni metal. To se radi u proizvodnji anodnih bakrenih ploča. Bačeni su u bakrene kalupe obložene slojem barijevog sulfata. Kada se tekući bakar stvrdne kao gotova anodna ploča, može se lako ukloniti iz kalupa.
Pirotehnička sredstva
Budući da spojevi barija ispaljuju zeleno svjetlo, soli ove tvari često koriste pirotehničke formule. Iako su nitrati i klorati češći od sulfata, potonji se široko koristi kao sastavni dio pirotehničkih stroboskopskih svjetala.
Radiokontrastni lijekovi
Barijev sulfat je radiopaque agent koji se koristi za dijagnosticiranje određenih medicinskih problema. Budući da su takve tvari neprozirne x zrake (blokirajte ih kao rezultat njihove visoke gustoće), tada se dijelovi tijela u kojima su lokalizirani pojavljuju kao bijele mrlje na rendgenskom filmu. To stvara potrebnu razliku između jednog (dijagnostičkog) organa i drugih (okolnih) tkiva. Kontrast će pomoći liječniku da vidi bilo koje posebne uvjete koji mogu postojati u ovom organu ili dijelu tijela.

Barijev sulfat se uzima usta ili rektalno s klistirom. U prvom slučaju, nepropustan je za rendgenske zrake jednjak, želudac ili tanko crijevo. Tako se mogu fotografirati. Ako se tvar primjenjuje pomoću klistira, tada se crijevo ili crijevo mogu vidjeti i fiksirati rendgenskim zrakama.
Doza barijevog sulfata će biti različita za različite pacijente, sve ovisi o vrsti testa. Lijek je dostupan u obliku posebne medicinske barijeve suspenzije ili tableta. Različiti testovi koji zahtijevaju kontrast i rendgensku opremu zahtijevaju različite količine suspenzije (u nekim slučajevima potrebno je uzeti lijek u obliku tableta). Kontrast treba koristiti samo pod izravnim nadzorom liječnika.