20 amino kiselina: imena, formule, vrijednost. Alanin, valin, serin, lizin, prolin, tirozin
Kemikalije koje sadrže strukturne komponente molekule karboksilne kiseline i amina nazivaju se aminokiseline. Ovo je uobičajeno ime grupe. organski spojevi koji sadrži ugljikovodični lanac, karboksilnu skupinu (-COOH) i amino skupinu (-NH2). Njihovi prekursori su karboksilne kiseline, a molekule u kojima je vodik na prvom ugljikovom atomu zamijenjen amino skupinom nazivaju se alfa-amino kiseline.
Samo je 20 aminokiselina vrijedno za enzimatske reakcije biosinteze koje se javljaju u organizmu svih živih bića. Te se tvari nazivaju standardnim aminokiselinama. Tu su i nestandardne aminokiseline, koje su uključene u sastav nekih posebnih proteinskih molekula. Oni se ne nalaze svugdje, iako u prirodi imaju važnu funkciju. Vjerojatno su radikali ovih kiselina modificirani već nakon biosinteze.
Opće informacije i popis tvari
Postoje dvije velike skupine aminokiselina koje su izolirane zbog zakona njihove prisutnosti u prirodi. Konkretno, postoji 20 aminokiselina standardnog tipa i 26 nestandardnih aminokiselina. Prvi se nalaze u sastavu proteina bilo kojeg živog organizma, dok su drugi specifični za pojedine žive organizme.
20 standardnih aminokiselina podijeljeno je u 2 tipa ovisno o sposobnosti sintetiziranja u ljudskom tijelu. To su međusobno zamjenjive, koje se u ljudskim stanicama mogu formirati iz prekursora, i nezamjenjive, za sintezu kojih nema enzimskih sustava ili supstrata. Zamjenjive aminokiseline možda neće biti prisutne u hrani, kao što njihovo tijelo može sintetizirati, i po potrebi dopuniti njihovu količinu. Esencijalne aminokiseline tijelo ne može dobiti samostalno i stoga mora doći iz hrane.
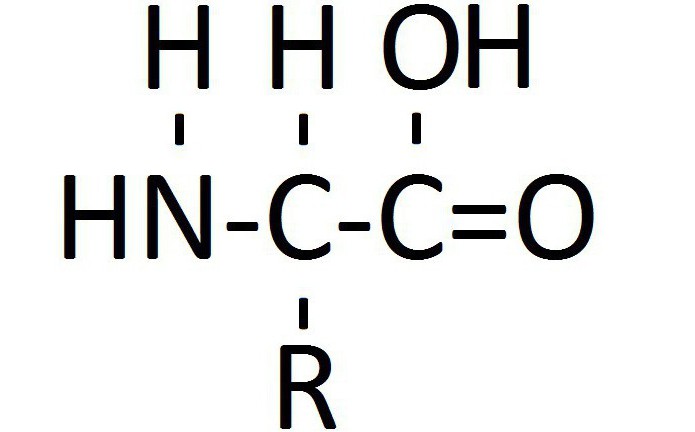
Biokemičari su definirali nazive amino kiselina iz skupine esencijalnih. Ukupno je poznato 8:
- metionin;
- treonin;
- izoleucin;
- leucin;
- fenilalanin;
- triptofan;
- valin;
- lizin;
- također često uključuju histidin.
To su tvari različite strukture ugljikovodičnog radikala, ali nužno s prisutnošću karboksilne skupine i amino skupine na alfa-C-atomu.
U skupini zamjenjivih aminokiselina nalazi se 11 tvari:
- alanin;
- glicin;
- arginin;
- asparagin;
- asparaginska kiselina;
- cistein;
- glutaminsku kiselinu;
- glutamin;
- prolin;
- serin;
- tirozin.
U osnovi, njihova je kemijska struktura jednostavnija od one nezamjenjive, pa je njihova sinteza olakšana tijelu. Većina esencijalnih aminokiselina ne može se dobiti samo zbog odsutnosti supstrata, odnosno molekule prekursora kroz reakciju transaminacije.
Glicin, alanin, valin
U biosintezi molekula proteina najčešće se koriste glicin, valin i alanin (formula svake supstance prikazana je na slici ispod). Ove aminokiseline su najjednostavnije u kemijskoj strukturi. Tvar glicin je najjednostavnija u klasi aminokiselina, to jest, osim alfa-ugljikovog atoma, spoj nema radikala. Međutim, čak i najjednostavnija struktura molekule ima važnu ulogu u održavanju života. Posebno, hemoglobin porfirinski prsten i purinske baze sintetizirani su iz glicina. Porfirni prsten je proteinski dio hemoglobina, dizajniran za držanje atoma željeza u sastavu cijele tvari.
Glicin je uključen u osiguravanje funkcioniranja mozga, djelujući kao inhibitorni posrednik središnjeg živčanog sustava. To znači da je više uključen u rad moždane kore - najteže organizirano tkivo. Još važnije, glicin je supstrat za sintezu purinskih baza, potrebnih za formiranje nukleotida koji kodiraju nasljedne informacije. Osim toga, glicin služi kao izvor za sintezu još 20 aminokiselina, dok se sam može formirati iz serina.
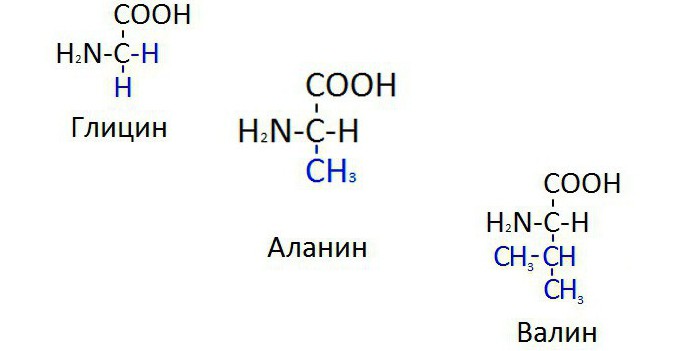
Formula aminokiseline alanin je nešto složenija od glicina, budući da ima metil radikal koji je zamijenjen s jednim atomom vodika na alfa ugljikovom atomu tvari. Istovremeno, alanin ostaje jedna od najčešće uključenih molekula u biosintezi proteina. Ona je dio bilo kojeg proteina u prirodi.
Valin, koji ne može sintetizirati u ljudskom tijelu, je aminokiselina sa razgranatim ugljikovodičnim lancem koji se sastoji od tri ugljikova atoma. Izopropilni radikal daje molekuli veću težinu, ali zbog toga je nemoguće pronaći supstrat za biosintezu u stanicama ljudskih organa. Stoga valin nužno mora potjecati iz hrane. Prisutan je uglavnom u strukturnim mišićnim proteinima.
Rezultati istraživanja potvrđuju da je valin neophodan za funkcioniranje središnjeg živčanog sustava. Posebno, zbog svoje sposobnosti da obnovi mijelinsku ovojnicu živčanih vlakana, može se koristiti kao pomoć u liječenju multiple skleroze, ovisnosti o drogama i depresije. Nalazi se u velikim količinama u mesnim proizvodima, riži, suhom grašku.
Tirozin, histidin, triptofan
U tijelu se tirozin može sintetizirati iz fenilalanina, iako dolazi u velikim količinama od mliječnih proizvoda, uglavnom iz skute i sireva. Uključeno u kazein - životinjski protein koji se nalazi u suhom siru i proizvodima od sira. Ključna vrijednost tirozina je da njegova molekula postaje supstrat za sintezu kateholamina. To su adrenalinski, norepinefrin, dopamin - medijatori humoralnog sustava regulacije tjelesnih funkcija. Tirozin može brzo prodrijeti i proći krvno-moždana barijera, gdje se brzo pretvara u dopamin. Molekula tirozina je uključena u sintezu melanina, osiguravajući pigmentaciju kože, kose i šarenice.
Aminokiselina histidina dio je strukturnih i enzimatskih proteina u tijelu, supstrat za sintezu histamina. Potonji regulira izlučivanje želuca, sudjeluje u imunološkim reakcijama, regulira zacjeljivanje ozljeda. Histidin je esencijalna aminokiselina, a tijelo obnavlja rezerve samo iz hrane.
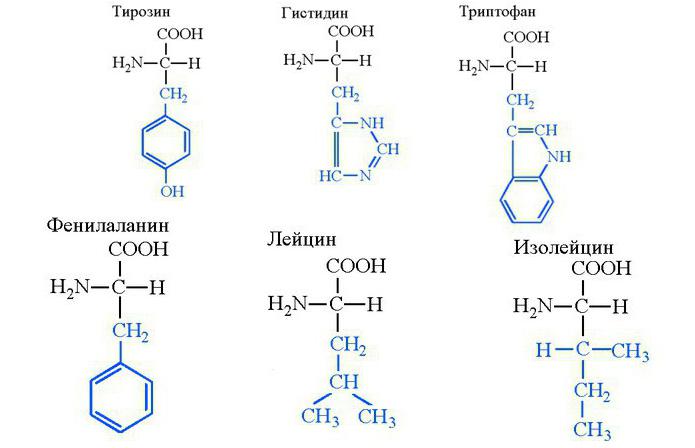
Tijelo ne može sintetizirati i triptofan zbog složenosti lanca ugljikovodika. Ona je dio proteina i supstrat za sintezu serotonina. Potonji je posrednik živčanog sustava, osmišljen da regulira cikluse budnosti i sna. Triptofan i tirozin - neurofiziolozi moraju zapamtiti ta imena aminokiselina jer se od njih sintetiziraju glavni medijatori limbički sustav (serotonin i dopamin), osiguravajući prisutnost emocija. U isto vrijeme, ne postoji molekularna forma koja osigurava nakupljanje esencijalnih aminokiselina u tkivima, zbog čega moraju biti prisutni u hrani dnevno. Proteinska hrana u količini od 70 grama dnevno u potpunosti zadovoljava te potrebe tijela.
Fenilalanin, leucin i izoleucin
Fenilalanin je izvanredan po tome što sintetizira aminokiselinu tirozin s njegovim nedostatkom. Fenilalanin je sama po sebi strukturna komponenta svih proteina u prirodi. To je metabolički prekursor feniletilamina neurotransmitera koji osigurava mentalnu koncentraciju, podizanje raspoloženja i psihostimulaciju. U Ruskoj Federaciji u koncentraciji većoj od 15%, promet ove tvari je zabranjen. Učinak feniletilamina sličan je učinku amfetamina, međutim, prvi se ne razlikuje po svojim štetnim učincima na tijelo i razlikuje se samo u razvoju psihološke ovisnosti.
Jedna od glavnih tvari aminokiselinske skupine je leucin, iz kojeg se sintetiziraju peptidni lanci bilo kojeg ljudskog proteina, uključujući enzime. Spoj koji se koristi u svom čistom obliku može regulirati funkcije jetre, ubrzati regeneraciju svojih stanica i omogućiti pomlađivanje tijela. Stoga je leucin aminokiselina koja je dostupna kao lijek. Vrlo je učinkovit u pomoćnom liječenju ciroze jetre, anemije i leukemije. Leucin je aminokiselina koja uvelike olakšava rehabilitaciju pacijenata nakon kemoterapije.

Izoleucin, kao i leucin, tijelo ne može samostalno sintetizirati i pripada skupini esencijalnih. Međutim, ova tvar nije lijek, jer tijelo ima malu potrebu u njoj. U osnovi, samo jedna od njegovih stereoizomera (2S, 3S) -2-amino-3-metilpentanska kiselina je uključena u biosintezu.
Prolin, serin, cistein
Tvar prolin je aminokiselina s cikličkim ugljikovodičnim radikalom. Njegova glavna vrijednost je u prisutnosti ketonske skupine lanca, zbog čega se supstanca aktivno koristi u sintezi strukturnih proteina. Redukcija ketona heterocikla u hidroksilnu skupinu da se dobije hidroksiprolin tvori višestruke vodikove veze između lanaca kolagena. Kao rezultat, niti ovog proteina su zajedno tkane i daju jaku intermolekularnu strukturu.
Proline - aminokiselina koja osigurava mehaničku snagu ljudskog tkiva i njegovog kostura. Najčešće se nalazi u kolagenu, koji je dio kostiju, hrskavice i vezivno tkivo. Kao i prolin, cistein je amino kiselina iz koje se sintetizira strukturni protein. Međutim, to nije kolagen, već skupina alfa-keratinskih tvari. Oni tvore stratum corneum kože, nokte, uključeni su u sastav kose ljuske.
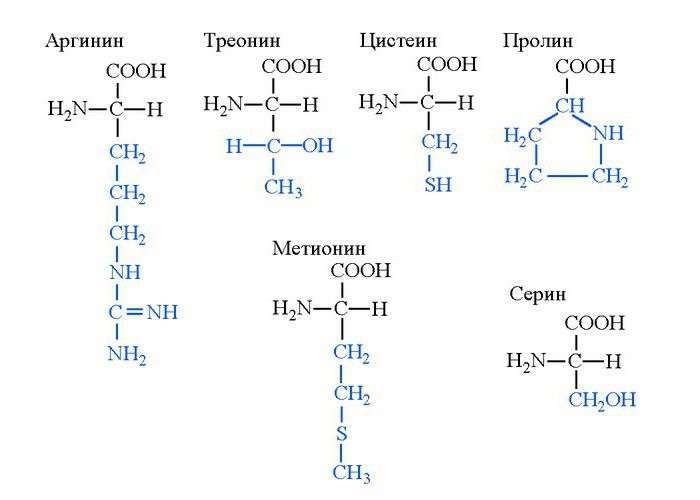
Supstanca serin je aminokiselina koja postoji kao optički L i D-izomeri. To je zamjenjiva tvar sintetizirana iz fosfoglicerata. Serin može nastati tijekom enzimske reakcije iz glicina. Ova interakcija je reverzibilna, pa se glicin može formirati iz serina. Glavna vrijednost ovog posljednjeg je da se enzimski proteini, točnije njihovi aktivni centri, sintetiziraju iz serina. Široko je prisutan serin u sastavu strukturnih proteina.
Arginin, metionin, treonin
Biokemičari su utvrdili da prekomjerna konzumacija arginina izaziva razvoj Alzheimerove bolesti. Međutim, uz negativnu vrijednost tvari prisutne su i vitalne funkcije za reprodukciju. Naročito, zbog prisutnosti gvanidinske skupine koja je smještena u stanici u kationskom obliku, spoj je sposoban formirati veliku količinu intermolekularnih veza vodika. Zbog toga arginin u obliku zwitteriona stječe sposobnost vezanja s fosfatnim regijama molekula DNA. Rezultat interakcije je stvaranje višestrukih nukleoproteina - oblik pakiranja DNA. Arginin se tijekom promjene pH nuklearnog matriksa stanice može odvojiti od nukleoproteina, osiguravajući odvijanje lanca DNA i početak translacije za biosintezu proteina.
Aminokiselina metionin u svojoj strukturi sadrži atom sumpora, zbog čega čista supstanca u kristalnom obliku ima neugodan truli miris zbog emitiranja sumporovodika. U ljudi metionin obavlja regenerativnu funkciju, potičući zacjeljivanje membrana jetrenih stanica. Stoga se proizvodi u obliku aminokiselinskog lijeka. Metionin se sintetizira, a drugi lijek namijenjen dijagnozi tumora. Sintetizira se zamjenom jednog atoma ugljika sa izotopom C11. U ovom obliku aktivno se nakuplja u tumorskim stanicama, što omogućuje određivanje veličine moždanih neoplazmi.
Za razliku od gore navedenih aminokiselina, treonin je manje važan: aminokiseline se ne sintetiziraju iz njega, a njegov sadržaj u tkivima je mali. Glavna vrijednost treonina - uključivanje proteina. Ova amino kiselina nema specifične funkcije.
Asparagin, lizin, glutamin
Asparagin je uobičajena, zamjenjiva aminokiselina koja je prisutna kao L-izomer slatkog okusa i gorki D-izomer. Proteini u tijelu nastaju iz asparagina, a oksaloacetat se sintetizira glukoneogenezom. Ova tvar može oksidirati u ciklusu trikarboksilne kiseline i proizvesti energiju. To znači da osim strukturne funkcije asparagin obavlja i energetsku funkciju.
Nije moguće sintetizirati u ljudskom tijelu lizin je aminokiselina s alkalnim svojstvima. Uglavnom se radi o sintetiziranim imunskim proteinima, enzimima i hormonima. U isto vrijeme, lizin je aminokiselina koja neovisno razvija antivirusna sredstva protiv virusa herpesa. Međutim, tvar se ne koristi kao lijek.
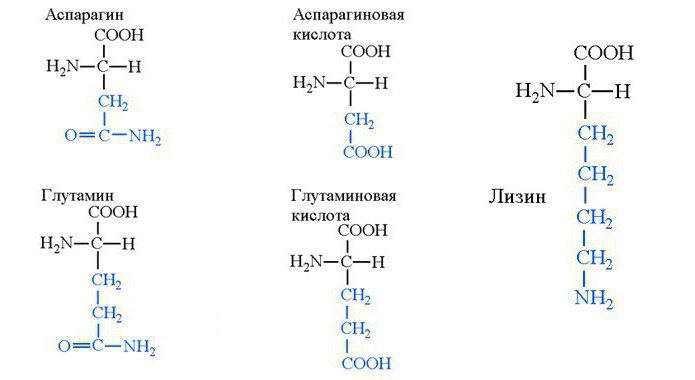
Aminokiselina glutamin je prisutna u krvi u koncentracijama daleko većim od sadržaja drugih aminokiselina. Ona igra važnu ulogu u biokemijskim mehanizmima metabolizma dušika i izlučivanja metabolita, sudjeluje u sintezi nukleinske kiseline enzimi, hormoni, mogu ojačati imunološki sustav, iako se ne koristi kao lijek. No, glutamin se široko koristi među sportašima, jer pomaže u oporavku od treninga, uklanja metabolite dušika i butiraje iz krvi i mišića. Ovaj mehanizam za ubrzavanje oporavka sportaša ne smatra se umjetnim i nije ispravno priznat kao doping. Osim toga, ne postoje laboratorijske metode za otkrivanje sportaša u takvom dopingu. Glutamin je također prisutan u značajnim količinama u hrani.
Asparaginsku i glutaminsku kiselinu
Asparaginske i glutaminske aminokiseline izuzetno su vrijedne za ljudsko tijelo zbog svojih svojstava koja aktiviraju neurotransmitere. One ubrzavaju prijenos informacija između neurona, osiguravajući održavanje učinkovitosti moždanih struktura koje leže ispod korteksa. U takvim strukturama važna je pouzdanost i konzistentnost, jer ti centri reguliraju disanje i cirkulaciju krvi. Dakle, u krvi postoji ogromna količina aspartinske kiseline i aminokiseline glutamina. Prostorna strukturna formula aminokiselina prikazana je na slici ispod.
Aspartinska kiselina je uključena u sintezu uree, eliminirajući amonijak iz mozga. To je značajna supstanca za održavanje visoke stope reprodukcije i obnove krvnih stanica. Naravno, uz leukemiju, ovaj mehanizam je štetan, pa se, radi postizanja remisije, koriste preparati enzima koji uništavaju aspartinsku aminokiselinu.
Jedna četvrtina broja svih aminokiselina u tijelu je glutaminska kiselina. To je neurotransmiter postsinaptičkih receptora, potrebnih za sinaptičko prenošenje impulsa između procesa neurona. Međutim, glutaminsku kiselinu karakterizira ekstra-sinaptički način prijenosa informacija - volumetrijska neurotransmisija. Ova metoda je osnova pamćenja i neurofiziološka zagonetka, jer još nije jasno koji receptori određuju količinu glutamata izvan stanice i izvan sinapsi. Međutim, pretpostavlja se da je količina tvari izvan sinapse važna za masovnu neurotransmisiju.
Kemijska struktura
Sve nestandardne i 20 standardnih aminokiselina imaju zajednički plan strukture. Uključuje ciklički ili alifatski ugljikovodični lanac sa ili bez radikala, amino skupinu na alfa ugljikovom atomu i karboksilnu skupinu. Ugljikovodični lanac može biti bilo koji, tako da tvar ima reaktivnost aminokiselina, važno je mjesto glavnih radikala.
Amino skupina i karboksilna skupina moraju biti vezane na prvi ugljikov atom u lancu. Prema nomenklaturi usvojenoj u biokemiji, ona se naziva alfa atom. Važan je za formiranje peptidne skupine - najvažnije kemijske veze zbog koje postoji protein. S točke gledišta biološke kemije, život se naziva načinom postojanja proteinskih molekula. Glavna vrijednost aminokiselina je stvaranje peptidne veze. U članku je prikazana opća strukturna formula aminokiselina.
Fizička svojstva
Unatoč sličnoj strukturi ugljikovodičnog lanca, aminokiseline su značajno različite u fizikalnim svojstvima od karboksilnih kiselina. Na sobnoj temperaturi, to su hidrofilne kristalne tvari koje se dobro otapaju u vodi. U organskom otapalu zbog disocijacije na karboksilnoj skupini i uklanjanju protona, aminokiseline se slabo otapaju, tvoreći smjese tvari, ali ne i stvarna rješenja. Mnoge aminokiseline imaju slatki okus, dok su karboksilne kiseline - kisele.
Ta fizikalna svojstva su posljedica prisutnosti dvije funkcionalne kemijske skupine, zbog čega se tvar u vodi ponaša kao otopljena sol. Pod djelovanjem molekula vode proton se cijepa iz karboksilne skupine, čiji je akceptor amino skupina. Zbog pomicanja elektronske gustoće molekule i odsutnosti pH protona (indeksa kiselosti), otopina ostaje prilično stabilna pri dodavanju kiselina ili lužina s visokim konstantama disocijacije. To znači da su aminokiseline sposobne formirati slabe puferske sustave, održavajući homeostazu tijela.
Važno je da modul naboja disocirane molekule aminokiselina bude nula, budući da se proton koji se odvaja od hidroksilne skupine uzima dušikov atom. Međutim, na dušiku u otopini formira se pozitivan naboj, a na karboksilnoj skupini formira se negativni naboj. Sposobnost disocijacije izravno ovisi o kiselosti, te stoga za otopine aminokiselina postoji izoelektrična točka. To je pH (indeks kiselosti) kod kojeg najveći broj molekula ima nulti naboj. U tom stanju, oni su stacionarni u električnom polju i ne provode struju.