Nenormalna svojstva vode: uzroci, značaj
Ljudi su naviknuti na vodu i smatraju je običnom supstancom. Često je uzimaju zdravo za gotovo dok suša ugrožava usjeve i pitku vodu, ili ozbiljne poplave predstavljaju prijetnju životu i imovini. Mnogi ne shvaćaju da struktura vode i njezine anomalne osobine osiguravaju postojanje života na Zemlji.
Jedan od ranih grčkih filozofa, Tales iz Mileta (640-546 pne. E.), Istraživao univerzalnu prirodu vode. Smatrao ga je glavnim elementom iz kojeg se sve rađa. Obilje vode bilo je očito, ali Thales je primijetio da je to jedina tvar koja je prirodno prisutna na Zemlji u isto vrijeme u tri različita stanja: čvrsta, tekuća i plinovita. U hladni zimski dan, snijeg i led prekrivaju polja, u blizini teče rijeka, a oblaci lebde iznad njih.
Oblici materije
Sve tvari postoje u tri različita stanja, koja ovise o temperaturi i tlaku. Krute tvari imaju određeni oblik i imaju kristalnu unutarnju strukturu. Prema ovoj definiciji, tvar poput stakla smatrat će se vrlo viskoznom tekućinom, budući da nema kristalnu strukturu. Čvrste tvari su otporne na vanjske utjecaje. Mogu se pretvoriti u tekućinu grijanjem. Točka smrzavanja vode pri tlaku od 1 atmosfere je 0 ° C, ispod koje postoji kao led.
Tekućina, za razliku od čvrstog tijela, nema čvrstoću i nema određeni oblik. Ima volumen i ima oblik posude u kojoj je pohranjen. Vanjski utjecaj prisiljava ga da teče. Voda je tekućina između temperature smrzavanja i vrenja (100 ° C). Tekućine se mogu prenijeti u plinovitu fazu kada se zagriju iznad točke vrenja.
Plin nema oblik ili volumen. Ima oblik i zauzima volumen posude u kojoj se nalazi. Plin se širi i skuplja s promjenama temperature i tlaka i lako se može difundirati u druge plinove.

Točke vrenja i smrzavanja
Nenormalna svojstva vode su njezine neuobičajeno visoke temperature vrenja i temperature smrzavanja u usporedbi s drugim spojevima slične molekularne strukture. Ostale slične tvari u normalnim uvjetima su plinovi. Očekuje se da voda s nižom molekularnom težinom od sličnih spojeva ima niže temperature vrenja i smrzavanja. Međutim, zbog polarne prirode njegovih molekula i vodikovih veza, vrelište je 100 ° C, a smrzavanje je 0 ° C. Za usporedbu, odgovarajuće vrijednosti za vodikov sulfid H 2 S su -60 ° C i -84 ° C, za vodikov sulfid H 2 Se, ovaj pokazatelj je -42 ° C i -64 ° C, a telurid za -2 ° C i -49 ° C ,
Čvrsta faza
U pravilu, uz smanjenje temperature, tvari postaju guste, a voda nije iznimka. Njegova gustoća na 25 ° C je 0.997 g / ml i povećava se do maksimuma (1 g / ml) na T = 4 ° C. U metričkom mjernom sustavu, kilogram se definira kao masa 1 litre vode s maksimalnom gustoćom. Nevjerojatna stvar se događa između 4 ° C i točke smrzavanja od 0 ° C, što se vidi u vrlo malom broju tvari. Voda se postupno širi i postaje manje gusta. Gustoća leda na 0 ° C je oko 0,917 g / ml. Molekule vode oblikuju kristale u obliku tetraedra (četverokutna figura, od kojih je svako lice jednakostraničan trokut). Budući da je gustoća čvrste faze manja od tekuće, led lebdi. Kada se smrzne, količina vode se povećava za 1%.
Vrlo je važno da se led širi i pluta na površini. Zbog toga se zimi puknu vodovodne cijevi i na cestama se pojave rupe. Zamrzavanje i topljenje vode u velikoj su mjeri odgovorni za uništavanje stijena i formiranje tla. Osim toga, ako se jezera i potoci zamrznu prema gore, vodeni život općenito bi prestao postojati, a klimatski i vremenski uvjeti dramatično bi se promijenili.

Kapacitet grijanja
Još jedna abnormalna svojstva vode je njegova iznimno visoka sposobnost apsorpcije topline bez značajnog povećanja temperature. Primjerice, ljetno sunce na plaži zagrijava pijesak do te mjere da je nemoguće hodati po njemu. Voda ostaje hladna. Obje tvari apsorbiraju jednaku količinu toplinske energije, ali je temperatura pijeska veća. Prazna gvozdena posuda koja visi iznad vatre brzo će zasvijetliti, ali ako je napunjena vodom, ona se postupno zagrijava. Visoki toplinski kapacitet vode čini ga dobrim rashladnim sredstvom u kondenzatorima i radijatorima automobila koji sprječavaju pregrijavanje motora. Njegova vrijednost je 5 puta veća od toplinskog kapaciteta pijeska i oko 10 puta veća od željeza.
Umjerena klima u obalnim područjima rezultat je apsorpcije tijekom dana velike količine solarne toplinske energije vodom i sporog oslobađanja tijekom noći. Kopnena područja udaljena od obale obično imaju mnogo veće ekstremne temperature. Ogromni oceani na Zemlji (oko 75% površine) odgovorni su za ublažavanje klime na našem planetu, podržavajući postojanje života.
Toplina topljenja i isparavanja
Toplina faznog prijelaza povezana je s toplinskim kapacitetom. To je količina toplinske energije koja se apsorbira ili oslobađa od strane tvari koja se mijenja u fazi (od tekućeg u kruto, ili obrnuto, i od tekućeg do plinovitog, ili obrnuto) bez promjene temperature. Neuobičajeno visoke vrijednosti specifične topline taljenja (332,4 kJ / kg) i isparavanja (2256,2 kJ / kg) sljedeće su anomalije fizikalnih svojstava vode. Zamrzavanje proizvodi istu količinu topline koja se apsorbira tijekom procesa taljenja.

Praktičan primjer korištenja specifične topline taljenja vode je korištenje leda za hlađenje pića u izoliranom hladnjaku. U procesu topljenja leda apsorbira toplinsku energiju pića, održavajući ih hladnima. Spremnik s vodom u stakleniku u hladnoj zimskoj noći omekšat će temperaturu u prostoriji zbog topline koja se oslobađa tijekom zamrzavanja. Kondenzacija pare otpušta istu količinu topline koja se apsorbira tijekom procesa isparavanja. Specifična toplina isparavanja je 5 puta veća od topline potrebne za podizanje temperature od 0 do 100 ° C. Nenormalno svojstvo vode za pohranjivanje velike količine akumulirane toplinske energije čini učinkovito parno grijanje. U procesu kondenzacije para otpušta akumuliranu toplinsku energiju. Dnevna grmljavina na vrući ljetni dan još je jedan primjer oslobađanja toplinske energije u gornjoj atmosferi tijekom kondenzacije vrućeg, vlažnog zraka. Čak i uragan je primjer učinka preraspodjele ogromne količine toplinske energije koju apsorbiraju tropski oceani.
Sustavi hlađenja isparavanjem rade obrnuto. Voda u procesu isparavanja upija toplinsku energiju iz zraka, hladi je.
Univerzalni otapalo
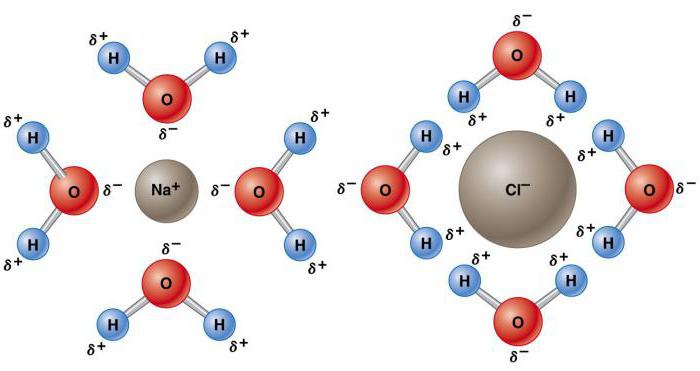
Otapalo je sposobno otopiti drugu tvar s nastankom homogene smjese (otopine) na molekularnoj razini. Još jedna abnormalna svojstva vode u kemiji zbog svoje polarne prirode je sposobnost otapanja drugih polarnih spojeva - soli, alkohola, karboksilnih spojeva, itd. Više se tvari otapa u vodi nego u bilo kojem drugom otapalu. U njemu se nalazi više od polovice poznatih kemijskih elemenata, neki u visokim koncentracijama, a drugi samo u tragovima. Na primjer, koncentracija zasićenja natrijeva klorida je oko 36 g na 100 ml, a kalcijev karbonat - oko 0,0015 g. Sposobnost vode da otopi tvar ovisi o njezinom kemijskom sastavu, snazi kemijskih veza elemenata, temperaturi i pH.
Nepolarni spojevi, uključujući većinu ugljikovodika, otapaju se u niskim ili u tragovima. Na primjer, ulja teže plutati na površini vode.

Površinska napetost
Nenormalna svojstva vode uključuju njezinu najveću (nakon žive) površinsku napetost u usporedbi s bilo kojom drugom tekućinom. To je snaga privlačenja molekula koje se nalaze ispod površine i one smještene na sučelju tekućina-zrak. To sprječava širenje vode. Polarni spojevi, u pravilu, imaju mnogo veću površinsku napetost od nepolarnih. I voda nije iznimka. Na 20 ° C, ovaj pokazatelj je jednak 0,07286 N / m (za etil alkohol - 0,0228 N / m).
Bez vanjskog utjecaja, kapljica H 2 O poprima oblik kugle, budući da ova brojka ima najmanju površinu po jedinici volumena. Kišne kapi su sićušni metci koji uništavaju stijene. Iz istog razloga, predmeti koji su teži od vode mogu se držati na njegovoj površini. Insekti mogu hodati po njemu, a britvice plivati.
Vodikova veza određuje anomalijsko svojstvo vode da mokre većinu površina. Takve tvari se smatraju hidrofilnim. Voda može rasti duž zidova stakla i drugih spremnika. Ostale tvari, kao što su ulja, masti, voskovi i sintetika (polipropilen, itd.), Ne smiju se smočiti. Oni su hidrofobni. Patrone s membranskim filterom s veličinom pora manjom od 1 mikrona izrađene su od hidrofobnih polimera uz pomoć sredstava za vlaženje koja smanjuju površinsku napetost vode tako da ona može prodrijeti i ostati u njima. Ovaj fenomen naziva se kapilarni učinak. On je odgovoran za kretanje vode u tlu i uz korijenje biljaka i krvi kroz krvne žile.

Nenormalna svojstva vode i njihova važnost za život
H 2 O je sastavni dio postojanja cijelog života. To objašnjava nedavni interes za pronalaženje vode u drugim dijelovima svemira. Svi poznati biokemijski procesi odvijaju se u vodenom okolišu. Većina živih bića sadrži 70–80% H 2 O po težini.
Osim toga, voda igra značajnu ulogu u procesu fotosinteze. Biljke koriste zračnu energiju sunca za pretvaranje vode i ugljičnog dioksida u ugljikohidrate: 6CO2 + 6H2O + 672 kcal → C6H12O6 + 6O2. Fotosinteza je najosnovnija i najvažnija kemijska reakcija na Zemlji. On daje izravno ili neizravno hranjive tvari svim živim organizmima i glavni je izvor atmosferskog kisika.
Nenormalna svojstva vode i njihovi uzroci
Sposobnost elemenata da formiraju spojeve ovisi o sposobnosti njihovih atoma da doniraju ili prihvaćaju elektrone. Elementi prvog tipa postaju pozitivno nabijeni ioni (kationi), a drugog tipa - negativno nabijeni anioni.
Sposobnost elementa da stupi u interakciju s drugim elementima u obliku spojeva naziva se valencija. Odgovara broju primljenih ili odaslanih elektrona. Za anorganske spojeve, algebarski zbroj valentnih brojeva elemenata je nula. Naziva se elektrostatička privlačnost suprotno nabijenih iona da se dobije spoj ionske veze.
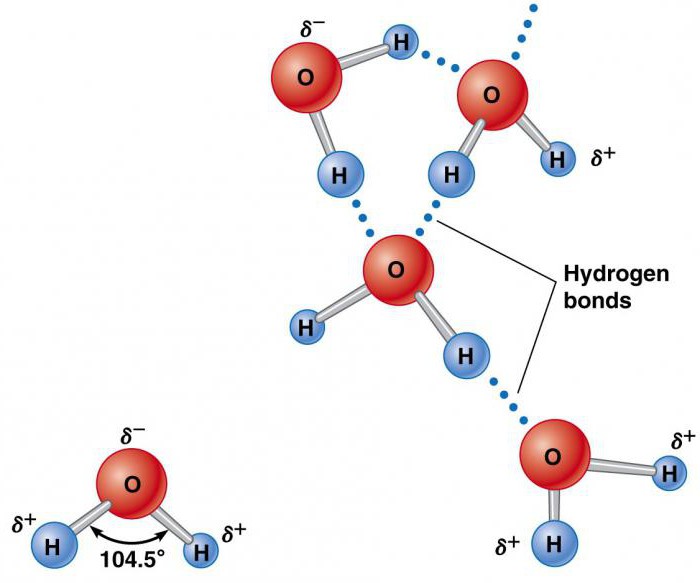
Elementi koji tvore vodu (vodik i kisik) postoje zasebno u molekulama H2 i O2 koje sadrže po dva atoma. Oni se drže zajedno razmjenom elektronskog para u kemijskoj vezi nazvanoj kovalentna veza. Mnogo je jači od iona. Dva atoma držana zajedno kovalentnu vezu oblikuju mnogo stabilniju molekulu od njezinih sastavnih dijelova. U njoj se vodik kombinira kisikom preko uobičajenih elektronskih parova. Ova jedinstvena raspodjela elektrona u dobivenom kemijskom spoju uzrokuje da se H-atomi pozicioniraju u odnosu na O pod kutom od 104,5 °.
Nenormalna fizikalna svojstva vode objašnjavaju se njezinom strukturom i kemijskom vezom.
Atom kisika ima relativno snažan učinak na ukupan par elektrona, tako da atomi vodika postaju elektropozitivni, a atom kisika elektronegativna regija. Budući da su pozitivna i negativno nabijena područja nejednako raspodijeljena s obzirom na središnju točku, molekula vode je polarna.
Takva njegova priroda čini elektrostatički privlačnim za druge H 2 O molekule, kao i ione i kontaktne površine s naelektrisanim područjima. Elektropozitivni atomi vodika privlače elektronegativni atomi kisika susjednih molekula vode. Ovaj fenomen naziva se vodikova veza. Njegova snaga je samo oko 10% kovalentna, ali je odgovorna za većinu anomalnih fizičkih svojstava vode. To uključuje visoke točke smrzavanja i vrenja, toplinski kapacitet, specifičnu toplinu taljenja i isparavanja, topljivost i površinsku napetost.
Vodikova veza je odgovorna za održavanje integriteta H 2 O molekule tijekom kemijskih reakcija. Dok se drugi spojevi podvrgavaju ionizaciji, sama voda zadržava svoj kemijski integritet. Samo relativno mali broj molekula ionizira se u vodikove i hidroksilne ione. Zbog toga je H 2 O relativno slabi vodič električne struje. Specifična otpornost teoretski čiste vode iznosi 18,3 MΩ cm, dok otpornost na piće ima specifični otpor manji od 10 000 ohm cm. Na taj način možete lako provjeriti čistoću H20.
Anomalna svojstva vode objašnjavaju se prisutnošću vodikovih veza, zbog kojih postoji mala gustoća leda. Uz njih se tijekom smrzavanja nalaze molekule, što dovodi do širenja tvari. Iz tog razloga led lebdi na površini vode. Povećani tlak snižava točku taljenja. Pritisak koji stvara oštrica klizaljke utapa led, stvarajući sloj koji pruža elegantno klizanje. Čak i pri ekstremno niskim temperaturama, visoki tlak slabi kristalna rešetka. Zbog toga se postupno kreću ogromne ledene mase, poput ledenjaka.
Dipolni trenutak
Polarna priroda molekule vode čini ga orijentiranim u električnom ili magnetskom polju. Elektronegativni atom kisika poravnan je s pozitivnim polom, a elektropozitivni atomi vodika - u negativnom smjeru. Voda ima iznimno velik dipolni moment, koji je produkt udaljenosti između naboja pomnožene s količinom naboja.
Dielektrična konstanta je drugo svojstvo povezano s dipolnim momentom. Molekule vode poravnavanjem u električnom polju teže neutraliziranju i stvaranju otpora prijenosu elektrostatičkog naboja. Dielektrična konstanta tvari određena je ε u jednadžbi F = Q1 2 Q2 / ε, r 2 , pri čemu je F sila između dva naboja Q, podijeljena udaljenosti r u mediju.
Kako dielektrična konstanta raste, sila između naboja se smanjuje. Visoka dielektrična konstanta smanjuje atraktivnu snagu iona, što objašnjava anomalijska kemijska svojstva vode za otapanje raznih tvari.
zaključak
Za ljude, voda je uobičajena tvar koja se često uzima zdravo za gotovo. Unatoč činjenici da su anomalna svojstva vode objašnjena na atomskoj razini, njezino je značenje doista veliko. Očito je neophodno za postojanje života na Zemlji. Nenormalna svojstva vode, ukratko, omogućuju joj da služi kao posrednik kemijskih i biokemijskih procesa, da oblikuju naše prirodno okruženje i sudjeluju u stvaranju klime i vremena.