Acetilen: kemijska svojstva, priprema, uporaba, mjere opreza
Acetilen (ili, prema međunarodnoj nomenklaturi, etin) je nezasićeni ugljikovodik koji pripada klasi alkina. Kemijska formula acetilena je C2H2. Atomi ugljika u molekuli povezani su trostrukom vezom. On je prvi u svojoj homolognoj seriji. To je bezbojni plin. Vrlo zapaljivo.
recepcija
Sve metode industrijske proizvodnje acetilena konvergiraju se u dvije vrste: hidroliza kalcijevog karbida i piroliza raznih ugljikovodika. Potonji zahtijeva manje energije, ali je čistoća proizvoda prilično niska. Metoda karbida je suprotna.
Suština pirolize je da se metan, etan ili drugi lagani ugljikovodik pretvaraju u acetilen kada se zagrijavaju na visoke temperature (od 1000 ° C). Grijanje se može izvesti električnim pražnjenjem, plazmom ili gorućim dijelom sirovine. No problem je u tome što se kao rezultat reakcije pirolize može formirati ne samo acetilen, nego i mnoge druge proizvode koji se kasnije moraju zbrinuti.
2CH4 → C2H2 + 3H2
Metoda karbida temelji se na reakciji interakcije kalcijevog karbida s vodom. Kalcijev karbid Dobiven je iz njegovog oksida spajanjem s koksom u električnim pećima. Dakle, tako visoka potrošnja energije. Ali čistoća acetilena dobivena na ovaj način je izuzetno visoka (99,9%).
CaC2 + H20 → C2H2 + Ca (OH) 2
U laboratoriju, acetilen se također može dobiti dehidrohalogenacijom dihalogenskih derivata alkana upotrebom alkoholne alkalne otopine.
CH2Cl-CH2Cl + 2KOH → C2H2 + 2KCl + 2H20
Fizikalna svojstva acetilena
Acetilen je plin bez boje i mirisa. Iako mu nečistoće mogu dati miris češnjaka. Praktično netopljiv u vodi, slabo topljiv u acetonu. Na temperaturi od -83,8 ° C ukapljuje se.
Kemijska svojstva acetilena
Na temelju trostruke veze acetilena, bit će karakterizirana reakcijama adicije i reakcije polimerizacije. Atomi vodika u molekuli acetilena mogu se zamijeniti drugim atomima ili skupinama. Stoga se može reći da acetilen pokazuje kiselinska svojstva. Ispitajmo kemijska svojstva acetilena na specifične reakcije.
Reakcije privitka:
- Hidrogenacije. Izvodi se na visokoj temperaturi i u prisutnosti katalizatora (Ni, Pt, Pd). Na paladijskom katalizatoru može biti nepotpuna hidrogenacija.
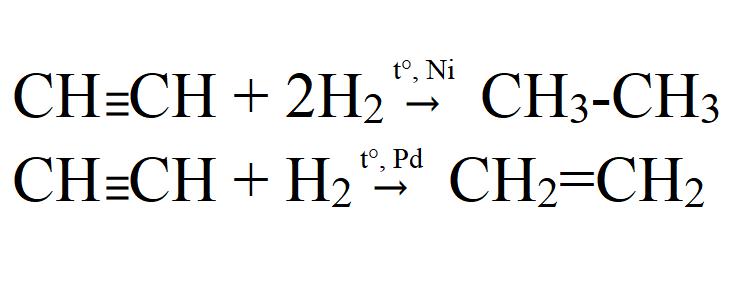
- Halogcniranjm. Može biti i djelomična i potpuna. Lako je i bez katalizatora ili grijanja. U svjetlu kloriranja dolazi s eksplozijom. U isto vrijeme, acetilen se potpuno razlaže na ugljik.
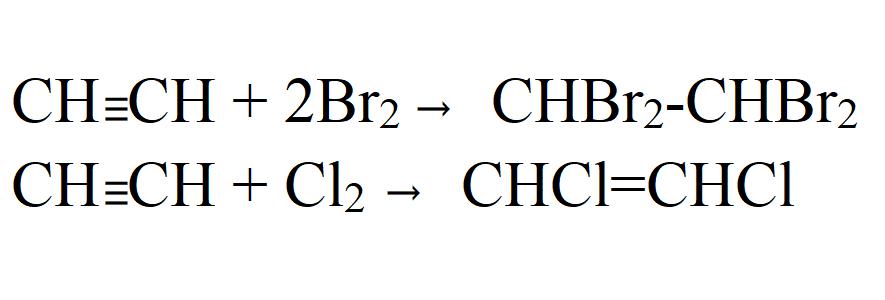
- Pristupanje octenoj kiselini i etilnom alkoholu. Reakcije idu samo u prisutnosti katalizatora.
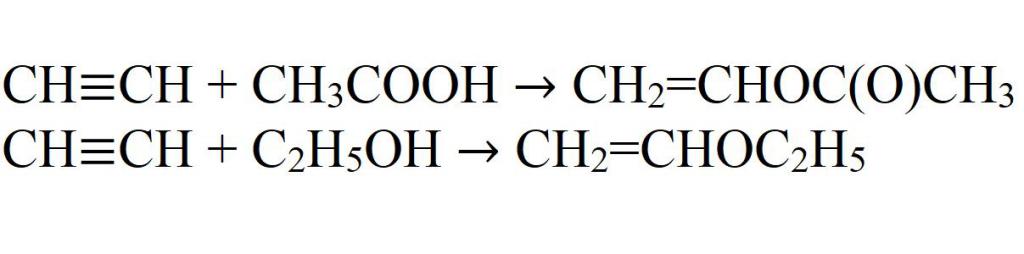
- Dodavanje cijanovodične kiseline.
CH2CH + HCN → CH2 = CH-CN
Reakcije zamjene:
- Interakcija acetilena s metal-organskim spojevima.
CH2CH2C2H5MgBr → 2C2H6 + BrMgC ^ CMGBr
- Interakcija s metalnim natrijem. Potrebna je temperatura od 150 ° C ili prethodno otapanje natrija u amonijaku.
2CH2CH + 2Na → 2CH2CNa + H2
- Interakcija s kompleksnim solima bakra i srebra.
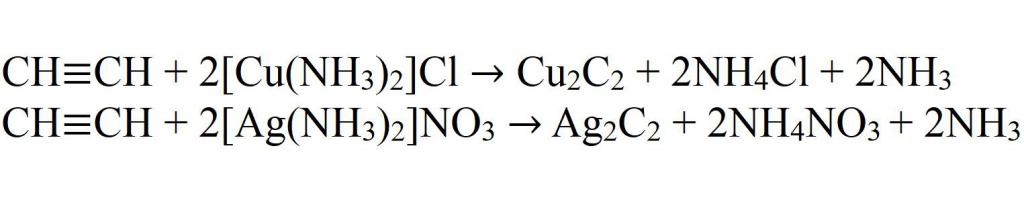
- Interakcija s natrijevim amidom.
CH2CH + 2NaNH2-NaCCNa + 2NH3
Reakcije polimerizacije:
- Dimerizaciju. U ovoj reakciji, dvije acetilenske molekule su spojene u jednu. Potreban je katalizator - monovalentna sol bakra.
- Trimerizacije. U ovoj reakciji, tri molekule acetilena tvore benzen. Potrebno je zagrijavanje do 70 ° C, tlak i katalizator.
- Tetramerization. Kao rezultat reakcije dobiven je osmeročlani ciklus - ciklooktatetren. Ova reakcija također zahtijeva malo topline, tlaka i prikladnog katalizatora. To su obično složeni spojevi dvovalentnog nikla.
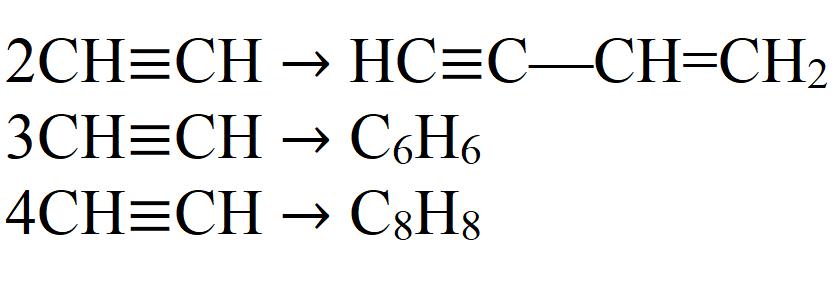
To nisu sva kemijska svojstva acetilena.
primjena
Strukturna formula acetilena pokazuje nam prilično jaku vezu između atoma ugljika. Kada se razbije, primjerice tijekom izgaranja, oslobađa se mnogo energije. Iz tog razloga, acetilenski plamen ima rekordnu temperaturu od oko 4000 ° C. Koristi se u bakljama za zavarivanje i rezanje metala, kao iu raketnim motorima.
Plamen izgaranja acetilena također ima vrlo visoku svjetlinu, pa se često koristi u rasvjetnim uređajima. Koristi se u eksplozivnoj tehnologiji. Istina, ne primjenjuje se sam acetilen, već njegove soli.
Kao što se može vidjeti iz raznih kemijskih svojstava, acetilen se može koristiti kao sirovina za sintezu drugih važnih tvari: otapala, lakova, polimera, sintetičkih vlakana, plastike, organskog stakla, eksploziva i octene kiseline.
sigurnosni
Kao što je već spomenuto, acetilen je zapaljiva tvar. S kisikom ili zrakom može oblikovati izuzetno zapaljive smjese. Da biste izazvali eksploziju, dovoljna je jedna iskra od statičkog elektriciteta, zagrijavanje do 500 ° C ili mali tlak. Na temperaturi od 335 ° C čisti acetilen se spontano zapali.
Zbog toga se acetilen pohranjuje u cilindrima pod tlakom, koji se pune poroznom tvari (plavac, aktivni ugljen, azbest). Tako se acetilen distribuira kroz pore, smanjujući rizik od eksplozije. Često su te pore impregnirane acetonom, zbog čega nastaje acetilenska otopina. Ponekad se acetilen razrijedi s drugim, više inertnim plinovima (dušik, metan, propan).
Ovaj plin također ima toksični učinak. Kada se udahne, započinje trovanje tijela. Znakovi trovanja su mučnina, povraćanje, tinitus i vrtoglavica. Velike koncentracije mogu čak dovesti do gubitka svijesti.