Aluminijev sulfat i drugi aluminijski spojevi u prirodi i ljudskom životu
U svakodnevnom životu, svatko od nas svake minute suočava se s količinom kemikalija koje oduzimaju dah, kako prirodnim tako i samim čovjekom. Osvrnimo se na dva kemijska spoja: aluminijev sulfat, aluminijev hidroksid. Što je to i zašto biste trebali obratiti pozornost na njih?
Da biste se upoznali, morate uzemljiti
Aluminijev sulfat (aluminijev oksid), zajedno s aluminosilikatima i različitim vrstama gline, čini glavninu zemljine kore. To omogućuje aluminijima da zauzmu prvo mjesto među metalima u smislu prevalencije na Zemlji. U prirodi, aluminijev sulfat, formula u kojoj je Al2 (S04) * 18H20, kristalni hidrat i bijeli je topljivi kristal topljiv u vodi sa sivom, plavom ili ružičastom nijansom.

Za razliku od aluminijevog sulfata, njegov hidroksid je bijela krutina, netopiva u vodi. Aluminij sulfat, aluminij hidroksid, kaolinit su široko rasprostranjeni. Minirana su u Sibiru, Krimu, Kini, Japanu, kao iu zemljama Srednje i Južne Amerike.
Zry u epruveti
Da bismo saznali istinu, utvrdit ćemo kakve kemijske značajke imaju sulfat i hidroksid Al. Preformulirajmo frazu Kozme Prutkova "Pogledaj u korijen!" U pragmatičniju: "Pogledaj u epruvetu!"
 Počnimo s Al hidroksidom, koji predstavlja tu tvar na slici Janus s dva lica. Vrlo malo kemijskih spojeva može istovremeno reagirati s kiselinama i lužinama. Takva "dvoličnost" u kemiji naziva se amfoterna. Dakle, u reakcijama aluminijevog hidroksida s kiselinom dobivamo srednje soli.
Počnimo s Al hidroksidom, koji predstavlja tu tvar na slici Janus s dva lica. Vrlo malo kemijskih spojeva može istovremeno reagirati s kiselinama i lužinama. Takva "dvoličnost" u kemiji naziva se amfoterna. Dakle, u reakcijama aluminijevog hidroksida s kiselinom dobivamo srednje soli.

S obzirom na interakciju aluminijevog hidroksida Al (OH) 3 s alkalijama, vodit ćemo računa o uvjetima pod kojima se reakcija događa. Od njih će ovisiti konačni proizvodi:

Sam Al (OH) 3 hidroksid se dobiva u laboratoriju posrednim sredstvima, to jest ne iz oksida i vode, što je u ovom slučaju nemoguće, već iz aluminijeve soli. Da biste to učinili, uzmite otopinu aluminij sulfata i djelovati na njega s alkalijama, kao što je kaustična soda, pažljivo sipanje u kapi.
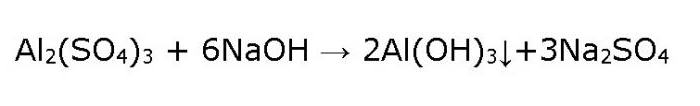
Kao rezultat, bijeli želatinozni precipitat, Al (OH) 3, formira se u epruveti.

Sumirajući sve gore navedene reakcije, dokazujući amfoterni aluminijev hidroksid, zaključujemo: u kiseloj sredini kemijska ravnoteža Ploča se pomiče prema formiranju Al soli, te u alkalnom smjeru, prema formiranju metaaluminata ili hidroksialuminata.
Podržavajuća tradicija
Uzmimo pauzu od poteškoća "dvoličnosti" amfoternog aluminijevog hidroksida i pretvorimo se u tradicionalnu srednju sol - aluminijev sulfat. Nema odstupanja od pravila. Otopine srednjih soli reagiraju s alkalijama, s kiselinama, s drugim solima, s metalima koji stoje u Beketovljevoj seriji (metalni stresni nizovi) do metala, čiji se ion nalazi u molekuli soli. Na primjer, aluminijev sulfat u otopini reagirat će s litijem, kalijem, kalcijem, natrijem i magnezijem. Potvrdite to s jednadžbama reakcije.
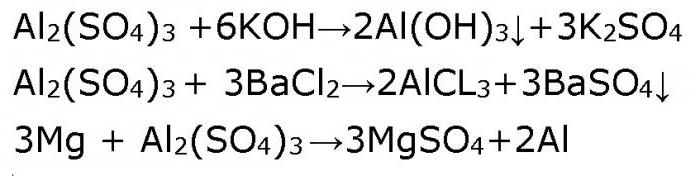
Aluminijev sulfat, čija je formula Al2 (SO4) 3, produkt je interakcije slabe aluminijeve hidroksidne baze Al (OH) 3 i jake sulfatne kiseline H2S04. Zbog toga se lako hidrolizira u vodenoj otopini. Višak vodikovih iona H + detektira se pomoću lakmusovog indikatora, koji mijenja njegovu plavu boju u otopini aluminijevog sulfata do crvene. Stoga smo ustanovili da je otopina aluminijevog sulfata kisela.

Bilo bi moguće i dalje se baviti detaljima ove teme koja su bila ugodna i uzbudljiva za kemičara-estetu, ako je sumnjivo skeptična osoba s pitanjem: "Pa što ću ja imati?"
Doći će u pomoć
Da bismo otklonili sve nedoumice, recimo da već imate mnogo korisnih, pa i vitalnih stvari, zahvaljujući spojevima kao što su aluminijev sulfat, aluminijev hidroksid i drugi reagensi koji sadrže aluminij. Prije svega, Al (OH) 3 se koristi za čišćenje tvrde vode. Nakon tog procesa voda postaje prozirnija i lakša te se oslobađa iz soli koje ga čine teškim.
Losioni, gelovi, tonici pomažu nam da uvijek budemo lijepi i njegovani. Ali oni također sadrže aluminijev sulfat. Široko reklamirana inovacija u industriji antiperspirantne dezodoransa koja se zove "kristali svježine" nije ništa drugo nego aluminijev kalijev aluminij, od čega je komponenta aluminijev sulfat. Spojevi aluminija imaju sposobnost omotanja i stoga se također koriste u proizvodnji višenamjenskih pamučnih tkanina iu farmakologiji.