Kemijska ravnoteža i stvaranje uvjeta za njezino pomicanje
Proučavanje parametara sustava, uključujući početne materijale i produkte reakcije, omogućuje nam da utvrdimo koji faktori pomiču kemijsku ravnotežu i dovode do željenih promjena. Na temelju nalaza Le Chateliera, Browna i drugih znanstvenika o načinima provođenja reverzibilnih reakcija, temelje se industrijske tehnologije, koje omogućuju provođenje prethodno naizgled nemogućih procesa i dobivanja ekonomskih koristi.
Raznolikost kemijskih procesa
Prema osobitostima toplinskog učinka, mnoge se reakcije pripisuju egzoteričnom ili endotermičkom. Prvi dolazi sa stvaranjem topline, na primjer, oksidacijom ugljika, hidratacijom koncentrirane sumporne kiseline. Druga vrsta promjene povezana je s apsorpcijom toplinske energije. Primjeri endotermnih reakcija: propadanje kalcijev karbonat s obrazovanjem hidratizirani vapno i ugljični dioksid stvaranje vodika i ugljika tijekom termičke razgradnje metana. U jednadžbama egzotermnih i endotermnih procesa potrebno je ukazati na toplinski učinak. Preraspodjela elektrona između atoma reagirajućih tvari odvija se u redoks reakcijama. Četiri vrste kemijskih procesa razlikuju se po karakteristikama reagensa i proizvoda:
- spoj A + B = C;
- razgradnja C = A + B;
- supstitucija AB + C = AC + B;
- izmjena AB + SD = AC + VD.
Za karakterizaciju procesa važna je cjelovitost interakcije spojeva koji reagiraju. Ova značajka podupire podjelu reakcija na reverzibilne i nepovratne.
Reverzibilnost reakcija
Reverzibilni procesi čine većinu kemijskih pojava. Formiranje krajnjih proizvoda iz reagensa je izravna reakcija. Obrnuto, izvorne tvari se dobivaju iz produkata njihove razgradnje ili sinteze. U reakcijskoj smjesi dolazi do kemijske ravnoteže, pri čemu se dobiva onoliko spojeva koliko se početne molekule razgrađuju. U reverzibilnim procesima umjesto znaka "=" između reagensa i proizvoda koriste se simboli "↔" ili "⇌". Strelice mogu biti nejednake duljine, zbog dominacije jedne od reakcija. U kemijskim jednadžbama može se ukazati na agregativne karakteristike tvari (d - plinovi, g - tekućine, t - krute tvari). Od velike su praktične važnosti znanstveno utemeljene metode utjecaja na reverzibilne procese. Tako je proizvodnja amonijaka postala profitabilna nakon stvaranja uvjeta koji pomiču ravnotežu prema stvaranju ciljnog produkta: 3H2 (g) + N2 (g) 2NH3 (g) . Nepovratne pojave dovode do pojave netopljivog ili slabo topljivog spoja, formiranja plina koji napušta reakcijsku sferu. Ti procesi uključuju ionsku izmjenu, razgradnju tvari.
Kemijska ravnoteža i uvjeti za njezino pomicanje
Na karakteristike izravnih i obrnutih procesa utječe nekoliko čimbenika. Jedan od njih je vrijeme. Koncentracija tvari koja se uzima za reakciju postupno se smanjuje, a koncentracija konačnog spoja se povećava. Reakcija smjera prema naprijed je sporija, obrnuti proces dobiva na brzini. U određenom intervalu dva su suprotna procesa sinhrono. Pojavljuje se interakcija između tvari, ali se koncentracije ne mijenjaju. Razlog je dinamička kemijska ravnoteža uspostavljena u sustavu. Njegovo očuvanje ili promjena ovisi o:
- temperaturni uvjeti;
- koncentracije spojeva;
- tlak (za plinove).
Premještanje kemijske ravnoteže
Godine 1884., istaknuti znanstvenik iz Francuske, A.Le Chatelier, predložio je opis načina na koji se sustav može izvući iz stanja dinamičke ravnoteže. Metoda se temelji na načelu izjednačavanja djelovanja vanjskih čimbenika. Le Chatelier je primijetio da u reakcijskoj smjesi postoje procesi koji kompenziraju utjecaj vanjskih sila. Princip koji je formulirao francuski istraživač navodi da promjena stanja u stanju ravnoteže pogoduje reakciji, što slabi vanjski učinak. Ravnotežni pomak podliježe tom pravilu, promatra se kada se sastav, temperaturni uvjeti i tlak promijene. Tehnologije koje se temelje na nalazima znanstvenika koriste se u industriji. Mnogi kemijski procesi, koji su se smatrali praktično neizvedivim, provode se zahvaljujući metodama pomicanja ravnoteže.

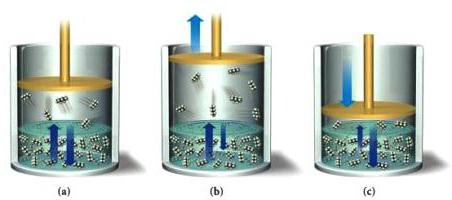
Učinak koncentracije
Do pomaka u ravnoteži dolazi kada se određene komponente uklone iz zone interakcije ili se uvedu dodatni dijelovi tvari. Uklanjanje produkata iz reakcijske smjese obično uzrokuje povećanje brzine njihovog stvaranja, dodavanje tvari, naprotiv, dovodi do njihove preferencijalne razgradnje. U postupku esterifikacije za dehidraciju koristiti sumporna kiselina. Kada se unese u reakcijsku sferu, prinos metil acetata se povećava: CH 3 COOH + CH 3 OH O CH 3 COOCH 3 + H 2 O. sumpor dioksid, Ova kemijska ravnoteža pomiče se prema izravnoj reakciji stvaranja sumpornog trioksida. Kisik se veže za molekule SO3, a njegova koncentracija se smanjuje, što je u skladu s Le Chatelierovim pravilom za reverzibilne procese.
Promjena temperature
Procesi s apsorpcijom ili generiranjem topline su endo- i egzotermni. Za pomicanje ravnoteže koristi se toplina ili toplina iz reakcijske smjese. Povećanje temperature popraćeno je povećanjem brzine endotermnih pojava u kojima se apsorbira dodatna energija. Hlađenje dovodi do prednosti egzotermnih procesa, uz oslobađanje topline. Kada ugljični dioksid stupa u interakciju s ugljenom, zagrijavanje je praćeno povećanjem koncentracije monoksida, a hlađenje dovodi do prevladavajućeg stvaranja čađe: CO 2 (g) + C (t) 2CO (g) .
Učinak tlaka
Promjena tlaka važan je čimbenik za reakcijske smjese koje uključuju plinovite spojeve. Također biste trebali obratiti pozornost na razliku u količinama izvornih i rezultirajućih tvari. Smanjenje tlaka dovodi do prevladavajućeg tijeka pojava u kojima se povećava ukupni volumen svih komponenti. Povećanje tlaka usmjerava proces prema smanjenju volumena cijelog sustava. Ovaj uzorak je opažen u reakciji stvaranja amonijaka: 0.5N2 (g) + 1.5H2 (g) NH3 (g) . Promjena tlaka neće utjecati na kemijsku ravnotežu u onim reakcijama koje se događaju pri konstantnom volumenu.

Optimalni uvjeti za provedbu kemijskog procesa
Stvaranje uvjeta za pomicanje ravnoteže u velikoj mjeri određuje razvoj suvremenih kemijskih tehnologija. Praktična primjena znanstvene teorije doprinosi dobivanju optimalnih proizvodnih rezultata. Najmarkantniji primjer je proizvodnja amonijaka: 0.5N2 (g) + 1.5H2 (g) NH3 (g) . Povećanje sadržaja N 2 i H 2 molekula u sustavu pogoduje sintezi složene tvari iz jednostavnih. Reakcija je praćena otpuštanjem topline, tako da će smanjenje temperature uzrokovati povećanje koncentracije NH3. Volumen polaznih komponenti je veći od ciljnog produkta. Povećanje tlaka će povećati prinos NH3.
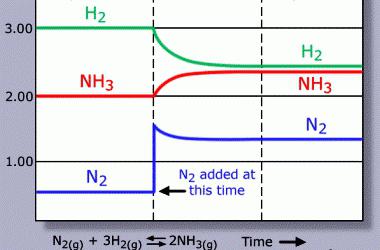
U uvjetima proizvodnje odabire se optimalni omjer svih parametara (temperatura, koncentracija, tlak). Osim toga, važno je područje kontakta između reagensa. U čvrstim heterogenim sustavima, povećanje površine dovodi do povećanja brzine reakcije. Katalizatori povećavaju brzinu izravnih i reverznih reakcija. Uporaba tvari s takvim svojstvima ne istiskuje kemijsku ravnotežu, već ubrzava njezin nastanak.

