Sumporna kiselina i njezina kemijska svojstva
Kiseline su kemijski spojevi koji se sastoje od vodikovih atoma i kiselinskih ostataka, na primjer, SO4, SO3, PO4, itd. Oni su anorganski i organski. Prvi uključuju klorovodičnu, fosfornu, sulfidnu, dušičnu, sumpornu kiselinu. Drugome - octena, palmitinska, mravlja, stearinska, itd.
Što je sumporna kiselina
Ova kiselina se sastoji od dva atoma vodika i kiselinskog ostatka SO4. Ima formulu H2SO4. 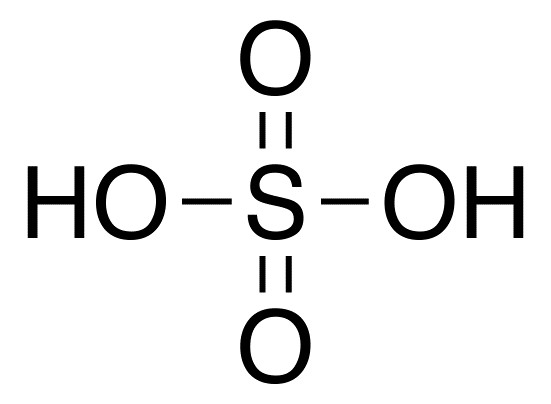 Sumporna kiselina ili, kako se još naziva, sulfat, odnosi se na dibazične kiseline s anorganskim kisikom. Ova tvar se smatra jednom od najagresivnijih i kemijski aktivnijom. U većini kemijskih reakcija djeluje kao oksidacijsko sredstvo. Ova se kiselina može koristiti u koncentriranom ili razrijeđenom obliku, u ta dva slučaja ima nešto drugačija kemijska svojstva.
Sumporna kiselina ili, kako se još naziva, sulfat, odnosi se na dibazične kiseline s anorganskim kisikom. Ova tvar se smatra jednom od najagresivnijih i kemijski aktivnijom. U većini kemijskih reakcija djeluje kao oksidacijsko sredstvo. Ova se kiselina može koristiti u koncentriranom ili razrijeđenom obliku, u ta dva slučaja ima nešto drugačija kemijska svojstva.
Fizička svojstva
Sumporna kiselina u normalnim uvjetima ima tekuće stanje, vrelište je oko 279,6 stupnjeva Celzijusa, točka smrzavanja, kada se pretvori u čvrste kristale, je oko -10 stupnjeva za sto posto i oko -20 za 95 posto.  Čista sto postotna sulfatna kiselina je uljna, bez mirisa i bezbojna tekuća tvar koja ima gotovo dvostruko više gustoće od vode - 1.840 kg / m3.
Čista sto postotna sulfatna kiselina je uljna, bez mirisa i bezbojna tekuća tvar koja ima gotovo dvostruko više gustoće od vode - 1.840 kg / m3.
Kemijska svojstva sulfatne kiseline
Sumporna kiselina reagira s metalima, njihovim oksidima, hidroksidima i solima. Razrijeđena vodom u različitim omjerima, može se ponašati drugačije, stoga detaljnije razmatramo svojstva koncentrirane i slabe otopine sumporne kiseline posebno.
Koncentrirana otopina sumporne kiseline
Koncentrirana je otopina koja sadrži 90% sulfatne kiseline. Takva otopina sumporne kiseline može reagirati čak i kod niskoaktivnih metala, kao i s nemetala, hidroksida, oksida, soli. Svojstva takve otopine sulfatne kiseline slična su onima koncentrirane dušične kiseline. 
Interakcija s metalima
Kada se kemijska reakcija koncentrirane otopine sulfatne kiseline s metalima nalazi s desne strane vodika u elektrokemijskom nizu metalnih naprezanja (to jest, ne najaktivnije), nastaju takve tvari: sulfat metala s kojim dolazi do interakcije, voda i sumporni dioksid. Bakar (cuprum), živa, bizmut, srebro (argentum), platina i zlato (aurum) su metali koji su rezultat interakcija s kojima se tvore navedene tvari.

Interakcija s neaktivnim metalima
Kod metala koji su na lijevoj strani vodika u nizu naprezanja, koncentrirana sumporna kiselina ponaša se malo drugačije. Kao rezultat takve kemijske reakcije nastaju sljedeće tvari: specifični metalni sulfat, vodikov sulfid ili čisti sumpor i voda. Željezo (ferum), magnezij, mangan, berilij, litij, barij, kalcij i svi ostali u nizu naprezanja lijevo od vodika, osim aluminija, kroma, nikla i titana - također su koncentrirani s metalima; sulfatna kiselina ne reagira.
Interakcija s nemetalima
Ova tvar je jako oksidacijsko sredstvo, stoga može sudjelovati u redoks kemijskim reakcijama s ne-metalima, kao što su, na primjer, ugljik (ugljik) i sumpor. Kao rezultat takvih reakcija, voda se nužno oslobađa. Dodavanje ove tvari ugljiku također oslobađa ugljični dioksid i sumporni dioksid. I ako dodajete kiselinu sumporu, dobivamo samo sumporni dioksid i vodu. U takvoj kemijskoj reakciji sulfatna kiselina ima ulogu oksidacijskog sredstva.
Interakcija s organskim tvarima
Među reakcijama sa sumpornom kiselinom organska tvar može se razlikovati charring. Takav se proces događa kada se određena tvar sudara s papirom, šećerom, vlaknima, drvom itd. U svakom slučaju, ugljik se oslobađa. Ugljik, koji je nastao tijekom reakcije, može djelomično djelovati sa sumpornom kiselinom kada je u suvišku. Fotografija prikazuje reakciju šećera s otopinom sulfatne kiseline prosječne koncentracije.

Reakcije s solima
Koncentrirana otopina H2SO4 također reagira sa suhim solima. U tom slučaju dolazi do standardne reakcije izmjene, u kojoj nastaje metalni sulfat, koji je prisutan u strukturi soli, i kiselina s ostatkom koji je u sastavu soli. Međutim, s otopinama soli koncentrirana sumporna kiselina ne reagira.
Interakcija s drugim tvarima
I ova tvar može reagirati s metalnim oksidima i njihovim hidroksidima, u tim slučajevima dolazi do reakcija razmjene, u prvom se otpuštaju metalni sulfat i voda, u drugom - isti.
Kemijska svojstva slabe otopine sulfatne kiseline
Razrijeđena sumporna kiselina reagira s mnogim tvarima i ima ista svojstva kao i sve kiseline. Ona, za razliku od koncentriranog, djeluje samo s aktivnim metalima, odnosno onima koji su lijevo od vodika u nizu naprezanja. U tom slučaju dolazi do iste supstitucijske reakcije kao u slučaju bilo koje kiseline. Time se oslobađa vodik. Također, takva otopina kiseline je u interakciji s otopinama soli, zbog čega dolazi do reakcije izmjene, o kojoj smo već govorili, s oksidima - kao i koncentriranim, s hidroksidima - također na isti način. Osim uobičajenih sulfata, postoje i hidrosulfati, koji su produkt interakcije hidroksida i sumporne kiseline.

Kako znati da otopina sadrži sumpornu kiselinu ili sulfate
Da bi se utvrdilo jesu li te tvari prisutne u otopini, posebno odgovor na kvalitetu na sulfatne ione, što vam daje do znanja. Sastoji se od dodavanja barija ili njegovih spojeva u otopinu. Kao rezultat, bijeli talog može ispasti. (barijev sulfat), što ukazuje na prisutnost sulfata ili sumporne kiseline.
Kako izlučiti sumpornu kiselinu
Najčešći način industrijske proizvodnje ove tvari je ekstrakcija iz željeznog pirita. Taj se proces odvija u tri faze, pri čemu se odvija specifična kemijska reakcija. Razmotrite ih. Prvo se piritu dodaje kisik, što dovodi do stvaranja željeznog oksida i sumpor dioksid, koji se koristi za daljnje reakcije. Ova interakcija se događa na visokim temperaturama. Nakon toga slijedi faza u kojoj se sumporni trioksid dobiva dodavanjem kisika u prisutnosti katalizatora, koji je vanadijev oksid. Sada, u zadnjoj fazi, dodanoj vodi dodana je voda, a dobivene su sulfatne kiseline. To je najčešći postupak za komercijalnu proizvodnju sulfatne kiseline, najčešće se koristi zato što je pirit najlakša sirovina pogodna za sintezu tvari opisane u ovom članku. Sumporna kiselina dobivena ovim postupkom koristi se u raznim industrijama, kako kemijskim tako i mnogim drugim, na primjer, rafiniranje nafte obogaćivanje ruda, itd. Također se često koristi u tehnologiji proizvodnje skupa sintetičkih vlakana.