Teorija elektrolitičke disocijacije - jedna od glavnih u kemiji
Kada se otopi u vodi, tvari elektrolita razgrađuju se u nabijene čestice - ione. Suprotno je molarizaciji ili asocijaciji. Formiranje iona objašnjava teoriju elektrolitičke disocijacije (Arrhenius, 1887). Na mehanizam razgradnje kemijskih spojeva tijekom taljenja i otapanja utječu karakteristike tipova kemijskih veza, struktura i priroda otapala.
Elektroliti i neprovodnici
Razaranje se događa u otopinama i otopi kristalne rešetke i molekule - elektrolitička disocijacija (ED). Raspadanje tvari popraćeno je stvaranjem iona, pojavom takvih svojstava kao što je električna vodljivost. Nije svaki spoj sposoban disociirati, već samo tvari koje se u početku sastoje od iona ili visoko polarnih čestica. Prisutnost slobodnih iona objašnjava svojstvo elektrolita za provođenje struje. Bazu, sol, mnoge anorganske i neke organske kiseline posjeduju tu sposobnost. Nevodnici se sastoje od nisko-polarnih ili nepolariziranih molekula. Oni se ne razgrađuju u ione, jer nisu elektroliti (mnogi organski spojevi). Nositelji naboja su pozitivni i negativni ioni (kationi i anioni).
Uloga S. Arrheniusa i drugih kemičara u proučavanju disocijacije
Teoriju elektrolitičke disocijacije dokazao je 1887. godine znanstvenik iz Švedske S. Arrhenius. No, prva opsežna istraživanja svojstava rješenja izvršio je ruski znanstvenik M. Lomonosov. Doprinosili su proučavanju nabijenih čestica koje nastaju otapanjem tvari, T. Grotgus i M. Faraday, R. Lenz. Arrhenius je dokazao da su mnogi anorganski elektroliti i neki organski spojevi. Švedski znanstvenik objasnio je električnu vodljivost otopina raspadanjem tvari u ione. Teorija Arrheniusove elektrolitičke disocijacije nije pridala važnost neposrednom sudjelovanju molekula vode u tom procesu. Ruski znanstvenici Mendeleev, Kablukov, Konovalov i drugi vjerovali su da se odvija solvatacija - interakcija otapala i otopljene tvari. Kada je riječ o vodenim sustavima, koristi se naziv "hidratacija". To je složen fizikalno-kemijski proces, o čemu svjedoče formiranje hidrata, termalnih pojava, promjenu boje tvari i pojava sedimenta.

Glavne odredbe teorije elektrolitičke disocijacije (TED)
Mnogi su znanstvenici radili na razjašnjavanju teorije S. Arrheniusa. Bilo je potrebno poboljšati ga, uzimajući u obzir suvremene podatke o strukturi atoma, kemijskoj vezi. Formulirane su glavne odredbe TED-a, koje se razlikuju od klasičnih teza s kraja XIX stoljeća:
- Postupak taljenja ili otapanja popraćen je disocijacijom elektrolita u ione. Dakle (na prijedlog Faradaya) nazivaju se čestice s nabojem ("+" ili "-") koje se razlikuju od neutralnih atoma u strukturi valentnih ljuski i stabilnosti su obojene i bezbojne. Ioni mogu biti jednostavni: Na + , Cl-, S2, Al3 + . Postoje nabijene čestice koje se sastoje od skupina atoma: CO 2- , NH 4+ . Iz grčkog jezika naziv "ion" se prevodi kao "lutanje", što ukazuje na slučajnost širenja tih čestica.
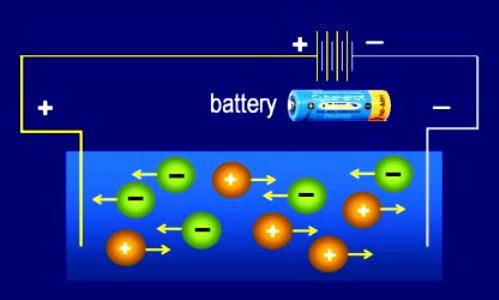
- Utjecaj vanjskog električnog polja uzrokuje da se ioni uredno kreću unutar prostora elektrolita. Svaka negativna čestica usmjerena je na anodu (pozitivna elektroda). Ioni sa znakom "+" počinju se kretati prema katodi (negativna elektroda).
- Istovremeno, raspadanje u ione i kombinacija tih čestica javljaju se u otopinama, stoga se disocijacija odnosi na reverzibilne fizičko-kemijske procese.
Pojava koja se pojavljuje mora se uzeti u obzir pri sastavljanju jednadžbi: primijeniti poseban znak reverzibilnog procesa, izračunati negativne i pozitivne naboje: moraju se podudarati u zbroju.
Mehanizam ED ionskih tvari
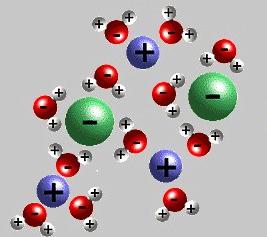
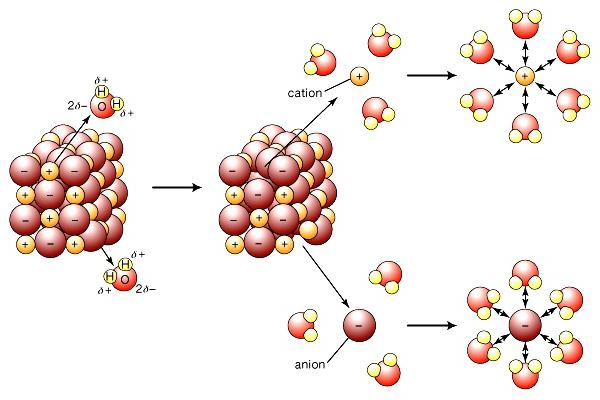
Moderna teorija elektrolitičke disocijacije uzima u obzir strukturu elektrolitskih tvari i otapala. Kada se otopi, veze između suprotno nabijenih čestica u ionskim kristalima uništavaju se djelovanjem polarnih molekula vode. Oni doslovno "vuku" ione iz mase u otopinu. Raspad prati stvaranje solvatne (u vodi - hidratacija) ljuske oko iona. Osim vode, ketoni, niži alkoholi, imaju veću dielektričnu konstantu. Tijekom disocijacije natrijev klorid Na + i Cl - ioni registriraju početni stupanj, što je praćeno orijentacijom vodenih dipola u odnosu na površinske ione u kristalu. U završnoj fazi, hidratizirani ioni se oslobađaju i difundiraju u tekućinu.
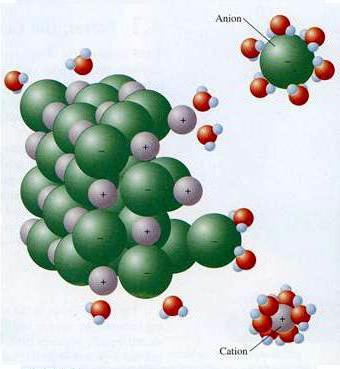
Mehanizam ED spojeva s kovalentno jako polarnom vezom
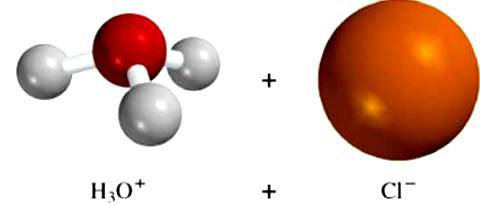
Molekule otapala utječu na kristalnu strukturu neionskih tvari. Na primjer, učinak vodenih dipola na klorovodičnu kiselinu dovodi do promjene tipa veze u molekuli od kovalentnog polara do ionskog. Tvar se disocira, hidratizirani vodik i ioni klora ulaze u otopinu. Ovaj primjer dokazuje važnost procesa koji se javljaju između čestica otapala i otopljenog spoja. Upravo ta interakcija dovodi do stvaranja iona elektrolita.
Teorija elektrolitičke disocijacije i glavne klase anorganskih spojeva
U svjetlu glavnih odredbi TED-a, elektrolit se može nazvati kiselinom, a za vrijeme raspada koji od pozitivnih iona može se detektirati samo proton H + . Disocijacija baze prati stvaranje ili oslobađanje kristalne rešetke samo OH aniona i kationa metala. Normalna sol kada se otopi daje pozitivan metalni ion i negativan - ostatak kiseline. Glavnu sol karakterizira prisutnost dva tipa aniona: OH skupina i kiselinski ostatak. U kiseloj soli kationa prisutni su samo vodik i metal.
Elektrolitska čvrstoća
Za karakterizaciju stanja tvari u otopini koristi se fizikalna veličina - stupanj disocijacije (α). Potražite njegovu vrijednost iz omjera broja slomljenih molekula i njihovog ukupnog broja u otopini. Dubina disocijacije određena je različitim uvjetima. Važni dielektrični pokazatelji otapala, struktura otopljenih spojeva. Tipično, stupanj disocijacije se smanjuje s povećanjem koncentracije i povećava se s povećanjem temperature. Često se stupanj disocijacije određene tvari izražava u frakcijama jedinice.
Klasifikacija elektrolita
Teorija elektrolitičke disocijacije na kraju XIX. Stoljeća nije sadržavala odredbu o interakciji iona u otopini. Učinak molekula vode na raspodjelu kationa i aniona bio je neznatan za Arrheniusa. Arrheniusove ideje o jakim i slabim elektrolitima bile su formalne. Na temelju klasičnih položaja može se dobiti α = 0.75–0.95 za jake elektrolite. Eksperimenti su dokazali ireverzibilnost njihove disocijacije (α → 1). Topljive soli, sumporne i klorovodična kiselina lužine. Djelomično razdvaja sumpor, dušik, fluorovodik, fosforna kiselina. Slabi elektroliti su silikatna, octena, sumporna i ugljična kiselina, amonijev hidroksid, netopljive baze. Voda se također naziva slabim elektrolitima. Mali dio H 2 O molekula disocira, a ioni su istovremeno molarizirani.