Kemijska svojstva etilena. Formula etilena
Nezasićeni ugljikovodici s dvostrukom kemijskom vezom u molekulama pripadaju skupini alkena. Prvi predstavnik homologne serije R3 je eten, ili etilen, čija je formula: C2H4. Alkeni se često nazivaju olefini. Ime je povijesno i nastalo je u 18. stoljeću, nakon što je dobiven produkt interakcije etilena s klor-etil kloridom, koji ima izgled uljne tekućine. Zatim ethen i zove naftni plin. U članku ćemo proučiti njegova kemijska svojstva, kao i njezinu proizvodnju i uporabu u industriji.
Odnos između strukture molekule i svojstava tvari
Prema teoriji strukture organskih tvari koju je predložio M. Butlerov, karakteristika spoja u potpunosti ovisi o strukturalnoj formuli i vrsti veza njezine molekule. Kemijska svojstva etilena također su određena prostornom konfiguracijom atoma, hibridizacijom oblaka elektrona i prisustvom pi veze u njegovoj molekuli. Dva ne-hibridizirana p-elektrona ugljikovih atoma preklapaju se u ravnini okomitoj na ravninu same molekule. Formira se dvostruka veza, čija ruptura određuje sposobnost alkena za reakcije adicije i polimerizacije.

Fizička svojstva
Eten je plinovita tvar sa suptilnim mirisom. Slabo je topljiv u vodi, ali dobro topljiv u benzenu, ugljikovom tetrakloridu, benzinu i drugim organskim otapalima. Na temelju formule etilena C 2 H 4 , njegova molekularna težina je 28, tj. Etilen je nešto lakši od zraka. U homolognoj seriji alkena s povećanjem njihove mase agregatno stanje tvari mijenja se prema shemi: plin - tekućina - kruti spoj.
Primanje plina u laboratoriju i industriji
Zagrijavanje etil alkohol do 140 ° C u prisutnosti koncentrirana sumporna kiselina može se dobiti u laboratoriju. Druga metoda je eliminacija atoma vodika iz molekula alkana. Djelovanjem s kaustičnim natrijem ili kalijem na spojeve zasićenih ugljikovodika supstituiranih halogenom, na primjer kloroetan, ekstrahira se etilen. U industriji, najperspektivniji način da se to postigne jest prerada prirodnog plina, kao i piroliza i pucanje nafte. Sva kemijska svojstva etilena - hidratacija, polimerizacija, dodavanje, oksidacijske reakcije - objašnjavaju se prisutnošću dvostruke veze u njezinoj molekuli.
Interakcija olefina s elementima glavne podgrupe sedme skupine
Svi članovi homologne serije etena pridaju atome halogena na mjestu gdje je pi veza prekinuta u svojoj molekuli. Dakle, crveno-smeđa vodena otopina broma postaje bezbojna, s rezultatom da je etilenska jednadžba dibromoetan:
C2H4 + Br2 = C2H4Br2
Reakcija s klorom i jodom odvija se na sličan način, dodavanje halogenih atoma također se događa na mjestu uništavanja dvostruke veze. Svi spojevi - olefini mogu međusobno djelovati s vodikovim halogenidima: klorovodikom, fluorovodikom itd. Kao rezultat reakcije adicije, koja se odvija putem ionskog mehanizma, tvore se tvari - halogeni derivati zasićenih ugljikovodika: kloroetan, fluoroetan.
Proizvodnja industrijskog etanola
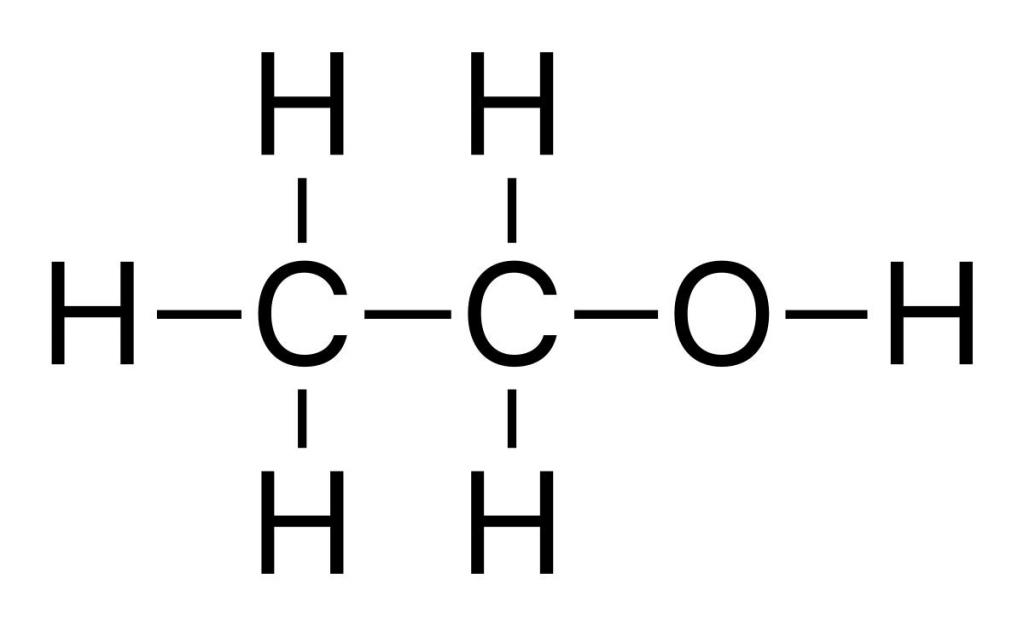
Kemijska svojstva etilena često se koriste za dobivanje važnih tvari koje se široko koriste u industriji i svakodnevnom životu. Na primjer, zagrijavanje etena s vodom u prisutnosti fosforne ili sumporne kiseline, pod djelovanjem katalizatora, dolazi do hidratacije. To ide uz stvaranje etilnog alkohola - višenamjenski proizvod dobiven u kemijskim postrojenjima organske sinteze. Mehanizam reakcije hidratacije odvija se analogno drugim reakcijama adicije. Osim toga, interakcija etilena s vodom također se javlja kao rezultat razbijanja pi veze. Slobodne valencije atoma ugljika etena spojene su atomima vodika i hidroksilnom skupinom, koje su dio molekule vode.
Hidrogenacija i izgaranje etilena
Bez obzira na prethodno navedeno, reakcija vodikovog spoja je od male praktične važnosti. Međutim, on pokazuje genetsku vezu između različitih klasa organskih spojeva, u ovom slučaju alkana i olefina. Dodavanjem vodika, eten se pretvara u etan. Suprotan proces je odvajanje od zasićenih ugljikovodika atomi vodika dovode do formiranja reprezentativnog alkena - etena. Snažna oksidacija olefina, zvana izgaranje, popraćena je oslobađanjem velikih količina topline, a reakcija je egzotermna. Proizvodi izgaranja jednaki su za tvari svih klasa ugljikovodika: alkane, nezasićene spojeve etilenske i acetilenske serije, aromatske tvari. To uključuje ugljični dioksid i vodu. Zrak reagira s etilenom i tvori eksplozivnu smjesu.

Reakcije oksidacije
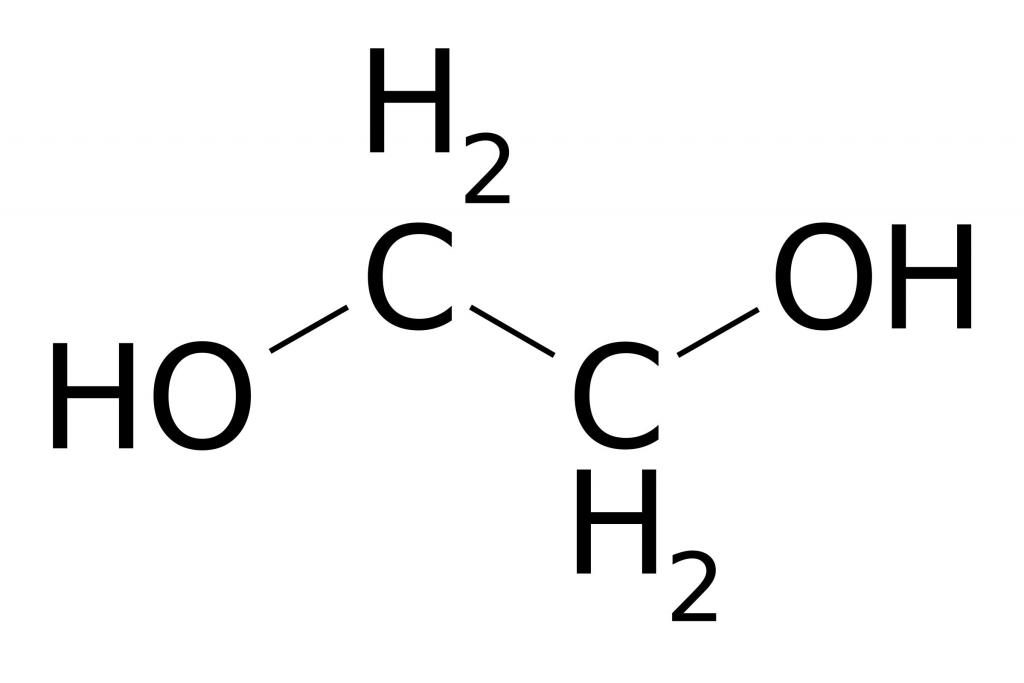
Eten se može oksidirati otopinom. kalijev permanganat. To je jedna od kvalitativnih reakcija koje dokazuju postojanje dvostruke veze u sastavu tvari koja se određuje. Ljubičasta boja otopine nestaje zbog razbijanja dvostruke veze i stvaranja diatomske granice alkohola - etilen glikola. Produkt reakcije ima širok raspon industrijskih primjena kao sirovina za proizvodnju sintetičkih vlakana, kao što su lavsan, eksplozivi i antifriz. Kao što možete vidjeti, kemijska svojstva etilena koriste se za dobivanje vrijednih spojeva i materijala.
Polimerizacija olefina
Povećanje temperature, povećanje tlaka i upotreba katalizatora nužni su uvjeti za provedbu procesa polimerizacije. Njegov mehanizam se razlikuje od reakcija adicije ili oksidacije. Predstavlja sekvencijalno vezanje mnogih molekula etilena na točkama razbijanja dvostrukih veza. Produkt reakcije je polietilen, čija fizička svojstva ovise o vrijednosti n, stupnju polimerizacije. Ako je mala, tada je tvar u tekućem agregacijskom stanju. Ako se brojka približava 1000 veza, tada se od takvog polimera izrađuju polietilenski film i fleksibilna crijeva. Ako je stupanj polimerizacije veći od 1500 jedinica u lancu, materijal je bijela krutina, masna na dodir.

Odlazi u proizvodnju čvrstih proizvoda i plastičnih cijevi. Etilenski halogenirani spoj - Teflon ima svojstva protiv gorenja i široko se koristi polimer, koji se zahtijeva u proizvodnji višeslojnih posuda, tava, posuđa. Njegova visoka otpornost na abraziju koristi se u proizvodnji maziva za automobilske motore, a niska toksičnost i tolerancija na tkiva ljudskog tijela omogućila je korištenje teflonskih proteza u kirurgiji.

U našem članku ispitali smo kemijska svojstva olefina, kao što su izgaranje etilena, dodavanje, oksidacija i polimerizacija.