Zasićeni ugljikovodici: svojstva i primjena
Prvo razmatramo rubne ugljikovodike, posebice njihovu strukturu, svojstva, primjene.
Opće informacije o alkanima
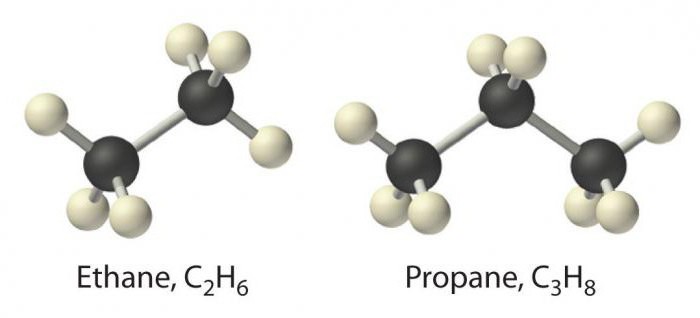
Ova klasa uključuje spojeve koji zadovoljavaju opću formulu CnH2n + 2. Njihove molekule su linearne, za njih je karakteristična samo jednostavna veza.
Granične ugljikovodike predstavljaju homologne serije metana. Između ugljikovih atoma u njihovim molekulama sp3 hibridizacija, koju karakterizira kut od 109 stupnjeva.
Biti u prirodi
Ograničeni ugljikovodici su široko rasprostranjeni u prirodi. Na primjer, metan, glava ove klase ShNu, nastaje razgradnjom životinjskih i biljnih organizama u močvarnim područjima (bez pristupa zraku).
Osim toga, ovaj je spoj prisutan u rudnicima ugljena, što često dovodi do ozbiljnih eksplozija i smrti rudara.
Ograničeni ugljikovodici u velikim količinama sadržani su u krutom, tekućem i plinovitom obliku u ulju. Osim metana, ulje sadrži propan, etan, butan i pentan.
Fizikalna svojstva alkana
Te su tvari slabo topive u vodi. Najniži članovi serije su plinovi. S povećanjem relativne molekularne težine spojeva, opaženo je povećanje točaka vrenja i tališta, dolazi do prijelaza iz plinovitog u tekuće.

Kemijska svojstva
Uzeti u obzir osnovna kemijska svojstva zasićenih ugljikovodika. Zbog niskog polariteta C-C veze, oni su kemijski neaktivni spojevi.
Među karakterističnim svojstvima predstavnika ove klase bilježimo radikalnu halogenaciju. Kao rezultat interakcije u prvoj fazi nastaje monohalogeno-spoj, kao i vodikov halid. S obzirom da reakcija ima lančani mehanizam, supstitucija se nastavlja sve dok se ne pojavljuju atomi halogena umjesto vodika.
Osim halogeniranja, zasićeni ugljikovodici međusobno djeluju dušična kiselina. Nitracija dovodi do stvaranja nitroalkana.
Sumpor je povezan s zamjenom vodikovog atoma sulfo-skupinom, a među reakcijskim produktima bit će alkansulfonska kiselina i voda. Postupak se provodi uz lagano zagrijavanje reakcijske smjese, sumporna kiselina uzeti u koncentriranom obliku.
Pod normalnim uvjetima, alkani pokazuju otpornost na tako jaka oksidirajuća sredstva kao kalijev permanganat, kalijev dikromat.
Kada temperatura raste, opaža se njihova oksidacija kisikom iz zraka ugljikov monoksid (4) i vodene pare.
Nekompletna (katalitička) oksidacija dovodi do stvaranja ketona, aldehida, karboksilnih kiselina.
Kada se C-C veze raskidaju, dolazi do pucanja, zbog čega se spojevi s manjim brojem ugljikovih atoma formiraju iz dugog ugljikovog lanca.
Među proizvodima dehidrogenacije nezasićenih ugljikovodika i molekula vodika, reakcija se odvija na visokim temperaturama.
Tijekom dehidrociklizacije formiraju se aromatski ugljikovodici koji imaju praktičnu primjenu.
Nezasićeni ShNu
Granični i nezasićeni ugljikovodici mogu imati cikličku ili alifatsku strukturu. Na primjer, alkeni koji imaju opću formulu CnH2n razlikuju se po prisutnosti dvostrukih veza između ugljikovih atoma.
Zbog toga za predstavnike niza etilenskih karakterističnih reakcija dodavanja dvostrukoj vezi. Hidrohalogeniranje i hidratacija provode se za asimetrične alkene prema Markovnikovom pravilu. Njegova suština je da se pri spajanju dvostrukom vezom vodikovog halida ili vode, atomi halogena ili hidrokso-skupine vežu na ugljik koji ima manji broj H, a vodik ide na prvi atom C.
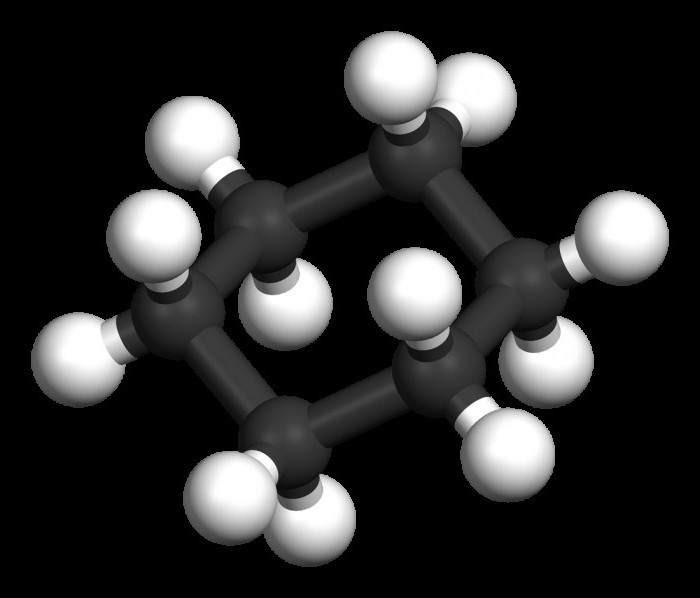
Osim toga, za predstavnike ove klase organski spojevi karakterističnu reakciju polimerizacije. Pronašao je široku primjenu u suvremenoj kemijskoj industriji. Na primjer, za proizvodnju polietilena, koji je tražen u poljoprivredi, medicina, etilen se uzima kao početni monomer. Tijekom procesa katalitičke polimerizacije, dvostruka veza se raspada i na kraju formira polimerni spoj.
Kvalitativna reakcija neodređenost (prisutnost dvostrukih i trostrukih veza u molekulama) je izbjeljivanje bromove (jodne) vode, kao i izbjeljivanje otopine kalijevog permanganata.
Među cikličkim ugljikovodicima, koji se danas široko koriste, treba spomenuti benzen i toluen. Ovi ShNu su tipični predstavnici brojnih aromatskih ugljikovodika, koji imaju opću formulu CnH2n-6.
Benzen, u kojem je gustoća elektrona ravnomjerno raspodijeljena, smatra se spojem niske aktivnosti. Toluen koji se koristi za industrijsku proizvodnju benzojeve kiseline, koji je izvrstan konzervans, ima veću reaktivnost.

zaključak
U organskoj kemiji razlikuje se nekoliko klasa ugljikovodika koji se razlikuju po rasporedu ugljikovih atoma i prisutnosti jednostrukih i dvostrukih (trostrukih) veza. Unatoč značajnim razlikama u strukturi, fizičkim i kemijskim svojstvima, sve su one tražene u različitim industrijama. Među zasićenim ugljikovodicima poseban interes su metan i njegovi najbliži homologi.
Među dienskim spojevima, vodeći pokazatelji u proizvodnji polimernih materijala su 1,3-butadien i 2-metilbutadien-1,3. Od posebnog interesa su aromatski ugljikovodici. Oni su osnova za proizvodnju organskih bojila, konzervansa.