Klasifikacija termodinamičkih sustava
Razmotrite značajke termodinamičkih sustava. Pod njima se obično podrazumijevaju fizički makroskopski oblici, koji se sastoje od značajnog broja čestica, a koji nisu namijenjeni za opisivanje makroskopskih parametara svake pojedine čestice.
Nema ograničenja u prirodi materijalnih čestica koje su sastavni dio takvih sustava. Mogu se prikazati u obliku molekula, atoma, iona, elektrona, fotona.
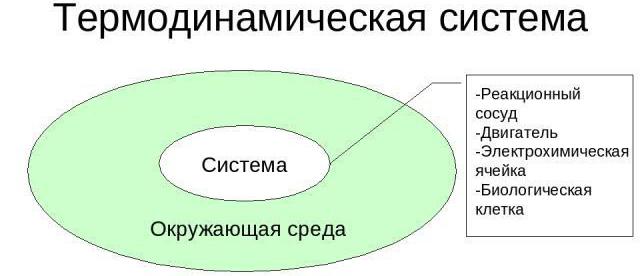
Posebne značajke
Analizirajmo karakteristične značajke termodinamičkih sustava. Kao primjer, možete uzeti bilo koji predmet koji se može promatrati bez uporabe teleskopa, mikroskopa. Da bi se dao potpuni opis takvog sustava, odabrani su makroskopski detalji, zahvaljujući kojima se može odrediti volumen, tlak, temperatura, električna polarizacija, magnetska indukcija, kemijski sastav i masa komponenata.
Za sve termodinamičke sustave postoje uvjetne ili stvarne granice koje ih razdvajaju od okoline. Umjesto toga, oni često koriste koncept termostata, koji je karakteriziran tako visokom vrijednošću toplinskog kapaciteta da, u slučaju razmjene topline s analiziranim sustavom, indeks temperature ostaje konstantan.
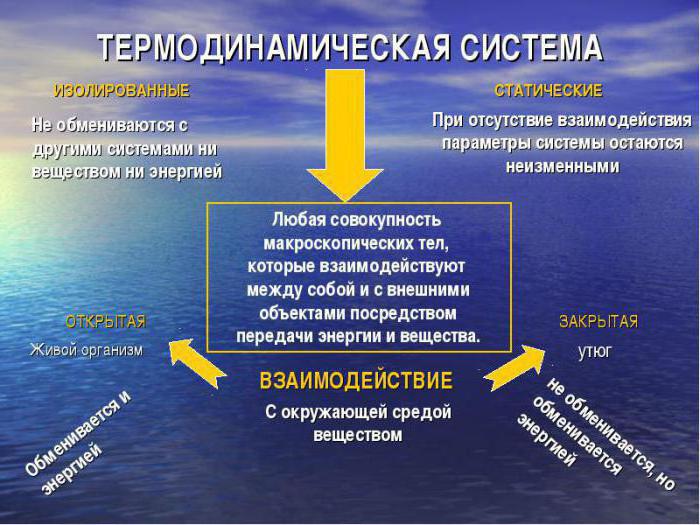
Klasifikacija sustava
Razmotrite što čini klasifikaciju termodinamičkih sustava. Ovisno o prirodi njegove interakcije s okolinom, uobičajeno je izdvojiti:
- izolirane vrste koje ne razmjenjuju materiju ili energiju s vanjskim okolišem;
- adijabatski izoliran, ne razmjenjujući supstancu s vanjskom okolinom, već ulazeći u razmjenu rada ili energije;
- zatvoreni termodinamički sustavi nemaju razmjenu tvari, dopuštena je samo promjena energetske vrijednosti;
- otvoreni sustavi karakterizira potpuni prijenos energije, materije;
- djelomično otvoreni mogu imati polupropusne pregrade, te stoga ne mogu u potpunosti sudjelovati u razmjeni materijala.
Ovisno o opisu, parametri termodinamičkog sustava mogu se podijeliti na složene i jednostavne varijante.

Značajke jednostavnih sustava
Jednostavni sustavi nazivaju se ravnotežna stanja, čije se fizičko stanje može odrediti specifičnim volumenom, temperaturom, tlakom. Primjeri termodinamičkih sustava ovog tipa su izotropna tijela koja imaju jednake značajke u različitim smjerovima i točkama. Dakle, tekućine, plinovite tvari, krute tvari, koje su u stanju termodinamičke ravnoteže, nisu izložene elektromagnetskim i gravitacijskim silama, površinskoj napetosti, kemijskim transformacijama. Analiza jednostavnih tijela prepoznata je u termodinamici kao važna i relevantna s praktičnog i teorijskog stajališta.
Unutarnja energija termodinamički sustav ovog tipa povezan je s okolnim svijetom. Kada se opisuje uporaba broja čestica, masa tvari svake pojedine komponente.
Složeni sustavi
Kompleks uključuje termodinamičke sustave koji ne potpadaju pod jednostavne oblike. Primjerice, to su magneti, dielektrika, čvrsta elastična tijela, supravodiči, površine sučelja, toplinsko zračenje, elektrokemijski sustavi. Kao parametri koji se koriste za njihovo opisivanje bilježimo elastičnost opruge ili šipke, površinu faznog odsječka, toplinsko zračenje.
Fizički sustav se naziva takvim skupom u kojem nema kemijske interakcije između tvari unutar granica temperature, tlaka, odabranih za proučavanje. I kemijski sustavi te opcije nazivaju interakcijom između njezinih pojedinačnih komponenti.
Unutarnja energija termodinamičkog sustava ovisi o prisutnosti njegove izolacije s vanjskim svijetom. Na primjer, kao varijanta adijabatske ljuske, može se zamisliti Brod Dewar. Homogeni karakter se očituje u sustavu u kojem sve komponente imaju slična svojstva. Primjeri za to su plinske, krute, tekuće otopine. Tipičan primjer homogene faze plina je atmosfera Zemlje.
Značajke termodinamike
Ovaj dio znanosti bavi se proučavanjem osnovnih zakona koji upravljaju procesima koji su povezani s oslobađanjem, apsorpcijom energije. U kemijskoj termodinamici je namjera proučiti međusobne transformacije sastavnih dijelova sustava, uspostaviti zakone koji reguliraju prijelaz jedne vrste energije u drugu pod danim uvjetima (tlak, temperatura, volumen).
Sustav, koji je predmet termodinamičkih istraživanja, može se predstaviti kao bilo koji objekt prirode, koji uključuje veliki broj molekula koje su međusobno odvojene sučeljem s drugim stvarnim objektima. Pod stanjem sustava podrazumijeva se kombinacija njegovih svojstava, što dopušta da se odredi sa stajališta termodinamike.
zaključak
U svakom sustavu postoji prijelaz jedne vrste energije u drugu, a uspostavljena je i termodinamička ravnoteža. Odsjek za fiziku koji su uključeni u detaljno proučavanje transformacija, promjena, očuvanja energije, od posebne je važnosti. Na primjer, u kemijskoj kinetici moguće je ne samo opisati stanje sustava, nego i izračunati uvjete koji su pogodni za njegovo pomicanje u pravom smjeru.
Hessov zakon, koji povezuje entalpiju, entropiju razmatrane transformacije, omogućuje da se identificira mogućnost spontane reakcije, da se izračuna količina topline koju oslobađa (apsorbira) termodinamički sustav.
Termokemija utemeljena na temeljima termodinamike je od praktične važnosti. Zahvaljujući ovom dijelu kemije, u proizvodnji se provode preliminarni izračuni učinkovitosti goriva i izvedivosti uvođenja određenih tehnologija u stvarnu proizvodnju. Informacije dobivene iz termodinamike omogućuju primjenu fenomena elastičnosti, termoelektričnosti, viskoznosti, magnetizacije na industrijsku proizvodnju različitih materijala.