Mehanizam donatora-akceptora - što je to?
Donatorsko-akceptorski mehanizam stvaranja kemijske veze uključuje prijenos naboja između akceptora i donora bez stvaranja zajedničke kemijske veze između njih. Također je moguće prenijeti usamljeni par elektrona u akceptor od donora, što rezultira vezom.
Nastajanje amonijevih soli
Razmotrimo mehanizam donor-akceptor na primjeru amonijevih soli. Započinjemo s interakcijom amonijaka (NH3) i borovog trifluorida (BF3). Tijekom reakcije oslobađa se 171,4 kJ / mol energije. Interakcija se nastavlja prema jednadžbi:
NH3 + BF3 = NH3BF3
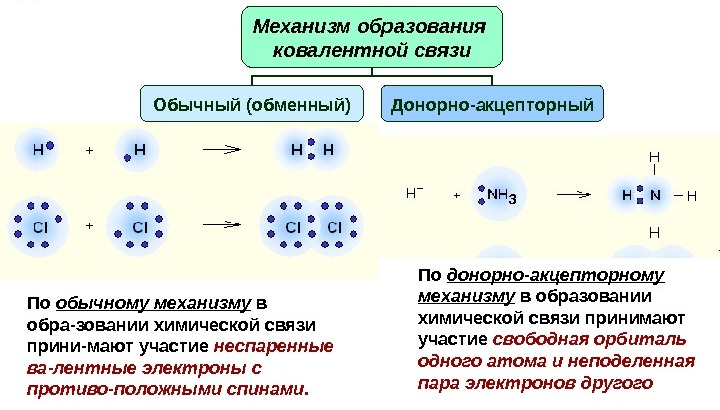
Od četiri orbitale prisutne u atomu bora, tri su ispunjene elektronima, stoga postoji jedna prazna orbita. U molekuli amonijaka, četiri orbitale dušika su opremljene elektronima, a tri od njih su dopunjene vodikovim elektronima kroz mehanizam razmjene. Jedna orbitala ima elektronski par koji pripada samo atomu dušika. Zove se usamljeni elektronski par. Zahvaljujući njoj, mehanizam donor-akceptor je moguć.
Veza između amonijaka i borovog trifluorida je moguća zbog činjenice da se prazni elektronski par amonijaka stavlja na slobodne orbitale bor-fluorida.
To je mehanizam donor-akceptor za stvaranje kovalentnih veza. Atom dušika povećava valenciju pomoću usamljenog para elektrona za dodatno vezanje. Bor povećava valenciju postavljanjem dodatnih elektrona u orbitalu.
Prema tome, valencija tih kemijskih elemenata karakteriziraju i nespareni elektroni, i usamljeni elektronski parovi, i slobodne orbitale na vanjskoj energetskoj razini.
definirati
Donor u ovom primjeru je atom dušika, koji daruje svoj elektronski par da formira kemijsku vezu. Prihvatnik je bor, ima praznu orbitalu, prihvaća elektronički par.
Proces je popraćen smanjenjem potencijalne energije ovog sustava, oslobađanjem ekvivalentne količine energije. Pitanja vezana uz mehanizam nastanka ove vrste kovalentne veze uključena su u tijek školskog programa iz kemije, a predložena su u završnim ispitima za maturante srednjih škola.
Nastajanje amonijevog kationa
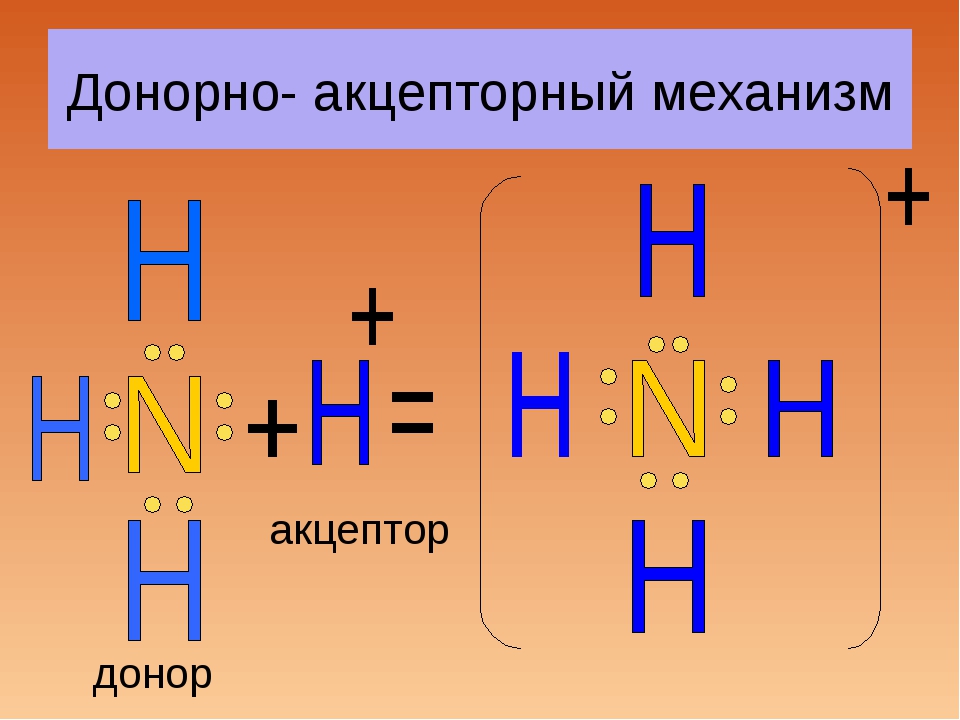
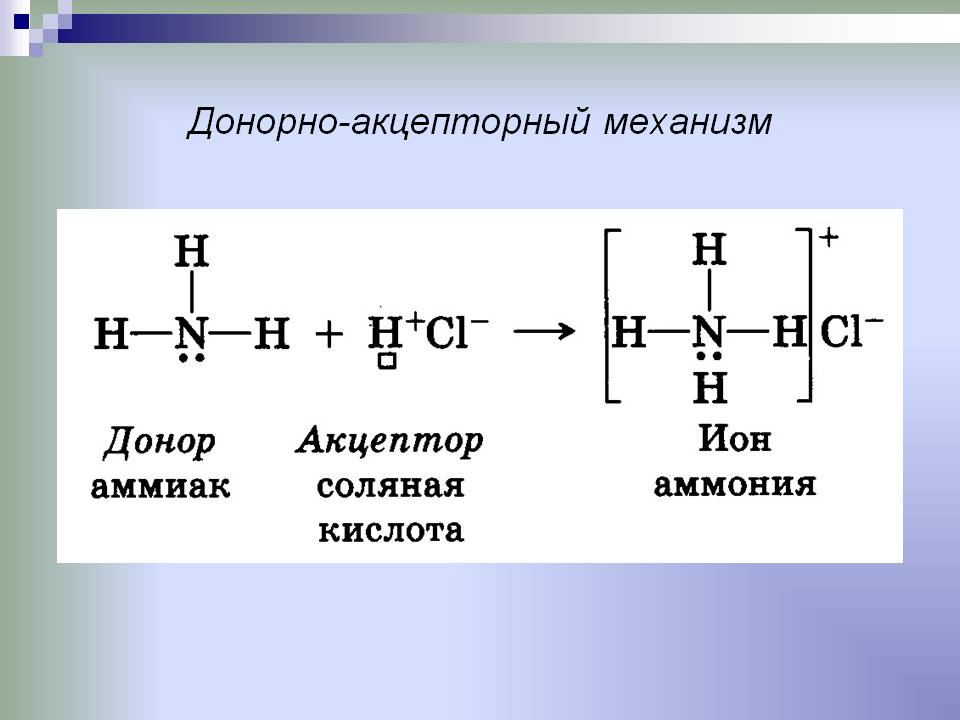
Kovalentna veza formirana donor-akceptor mehanizmom je karakteristična za amonijeve soli. Osvrnimo se na njegove značajke. Dakle, putem mehanizma donor-akceptor se formira veza između atoma dušika i vodika u reakciji:
NH3 + H + = NH4 +
Akceptor je prazna orbita kationa vodika. Dušik u amonijevom kationu pokazuje valenciju 4. Nastajanje veze također nastaje zbog para elektrona koji pripadaju dušiku prije početka interakcije.
To je kovalentna veza pomoću mehanizma donor-akceptor. Kao rezultat interakcije nastaje amonijev kation, koji će se ionskim mehanizmom kombinirati s anionima sadržanim u kiselinama.

Nastajanje ugljičnog monoksida
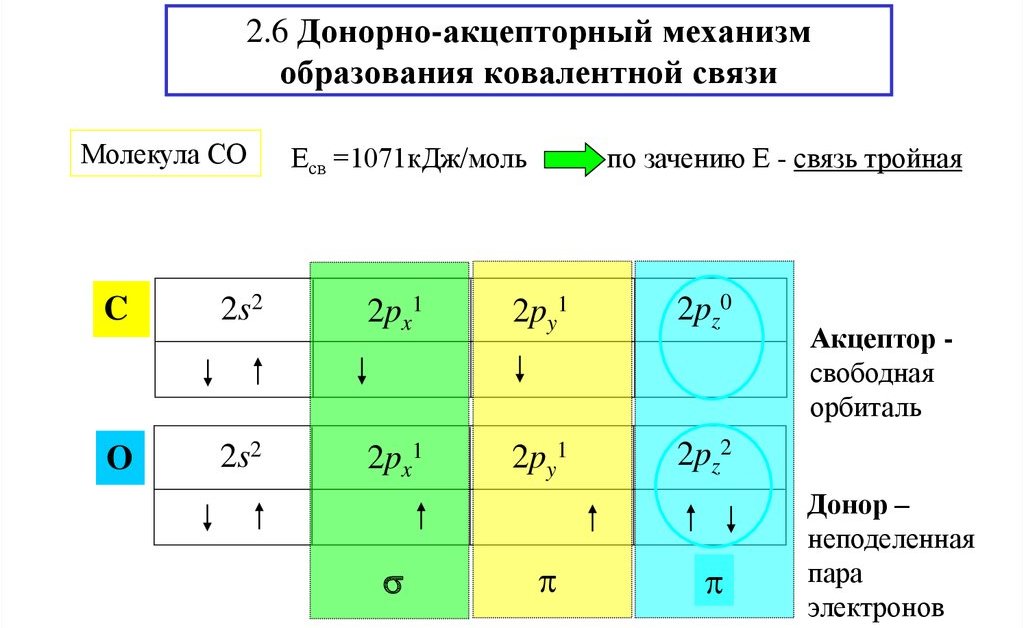
Mehanizam donor-akceptor može se uzeti kao molekula CO kao primjer. Na atomu ugljika na vanjskoj energetskoj razini nalaze se dva nesparena elektrona. Isti broj nesparenih elektrona nalazi se na atomu kisika. Kao rezultat, između atoma nastaje dvostruka veza.
Zbog para elektrona kisika i prazne orbite ugljika, za dobivanje veze koristi se mehanizam donor-akceptor.
Molekula dušične kiseline
Zbog prisutnosti tri nesparena elektrona, atom dušika u ovom spoju tvori tri varijante veza: s dvostrukim kisikom, jednim kisikom s hidroksilnom skupinom. Prema donor-akceptorskom mehanizmu, veza se formira između drugog atoma kisika i dušika.
Nepareni elektroni stavljaju se na jednu orbitalu, dok se jedan oslobađa.
Također možete pretpostaviti da atom dušika dobiva kisik pomoću elektrona. Pretvoren u amonijev kation s 4 neparena elektrona, zadržava anion zbog sila elektrostatske interakcije.
Svojstva komunikacije
Kao donor postoje molekule u kojima postoje atomi N, O, F, Cl, povezani s atomima drugih kemijskih elemenata. Akceptor je čestica s praznim elektroničkim razinama. Na primjer, to mogu biti predstavnici d-obitelji koje imaju nepopunjene d-orbitale.
U molekuli amonijaka koriste se tri nesparena elektrona dušikovog atoma za formiranje veze, a uključen je 1s-elektron od tri atoma vodika. Veze su duž tri osi p-orbitala. Molekula ima varijantu pravilne piramide, u čijim uglovima se nalaze atomi vodika, a na vrhu dušikov dušik. Kut između veza je 107 stupnjeva. Molekule sličnog oblika tvore sljedeće elemente s vodikom: antimon, arsen, fosfor.
Svojstva kovalentne veze, koja se stvara mehanizmom donor-akceptor, ne razlikuju se od karakteristika veze koju stvara mehanizam razmjene. Donori mogu biti atomi dušika, sumpora, fosfora, kisika, koji posjeduju usamljene elektronske parove na malim valentnim orbitalima.
Funkcija akceptora provodi se pomoću kationa vodika, dijela p-metala, primjerice aluminija, koji tvore AlH 4 - ion.
Također, akceptori su d-elementi koji imaju praznu energetsku ćeliju u vanjskom elektroničkom sloju.
Treba napomenuti da se sve glavne karakteristike, kao što su zasićenost, dužina, višestrukost, primjenjuju na ovaj mehanizam formiranja komunikacije.
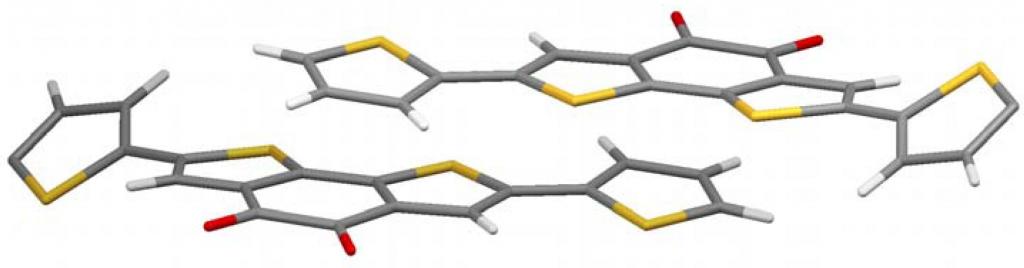
Značajke organskih spojeva
Interakcija mehanizma razmjene je moguća za organske donatore. Konkretno, među njima su π-donori, čiji je tipičan primjer tetrakis (dimetilamino) etilen (TDAE), organski akceptori (fulereni), kinodimetani s akceptorskim supstituentima.
Kemijska interakcija takvih spojeva stvara kompleks s prijenosom naboja. U njemu pozitivno nabijeni donor djeluje s negativno nabijenim akceptorom zbog sila elektrostatičke prirode. Značajni su sustavi u kojima se prijenos naboja u prizemnom elektroničkom stanju dešava djelomično, au slučaju foto ekscitacije promatra se njegov cjeloviti prijenos.
Takvi sustavi, donorsko-akceptorske dijade, triade u kojima postoji mostna skupina između akceptora i donora, koji omogućuje povećanje trajanja stanja s prijenosom električnog naboja, koriste se za proizvodnju uređaja koji pretvaraju solarnu energiju. Sličan fenomen povezan s prijenosom naboja u bilo kojem od njegovih oblika koristi se u mnogim biološkim procesima.
Stoga se detaljno istražuju značajke interakcije kroz mehanizam donor-akceptor u organskim spojevima, analiziraju se mogućnosti ubrzavanja (usporavanja) sličnih procesa, mogućnosti uvođenja dodatnih tvari (katalizatora).
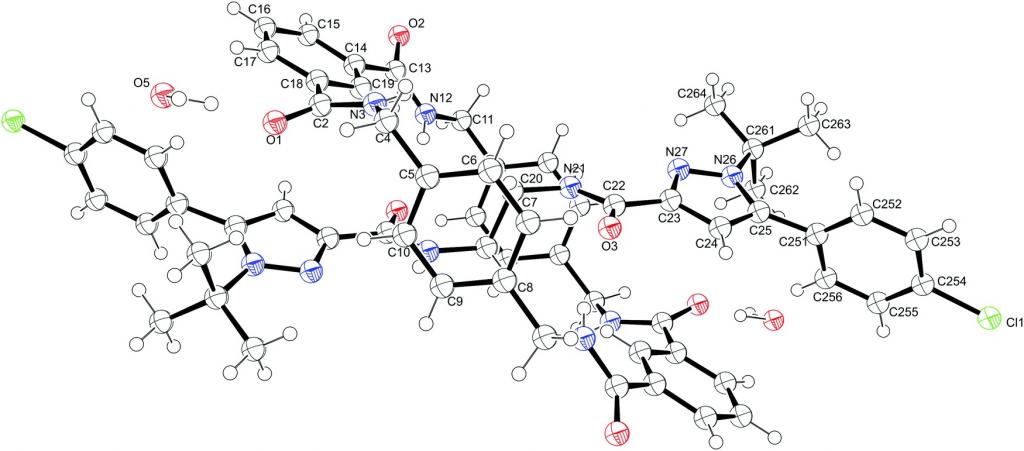
Sažimo neke
Interakcija donor-akceptor je jedna od najvažnijih manifestacija kovalentne polarne kemijske veze. Veliku pozornost posvećuje anorganskoj, analitičkoj, organskoj kemiji.
Primjerice, upravo je sa stajališta mehanizma donor-akceptor objašnjeno stvaranje kovalentno lokaliziranih veza u molekularnim ionima koordinacijskih (kompleksnih) spojeva. Veza u njima nastaje zbog usamljenog elektronskog para liganda i slobodnih orbitala sredstva za kompleksiranje. Mehanizam donor-akceptor također objašnjava formiranje međuproizvoda. Konkretno, ovo je stvaranje kompleksa s prijenosom naplate.
Postoji model donor-akceptorskog mehanizma samo u okviru koncepta valencije kao mogućnosti lokaliziranja elektronske gustoće u procesu oblikovanja kovalentnih veza. Ovaj mehanizam je osnova za formiranje različitih kompleksnih spojeva. Takva interakcija nužna je za kiselinsko-bazne transformacije vezane uz prijenos vodikovog iona (akceptor), stvaranje nanostruktura.