Kako odrediti stupanj oksidacije: periodni sustav i algoritam djelovanja
Kako odrediti stupanj oksidacije? Periodni sustav omogućuje vam da zabilježite ovu količinu za svaki kemijski element.
definicija
Za početak, pokušajmo razumjeti što je ovaj pojam. Stanje oksidacije prema periodnom sustavu, on predstavlja broj elektrona koji se prihvaćaju ili daju od strane elementa u procesu kemijske interakcije. Može imati negativnu i pozitivnu vrijednost.

Veza na tablicu
Kako se određuje stupanj oksidacije? Periodni sustav sastoji se od osam skupina postavljenih okomito. U svakoj od njih postoje dvije podskupine: glavno i sekundarno. Da bi se postavili pokazatelji za elemente, potrebno je koristiti određena pravila.
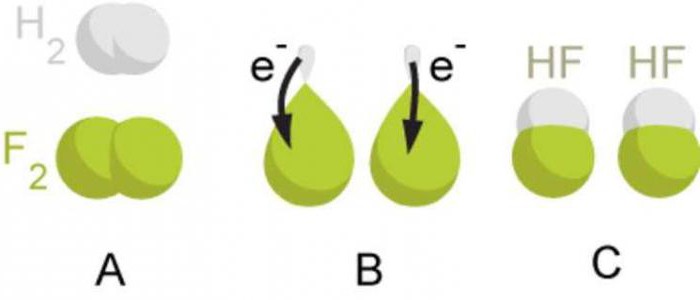
instrukcija
Kako izračunati stupanj oksidacije elemenata? Tablica omogućuje potpuno rješavanje ovog problema. Alkalni metali koji se nalaze u prvoj skupini (glavna podgrupa), stupanj oksidacije se manifestira u spojevima, odgovara +, jednak je njihovoj višoj valenciji. Metali druge skupine (podskupine A) +2 oksidacijskog stanja.
Tablica omogućuje određivanje ove vrijednosti ne samo za elemente koji pokazuju metalna svojstva, nego i za nemetale. Njihova maksimalna vrijednost odgovara najvišoj valenciji. Na primjer, za sumpor će biti +6, za dušik +5. Kako se izračunava minimalna (najniža) brojka? Tablica odgovara na ovo pitanje. Potrebno je oduzeti broj skupine od osam osoba. Na primjer, u kisiku će biti -2, u dušiku -3.
Za jednostavne tvari koje ne ulaze u kemijske interakcije s drugim tvarima, indeks koji se određuje smatra se nula.
Pokušajmo identificirati glavne akcije koje se odnose na aranžman u binarnim spojevima. Kako staviti u njih stupanj oksidacije? Periodni sustav pomaže u rješavanju problema.
Primjerice, uzmite kalcijev oksid CaO. Za kalcij, koji se nalazi u glavnoj podskupini druge skupine, vrijednost će biti konstanta jednaka +2. Za kisik koji ima nemetalna svojstva, ovaj indikator će biti negativna vrijednost i odgovara -2. Da bismo provjerili ispravnost definicije, sumiramo dobivene brojeve. Kao rezultat, dobivamo nulu, dakle, kalkulacije su točne.
Slične pokazatelje definiramo u drugom binarnom spoju CuO. Budući da se bakar nalazi u sekundarnoj podskupini (prva skupina), stoga indikator koji se istražuje može pokazivati različite vrijednosti. Stoga, da biste to utvrdili, najprije morate identificirati pokazatelj za kisik.
U nemetalu koji se nalazi na kraju binarne formule, stupanj oksidacije ima negativnu vrijednost. Budući da se taj element nalazi u šestoj skupini, pri oduzimanju od osam šest, dobivamo da oksidacijsko stanje kisika odgovara -2. Budući da u spoju nema indeksa, indeks oksidacije bakra će biti pozitivan, jednak +2.
Kako se inače koristi kemijski stol? Stupanj oksidacije elemenata u formulama sastavljenim od tri elementa također se izračunava specifičnim algoritmom. Prvo, postavite te pokazatelje u prvi i zadnji element. Za prvi, ovaj indikator će imati pozitivnu vrijednost, odgovara valenciji. Na ekstremnom elementu, koji služi kao nemetalni, ovaj pokazatelj ima negativnu vrijednost, definira se kao razlika (broj skupine uzima se iz osam). Pri izračunavanju stupnja oksidacije središnjeg elementa koristi se matematička jednadžba. U izračunima se uzimaju u obzir indeksi koji su dostupni za svaki element. Zbroj svih oksidacijskih stanja mora biti nula.
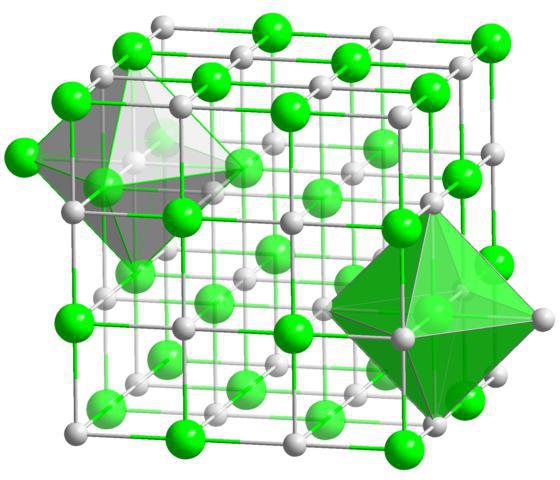
Primjer određivanja u sumpornoj kiselini
Formula za ovaj spoj je H2S04. U vodiku, oksidacijsko stanje će biti +1, u kisiku je -2. Da bismo odredili stupanj oksidacije u sumporu, izrađujemo matematičku jednadžbu: + 1 * 2 + X + 4 * (-2) = 0. Dobivamo da stupanj oksidacije sumpora odgovara +6.
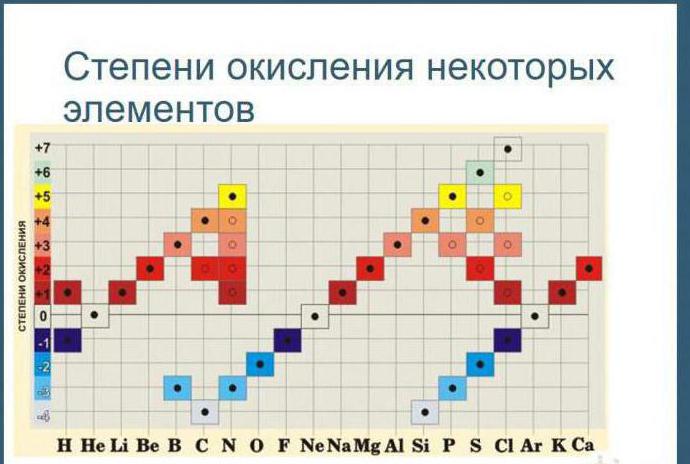
zaključak
Kada koristite pravila, možete urediti koeficijente u redoks reakcijama. Ovaj se problem bavi predmetom kemije devetog razreda u školskom kurikulumu. Osim toga, informacije o stupnjevima oksidacije omogućuju obavljanje zadataka OGE i EGE.