Kako odrediti stupanj oksidacije atoma kemijskog elementa
Formalni naboj atoma u spojevima je pomoćna vrijednost, obično se koristi u opisima svojstava elemenata u kemiji. To je uvjetno električni naboj i postoji oksidacijsko stanje. Njegova se vrijednost mijenja kao rezultat mnogih kemijskih procesa. Iako je naboj formalni, on živo karakterizira svojstva i ponašanje atoma u redoks reakcije (OVR).
Oksidacija i redukcija
U prošlosti su kemičari koristili izraz "oksidacija" da bi opisali interakciju kisika s drugim elementima. Naziv reakcije potječe od latinskog naziva kisik - oksigen. Kasnije se pokazalo da su i drugi elementi oksidirani. U ovom slučaju, one se obnavljaju - pridaju elektrone. Svaki atom u formiranju molekule mijenja strukturu svoje valentne elektronske ljuske. U ovom slučaju pojavljuje se formalni naboj čija vrijednost ovisi o broju uvjetno danih ili primljenih elektrona. Za karakterizaciju ove vrijednosti prethodno je korišten engleski kemijski pojam "oksidacijski broj", što u prijevodu znači "oksidacijski broj". Kada se koristi, pretpostavlja se da su vezni elektroni u molekulama ili ionima pripadali atomu s višom elektronegativnom vrijednošću (EO). Sposobnost da zadrži svoje elektrone i privuče ih iz drugih atoma dobro je izražena u jakim ne-metalima (halogenima, kisiku). Suprotna svojstva imaju jake metale (natrij, kalij, litij, kalcij, drugi alkalni i zemno alkalni elementi).
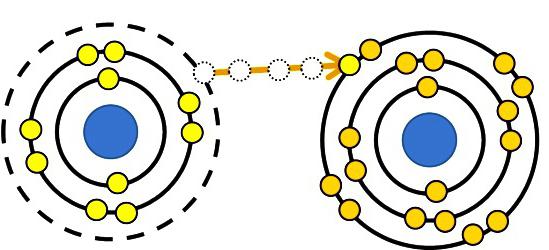
Određivanje stupnja oksidacije
Stanje oksidacije odnosi se na naboj koji bi atom mogao steći ako bi elektroni koji sudjeluju u formiranju veze bili potpuno pomaknuti u više elektronegativni element. Postoje tvari koje nemaju molekularnu strukturu (halidi alkalijskih metala i drugi spojevi). U tim slučajevima stupanj oksidacije podudara se s nabojem iona. Uvjetni ili stvarni naboj pokazuje koji se proces dogodio prije nego što su atomi stekli svoje sadašnje stanje. Pozitivna vrijednost za stupanj oksidacije je ukupan broj elektrona koji su uklonjeni iz atoma. Negativna vrijednost stupnja oksidacije je broj dobivenih elektrona. Promjenom oksidacijskog stanja kemijskog elementa procjenjuje se što se događa s njegovim atomima tijekom reakcije (i obratno). Boja tvari određuje promjene koje su se dogodile u oksidacijskom stanju. Spojevi kroma, željeza i brojnih drugih elemenata u kojima imaju različite valencije različito su obojeni.
Negativne, nulte i pozitivne vrijednosti oksidacijskog stanja

Jednostavne tvari formiraju kemijski elementi s istom vrijednošću EO. U ovom slučaju, vezni elektroni pripadaju jednako svim strukturnim česticama. Stoga, u jednostavnim tvarima, oksidacijsko stanje (H 0 2 , O 0 2 , C 0 ) je neuobičajeno za elemente. Kada atomi prihvaćaju elektrone ili se obični oblak pomiče u njihovom smjeru, uobičajeno je pisati punjenja sa znakom minus. Na primjer, F – 1 , O – 2 , C – 4 . Doniranjem elektrona, atomi stječu stvarni ili formalni pozitivni naboj. U oksidu OF2 , atom kisika daje jedan elektron na dva atoma fluora i nalazi se u oksidacijskom stanju O + 2 . Vjeruje se da u molekuli ili poliatomskom ionu više elektronegativnih atoma prima sve elektrona.
Sumpor - element koji pokazuje različita valentnost i oksidacijska stanja
Kemijski elementi glavnih podskupina često pokazuju nižu valenciju jednaku VIII. Na primjer, valencija sumpora u sumporovodiku i metalnim sulfidima - II. Element karakterizira srednja i viša valencija u pobuđenom stanju, kada atom odustaje od jednog, dva, četiri ili svih šest elektrona i pokazuje valencije I, II, IV, VI. Iste vrijednosti, samo s znakom "minus" ili "plus", imaju stupanj oksidacije sumpora:
- jedan elektron u fluorid sulfidu daje: - 1;
- u sumporovodiku najniža vrijednost: –2;
- Dioksidno intermedijerno stanje: +4;
- u trioksidu, sumporna kiselina i sulfati: +6.
U svom najvišem oksidacijskom stanju, sumpor prihvaća samo elektrone, u najnižem stupnju pokazuje jaka reducirajuća svojstva. Atomi S + 4 mogu manifestirati funkcije reducirajućih ili oksidirajućih sredstava u spojevima, ovisno o uvjetima.
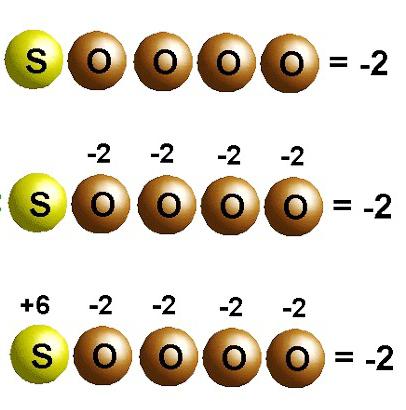
Prijelaz elektrona u kemijskim reakcijama
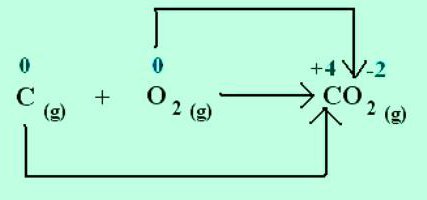
Kada se formira natrijev klorid, natrij odaje elektrone elektronegativnijem kloru. Oksidacijska stanja elemenata podudaraju se s ionskim nabojem: Na + 1 Cl –1 . Za molekule stvorene socijalizacijom i premještanjem elektronskih parova na elektronegativniji atom, primjenjuju se samo koncepti formalnog naboja. No, može se pretpostaviti da su svi spojevi sastavljeni od iona. Tada atomi, privlačeći elektrone, dobiju uvjetni negativni naboj i daju pozitivan. U reakcijama pokazuju koliko elektrona je pomaknuto. Na primjer, u molekuli ugljičnog dioksida C + 4 O - 2 , indeks u gornjem desnom kutu s kemijskim simbolom za ugljik prikazuje broj elektrona uklonjenih iz atoma. Za kisik u ovoj tvari karakterizira oksidacijsko stanje –2. Odgovarajući indeks kemijskog znaka O je broj dodanih elektrona u atomu.
Kako izračunati stupanj oksidacije
Brojanje broja elektrona koji su dani i vezani atomima može biti dugotrajno. Sljedeća pravila olakšavaju ovaj zadatak:
- Kod jednostavnih tvari oksidacijska stanja su nula.
- Zbroj oksidacije svih atoma ili iona u neutralnoj tvari je nula.
- U kompleksnom ionu zbroj oksidacijskih stanja svih elemenata mora odgovarati naboju cijele čestice.
- Što je više elektronegativni atom dobiva negativno oksidacijsko stanje, što je zapisano sa minus znakom.
- Manje elektronegativni elementi dobivaju pozitivna oksidacijska stanja, zapisani su s plus znakom.
- Kisik općenito pokazuje oksidacijsko stanje –2.
- Za vodik, karakteristična vrijednost: +1, u metalnim hidridima javlja se: H - 1.
- Fluor je najviše elektronegativan od svih elemenata, njegovo oksidacijsko stanje je uvijek –4.
- Za većinu metala, oksidacijski brojevi i valencije su isti.
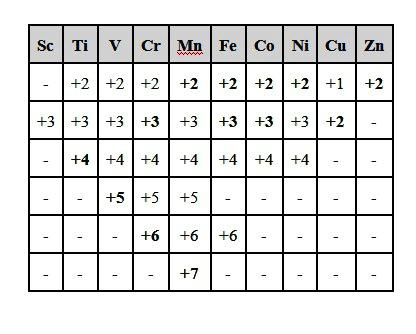
Stanje oksidacije i valencija
Većina spojeva nastaje kao rezultat redoks procesa. Prijelaz ili pomak elektrona iz jednog elementa u drugi dovodi do promjene njihova oksidacijskog stanja i valencije. Često su te vrijednosti iste. Kao sinonim za pojam "stupanj oksidacije", možete upotrijebiti izraz "elektrokemijska valencija". No postoje iznimke, na primjer, u amonijevom ionu je dušik tetravalentan. Istodobno, atom tog elementa je u oksidacijskom stanju –3. органических веществах organska tvar ugljik je uvijek tetravalentan, ali oksidacijska stanja C atoma u metanu CH4, mravlji alkohol CH3OH i HCOOH kiselina imaju različite vrijednosti: –4, –2 i +2.
Redoks reakcije

Redox uključuje mnoge od najvažnijih procesa u industriji, tehnologiji, divljim životinjama i neživoj prirodi: spaljivanje, korozija, fermentacija, unutarstanično disanje, fotosinteza i druge pojave.
Pri izradi jednadžbi OVR odabiru se koeficijenti metodom elektroničke bilance, koji djeluju u sljedećim kategorijama:
- oksidacijska stanja;
- reducirajući agens daruje elektrone i oksidira;
- oksidans uzima elektrona i smanjuje se;
- broj emitiranih elektrona mora biti jednak broju pričvršćenih.
Stjecanje elektrona od strane atoma dovodi do smanjenja njegovog stupnja oksidacije (redukcije). Gubitak jednog ili više elektrona od strane atoma popraćen je povećanjem oksidacijskog broja elementa kao posljedice reakcija. Za OVR, teče između iona jakih elektrolita u vodenim otopinama, a ne elektronska vaga, ali se češće koristi metoda polu-reakcije.