Ioni su nabijeni atomi i atomske skupine. Pojam ionskih reakcija i ionskog naboja
Po prvi put je pojam "ion" uveden 1834. godine, u kojem je zasluga Michaela Faradaya. Nakon proučavanja utjecaja električne struje na otopine soli, lužina i kiselina, došao je do zaključka da one sadrže čestice koje imaju određeni naboj. Faradayovi kationi nazivaju se ioni, koji se u električnom polju pomiču na katodu, koja ima negativan naboj. Anioni su negativno nabijene ne-elementarne ionske čestice, koje se u električnom polju kreću prema plus-anodi.
Ova se terminologija sada koristi, a čestice se dalje proučavaju, što nam omogućuje razmatranje kemijske reakcije kao posljedice elektrostatske interakcije. Mnoge reakcije se odvijaju prema ovom principu, što je omogućilo razumijevanje njihovog tijeka i odabira katalizatora i inhibitora kako bi se ubrzao njihov tijek i inhibirala sinteza. Također je postalo poznato da su mnoge tvari, osobito u otopinama, uvijek u obliku iona.
Nomenklatura i klasifikacija iona
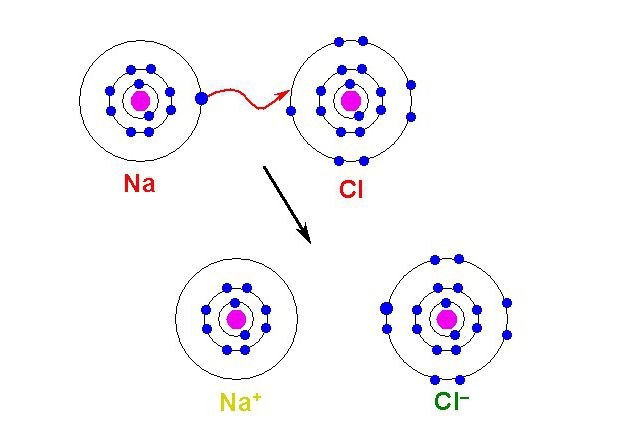
Ioni su nabijeni atomi ili skupina atoma koji su izgubili ili stekli elektrone tijekom kemijske reakcije. Oni tvore vanjske slojeve atoma i mogu se izgubiti zbog niske sile gravitacije jezgre. Tada je rezultat odvajanja elektrona pozitivan ion. Također, ako atom ima jak nuklearni naboj i usku elektronsku ljusku, jezgra je akceptor dodatnih elektrona. Kao rezultat, formira se negativna ionska čestica.
Sami ioni nisu samo atomi s viškom ili nedovoljnom elektronskom ljuskom. Može biti skupina atoma. U prirodi se najčešće javljaju upravo grupni ioni koji su prisutni u otopinama, biološkim tekućinama tijela organizama iu morskoj vodi. Postoji veliki broj tipova iona čija su imena tradicionalna. Kationi su ionske čestice koje su pozitivno nabijene, a negativno nabijeni ioni su anioni. Ovisno o sastavu nazivaju se različito. Na primjer, natrijev kation, cezijev kation i drugi. Anioni se nazivaju različito, jer se najčešće sastoje od više atoma: sulfatnog aniona, ortofosfatnog aniona i drugih.
Mehanizam stvaranja iona
Kemijski elementi u spojevima su rijetko električki neutralni. To jest, oni gotovo nikada nisu u stanju atoma. U obrazovanju kovalentna veza, što se smatra najčešćim, atomi također imaju određeni naboj, a gustoća elektrona pomiče se duž veza unutar molekule. Međutim, ionski naboj ovdje nije formiran, jer je energija kovalentne veze manja od energije ionizacije. Stoga, unatoč različitoj elektronegativnosti, neki atomi ne mogu u potpunosti privući elektrone vanjskog sloja drugih.
U ionskim reakcijama, gdje je razlika u elektronegativnosti između atoma dovoljno velika, jedan atom može uzeti elektrone vanjskog sloja iz drugog atoma. Tada je stvorena veza jako polarizirana i slomljena. Energija potrošena na to, koja stvara ionski naboj, naziva se ionizacijska energija. Za svaki atom je različit i naveden je u standardnim tablicama.
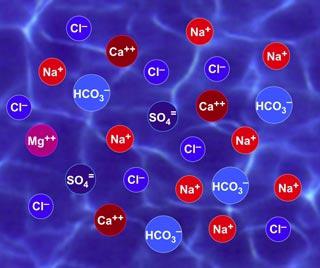
Ionizacija je moguća samo u slučaju kada je atom ili grupa atoma sposobna ili donirati elektrone ili ih prihvatiti. Najčešće se to promatra u otopini i kristalima soli. Kristalna rešetka također sadrži gotovo nepokretne nabijene čestice, lišene kinetička energija. Budući da ne postoji mogućnost kretanja u kristalu, reakcije iona najčešće se javljaju u otopinama.
Ioni u fizici i kemiji
Fizičari i kemičari aktivno proučavaju ione iz nekoliko razloga. Prvo, ove čestice su prisutne u svim poznatim agregatna stanja materije. Drugo, energija odvajanja elektrona od atoma može se izmjeriti kako bi se koristila u praktičnim aktivnostima. Treće, u kristalima i otopinama ioni se ponašaju različito. I, četvrto, ioni omogućuju električnu struju, a fizičko-kemijska svojstva otopina variraju s koncentracijama iona.
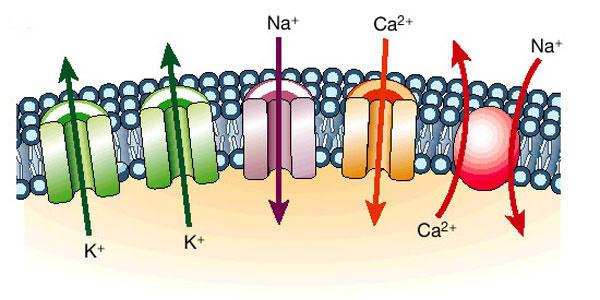
Jonske reakcije u otopini
Rješenja i sami kristali trebali bi se detaljnije razmatrati. U kristalima soli postoje odvojeno locirani pozitivni ioni, na primjer, natrijevi kationi i negativni, klorni anioni. Kristalna struktura je nevjerojatna: zbog sila elektrostatskog privlačenja i odbijanja, ioni su orijentirani na poseban način. U slučaju natrijev klorid oni tvore tzv. kristalnu rešetku dijamanta. Ovdje je svaki natrijev kation okružen sa 6 kloridnih aniona. S druge strane, svaki kloridni anion okružuje 6 klornih aniona. Zbog toga je jednostavno sol a u hladnoj i vrućoj vodi otapa se gotovo istom brzinom.

U otopini također ne postoji čvrsta molekula natrijevog klorida. Svaki od tih iona ovdje je okružen dipolima vode i kaotično se kreće u svojoj debljini. Prisutnost naboja i elektrostatskih interakcija dovodi do činjenice da otopine slane vode zamrzavaju na temperaturi nešto manjoj od nule, i vriju na temperaturi iznad 100 stupnjeva. Štoviše, ako u otopini postoje druge tvari koje mogu ući u kemijsku vezu, tada se reakcija ne događa uz sudjelovanje molekula, nego iona. Time je stvorena doktrina o kemijskoj reakciji.
Proizvodi koji se dobiju na kraju ne nastaju odmah tijekom interakcije, već se postupno sintetiziraju iz međuproizvoda. Proučavanje iona omogućilo je razumijevanje da se reakcija odvija upravo prema načelima elektrostatskih interakcija. Njihov rezultat je sinteza iona, koji su elektrostatički u interakciji s drugim ionima, stvarajući konačni ravnotežni proizvod reakcije.
rezime
Takva čestica kao ion je električki nabijeni atom ili skupina atoma, koja se dobiva tijekom gubitka ili stjecanja elektrona. Najjednostavniji ion je vodik: ako izgubi jedan elektron, on je samo jezgra s nabojem +1. On uzrokuje kiselo okruženje otopina i medija, što je važno za funkcioniranje bioloških sustava i organizama.
Ioni mogu imati i pozitivne i negativne naboje. Zbog toga, u otopinama svaka čestica ulazi u elektrostatičku interakciju s dipolima vode, što također stvara uvjete za život i prijenos signala stanicama. Štoviše, ionska tehnologija se dalje razvija. Na primjer, stvoreni su ionski motori koji su već opremili 7 NASA svemirskih misija.