Molekularna struktura tvari
Već dugo vremena znanstvenici su stvarali teorije i modele koji bi objasnili osnovna svojstva tvari i materijala koji čine svijet oko sebe.
Tijekom priče mnogi pokusi, pokusi; Otkriveni su novi zakoni i fizikalno-kemijska svojstva materijala. To je uglavnom bilo zbog otkrića pojmova "molekula" i "atomsko-molekularna struktura tvari". Razgovarajmo o njima detaljnije u ovom članku.
Pojava pojma "atomsko-molekularna struktura materije"
Čak iu doba antičke Grčke pojavila se misao da se sve na svijetu sastoji od najmanjih dijelova. Grci su te molekule i atome nazivali. Autor te hipoteze bio je Demokrit, koji je kasnije postao predak atomske teorije. Ali to znanje u tim danima nije se mnogo razvilo sve do 17. stoljeća. Sva proučavanja materijala ponovno su dovela do činjenice da se mnoge tvari sastoje od molekula, čija je strukturna jedinica atomi.
Kasnije, znanstvenici su počeli dolaziti do zaključka da se jedna vrsta minerala sastoji, na primjer, od 38% željeza i 62% kisika, a svaki od uzoraka će pokazati takav kemijski sastav. Ali ako uzmete još jedno tijelo s izvrsnim svojstvima, analiza atomsko-molekularne strukture tvari pokazat će da se sastoji od 60% željeza i 40% kisika.
Dakle, unatoč činjenici da još uvijek nije postojao određeni pojam, tijekom istraživanja pojavila se teorija da je svaka supstanca različiti skup molekula i atoma koji određuju njegova osnovna svojstva.
Razvoj koncepta "molekularne strukture materije"
 Izraz "molekula" prvi je put uveo 1811. talijanski fizikalni kemičar Amadeo Avogadro. On je postao pionir teorije atomsko-molekularne strukture.
Izraz "molekula" prvi je put uveo 1811. talijanski fizikalni kemičar Amadeo Avogadro. On je postao pionir teorije atomsko-molekularne strukture.
Potvrde te teorije pojavile su se tek 1860-ih, kada je ruski kemičar A. M. Butlerov oblikovao i bio u stanju objasniti molekularnu teoriju strukture materije. U skladu s njegovim radom, svojstva bilo koje tvari određuju način na koji su atomi u molekulama međusobno povezani, njihovom interakcijom. Znanstvenik je pretpostavio da je molekula mikročestica materijala koji se sastoji od atoma, koji može postojati neovisno.
Koncept molekule bio je fiksiran zahvaljujući radu drugog ruskog znanstvenika. Radi se o M. V. Lomonosovu.
Mnogi znanstvenici iz cijelog svijeta sudjelovali su u razvoju atomističke nastave: J. Maxwell, L. Boltzmann, J. Gibbs, R. Clausius, J. Dalton, D. I. Mendeleev, V. Roentgen, A. Becquerel, J. Thomson, M Planck i mnogi drugi. Doprinos tih ljudi molekularnoj fizici i kemiji je neprocjenjiv.
Suština molekularne teorije strukture materije
 Na temelju dugogodišnjeg kompleksa vježbi izvedena je molekularna teorija strukture materije. Postoji nekoliko osnovnih postavki te teorije: tri temeljne tvrdnje koje su više puta dokazane laboratorijskim istraživanjima:
Na temelju dugogodišnjeg kompleksa vježbi izvedena je molekularna teorija strukture materije. Postoji nekoliko osnovnih postavki te teorije: tri temeljne tvrdnje koje su više puta dokazane laboratorijskim istraživanjima:
- Svako tijelo se sastoji od najmanjih čestica - molekula i atoma, koje se također sastoje od manjih elemenata. Struktura svih tvari je povremena.
- Atomi i molekule su u stalnom kretanju kaotične prirode.
- Sve tvari međusobno djeluju na temelju elektromagnetskog privlačne sile i odbojnost.
Opravdanost molekularno-molekularne kinetičke teorije
Prva potvrda teorije jest Brownovo gibanje, koju je 1827. otkrio poznati botaničar R. Brown. Uzrok ovog fenomena je kaotičan tijek molekula u različitim smjerovima, koji se javlja kao posljedica njihovih međusobnih udaraca.
Druga potvrda te teorije bit će bezbrojni eksperimenti s procesom difuzije, tj. Sposobnost jedne tvari da prodre u drugu. Živi primjer takvog iskustva iz svakodnevnog života je parfem ili bilo koja aromatična tvar. Ako se takva tvar stavi u zatvorenom prostoru, nakon određenog razdoblja miris će se raspršiti na cijelom području.
Atom i molekula
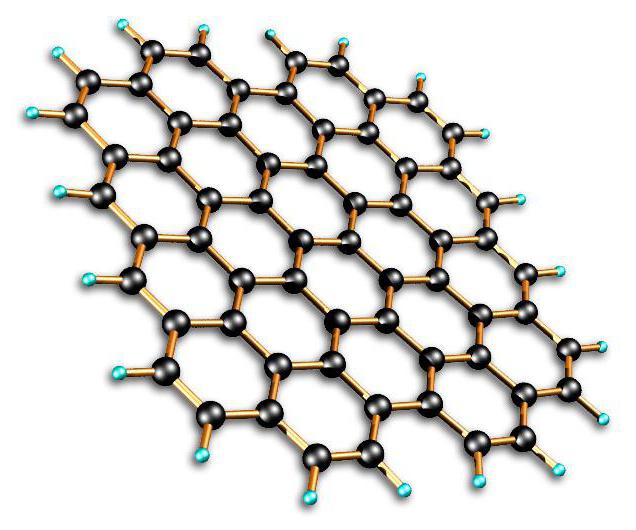
Danas su ti pojmovi već potkrijepljeni i izvedeni točno i uvjerljivo. Jednostavno rečeno, atom je kemijski nedjeljiva čestica bilo koje tvari ili materijala koji čini molekulu. I molekula je također najmanji dio nečega, ali ono što je važno je da ona postavlja osnovna svojstva tijela. Molekularna struktura tvari je kostur određenog materijala, u spojevima kojih postoje molekule. 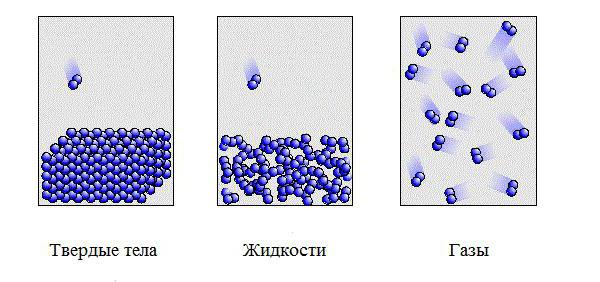
Ako je materijal karakteriziran molekulom kristalna rešetka tada on, u pravilu, ima nisku tvrdoću, lako se topi; takva tvar će biti hlapljiva ili topljiva u vodi, a električna energija se ne provodi.
Znanost koja proučava snagu interakcije tih čestica i molekularne strukture tijela naziva se molekularna fizika. Ovdje proučavamo različita svojstva tijela u različitim agregativnim stanjima.
Koje tvari imaju molekularnu strukturu?
Molekularna veza je obično slaba i dominira u organska tvar. Mnoge tvari koje su nam poznate imaju molekularnu strukturu. Na primjer, voda (H20), vodik (H2), klor (Cl2), ugljični dioksid (CO2), kisik (02), etanol, ili etil alkohol (C2H5OH), organski polimeri i mnogi drugi.
Drugim riječima, tvari s molekularnom strukturom su uglavnom plinovi. U njima su molekule udaljene jedna od druge i slabo komuniciraju. Uska povezanost čestica tvari tvori krute tvari. Jedina tekućina koja ima molekularnu strukturu je Br2. Ova tvar je vrlo hlapljiva.
Molekularni nemetali uključuju krutine kao što su I2, P4, S8. Ovi materijali su topljivi i mogu se sublimirati.