Vrste kemijskih veza. Kako povezati atome?
Kemija je nevjerojatna i, priznajem, komplicirana znanost. Iz nekog razloga, to je povezano sa svijetlim eksperimentima, raznobojnim epruvetama, gustim oblacima pare. Ali malo ljudi razmišlja o tome odakle dolazi ta “magija”. U stvari, reakcija se ne odvija bez stvaranja spojeva između atoma reaktanata. Štoviše, ovi "skakači" se ponekad nalaze u jednostavnim elementima. One utječu na sposobnost tvari da reagiraju i objasne neka od njihovih fizičkih svojstava.
Koje vrste kemijskih veza postoje i kako one utječu na spojeve?
teorija
Moramo početi s najjednostavnijim. Kemijska veza je interakcija u kojoj se atomi tvari spajaju u složenije tvari. Pogrešno je vjerovati da je to svojstveno samo spojevima kao što su soli, kiseline i baze - čak i jednostavne tvari, čije se molekule sastoje od dva atoma, imaju te “mostove”, ako je tako, možete uvjetno nazvati vez. Usput, važno je zapamtiti da se mogu ujediniti samo atomi s različitim nabojem (to su osnove fizike: jednako nabijene čestice odbijaju, a suprotne privlače jedna drugu), tako da u složenim tvarima uvijek postoji kation (ion s pozitivnim nabojem) i anion (negativna čestica) i sama veza će uvijek biti neutralna.
Sada ćemo pokušati shvatiti kako nastaje stvaranje kemijske veze.
Mehanizam obrazovanja
Svaka tvar ima određeni broj elektrona distribuiranih u energetskim slojevima. Najudaljeniji sloj, na kojem se obično nalazi najmanja količina tih čestica, smatra se najranjivijom. Njihov broj možete saznati promatrajući broj skupine (red s brojevima od jedan do osam na vrhu periodnog sustava) u kojem se nalazi kemijski element, a broj energetskih slojeva jednak je broju razdoblja (od jednog do sedam, okomita crta lijevo od elemenata).
U idealnom slučaju, postoji osam elektrona u vanjskom energetskom sloju. Ako nisu dovoljni, atom ih pokušava izvući iz druge čestice. Tijekom procesa odabira elektrona potrebnih za dovršenje vanjskog energetskog sloja nastaju kemijske veze. Njihov broj može varirati i ovisiti o broju valencija, ili nesparenih čestica (kako bi se utvrdilo koliko ih ima u atomu, potrebno je napraviti njegovu elektronsku formulu). Broj elektrona koji nemaju par bit će jednak broju formiranih veza.
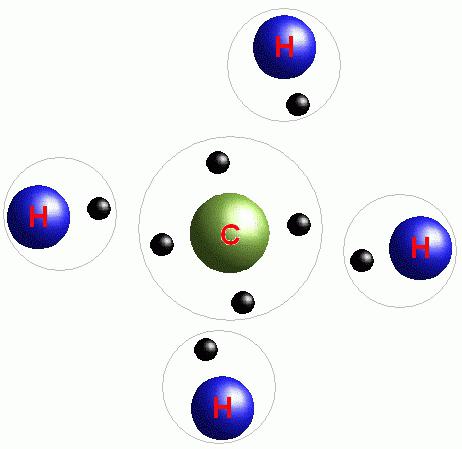
Još malo o tipovima
Vrste kemijskih veza nastalih tijekom reakcija ili jednostavno u molekuli tvari u potpunosti ovise o samom elementu. Postoje tri vrste "skakača" između atoma: ionski, metalni i kovalentni. Potonji je, pak, podijeljen na polarne i nepolarne.
Da bi se razumjelo s kojim su vezama povezani atomi, upotrijebiti neku vrstu pravila: ako su elementi u desnom i lijevom dijelu tablice (to jest, oni su metalni i nemetalni, na primjer, NaCl), tada je njihova veza izvrstan primjer ionske veze. Dva oblika nemetala kovalentna polarna veza (HCl), i dva atoma iste tvari, kombinirajući se u jednu molekulu - kovalentnu nepolarnu (Cl2, O2). Navedene vrste kemijskih veza nisu pogodne za tvari koje se sastoje od metala - postoje samo metalne veze.
Kovalentna interakcija
Kao što je ranije spomenuto, vrste kemijskih veza imaju određeni učinak na tvari. Na primjer, kovalentni "most" je vrlo nestabilan, zbog čega se spojevi s njom lako uništavaju s najmanjim vanjskim utjecajem, primjerice zagrijavanjem. Međutim, to se odnosi samo na molekularne tvari. Oni koji imaju ne-molekularnu strukturu praktički su neuništivi (savršen primjer je dijamantni kristal - kombinacija ugljikovih atoma).

Natrag na polarnu i nepolarnu kovalentnu vezu. Sa nepolarnim, sve je jednostavno - elektroni između kojih se formira "most" su na jednakoj udaljenosti od atoma. Ali u drugom slučaju, oni su prebačeni na jedan od elemenata. Pobjednik u "prenaprezanju" bit će supstanca čija je elektronegativnost (sposobnost privlačenja elektrona) veća. To je određeno posebnim tablicama, i što je veća razlika ove magnitude između dva elementa, to će biti više polarna veza između njih. Istina, jedino za što je znanje o elektronegativnosti elemenata korisno je definicija kationa (pozitivni naboj - tvar koja ima tu količinu manje) i anion (negativna čestica s boljom sposobnošću privlačenja elektrona).
Jonska veza
Nisu sve vrste kemijskih veza prikladne za kombinaciju metala i nemetala. Kao što je već spomenuto, ako je razlika u elektronegativnosti elemenata velika (a to je slučaj kada se nalaze u suprotnim dijelovima tablice), između njih se stvara ionska veza. U ovom slučaju, valentni elektroni prelaze iz atoma s nižom elektronegativnošću na atom s većim atomom, tvoreći anion i kation. Najupadljiviji primjer takve veze je spoj halogena i metala, na primjer AlCl2 ili HF.
Metalna veza
S metalima je još lakše. Oni su tuđim gornjim tipovima kemijskih veza, jer imaju svoje. Može se kombinirati oba atoma jedne tvari (Li 2 ), a različiti (AlCr 2 ), u potonjem slučaju nastaju legure. Ako govorimo o fizičkim svojstvima, onda metali u sebi spajaju plastičnost i snagu, to jest, oni se ne kolapsiraju pri najmanjem utjecaju, već jednostavno mijenjaju oblik.

Međumolekularna veza
Usput, kemijske veze u molekulama također postoje. Oni se nazivaju intermolekularni. Najčešći tip je vodikova veza, u kojoj atom vodika posuđuje elektrone iz elementa s visokom elektronegativnošću (primjerice, iz molekule vode).