Vrste kristalnih rešetki. Vrste kristalnih rešetki metala
Prilikom izvođenja mnogih fizikalnih i kemijskih reakcija, tvar prelazi u čvrsto agregatno stanje. U isto vrijeme, molekule i atomi nastoje se smjestiti u takvom prostornom poretku da bi sile interakcije između čestica tvari bile što uravnoteženije. Time se postiže čvrstoća. Atomi, jednom zauzeti određeni položaj, prave male oscilatorne pokrete, čija amplituda ovisi o temperaturi, ali njihov položaj u prostoru ostaje fiksiran. Snage privlačenja i odbijanja uravnotežuju se na određenoj udaljenosti.
Suvremene ideje o strukturi materije
Moderna znanost tvrdi da se atom sastoji od nabijene jezgre koja nosi pozitivan naboj i elektrona koji nose negativne naboje. Sa brzinom od nekoliko tisuća trilijuna obrtaja u sekundi, elektroni rotiraju u svojim orbitama, stvarajući elektronski oblak oko jezgre. Pozitivni naboj jezgre numerički je jednak negativnom naboju elektrona. Dakle, atom materije ostaje električno neutralan. Moguće interakcije s drugim atomima javljaju se kada se elektroni odvoje od prirodnog atoma i time naruše električnu ravnotežu. U jednom slučaju atomi su raspoređeni u određenom redu, koji se naziva kristalna rešetka. U drugom, zbog složene interakcije jezgara i elektrona, oni se spajaju u molekule različitih tipova i složenosti. 
Definicija kristalne rešetke
U agregatu, različiti tipovi kristalnih rešetki tvari su rešetke različite prostorne orijentacije, u čijim čvorovima postoje ioni, molekule ili atomi. Ova stabilna geometrijska prostorna pozicija naziva se kristalna rešetka materije. Udaljenost između čvorova jedne kristalne stanice naziva se razdoblje identiteta. Prostorni kutovi u kojima se nalaze čvorovi stanice nazivaju se parametri. Prema metodi izgradnje veza, kristalne rešetke mogu biti jednostavne, bazne, centrirane prema sredini i usmjerene ka tijelu. Ako se čestice materije nalaze samo u kutovima paralelepipeda, takva se rešetka naziva jednostavna. Primjer takve mreže prikazan je u nastavku: 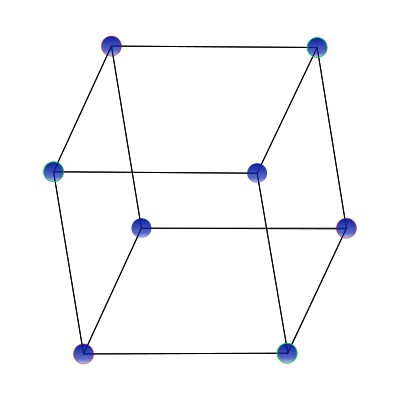
Ako se, osim čvorova, čestice tvari nalaze u sredini prostornih dijagonala, tada se takva konstrukcija čestica u tvari naziva kristalna rešetka usmjerena na tijelo. Na slici je ovaj tip prikazan vizualno. 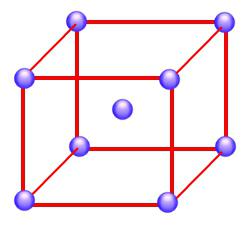
Ako, osim čvorova na vrhovima rešetke, postoji čvor, a na mjestu gdje se križaju imaginarne dijagonale paralelepipeda, tada imate rešetkastu vrstu rešetkastog tipa. 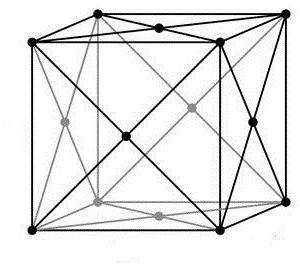
Vrste kristalnih rešetki
Različite mikročestice koje sačinjavaju tvar određuju različite vrste kristalnih rešetki. Oni mogu odrediti princip izgradnje odnosa između mikročestica unutar kristala. Fizički tipovi kristalnih rešetki - ionski, atomski i molekularni. To također uključuje različite vrste kristalne rešetke metali. Proučavanje načela unutarnje strukture elemenata uključenih u kemiju. Vrste kristalnih rešetki prikazane su detaljnije u nastavku.
Jonske kristalne rešetke
Tipovi podataka kristalne rešetke su prisutne u spojevima tipa ionske veze. U tom slučaju, rešetkasta mjesta sadrže ione s suprotnim električnim nabojem. S obzirom na elektromagnetsko polje, sile inter-ionske interakcije su prilično jake, a to uzrokuje fizička svojstva tvari. Uobičajene karakteristike su vatrostalnost, gustoća, tvrdoća i sposobnost vođenja električne struje. Ionski tipovi kristalnih rešetki prisutni su u tvarima kao što su sol, kalijev nitrat i drugo. 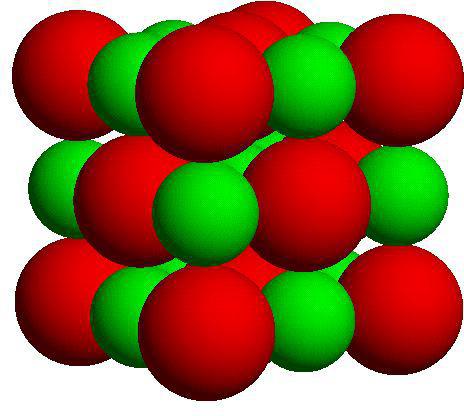
Atomske kristalne rešetke
Ova vrsta strukture tvari svojstvena je elementima čija se struktura određuje kovalentnom kemijskom vezom. Vrste kristalnih rešetki ove vrste sadrže odvojene atome u čvorovima, koji su međusobno povezani jakim kovalentne veze. Sličan tip veze nastaje kada dva identična atoma "dijele" elektrone, formirajući tako zajednički par elektrona za susjedne atome. Zbog te interakcije kovalentne veze ravnomjerno i snažno vežu atome u određenom redoslijedu. Kemijski elementi koji sadrže atomske vrste kristalnih rešetki, imaju tvrdoću, visoku točku taljenja, slabo ponašanje električna struja i kemijski neaktivni. Klasični primjeri elemenata sa sličnom unutarnjom strukturom uključuju dijamant, silicij, germanij i bor.
Molekularne rešetke
Tvari koje imaju molekularni tip kristalne rešetke su sustav stabilnih, međudjelujućih, zbijenih molekula koje se nalaze na mjestima kristalne rešetke. U takvim spojevima molekule zadržavaju svoj prostorni položaj u plinovitim, tekućim i krutim fazama. U čvorovima kristala, molekule drže slabe van der Waalsove sile, koje su desetak puta slabije od sila ionske interakcije. 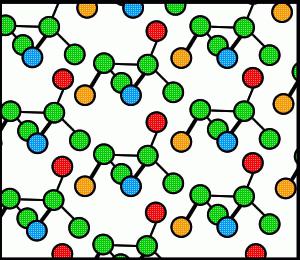
Molekule za stvaranje kristala mogu biti i polarne i nepolarne. Zbog spontanog kretanja elektrona i oscilacija jezgara u molekulama, električna ravnoteža može se pomaknuti - tako nastaje trenutni električni dipolni trenutak. Pravilno usmjereni dipoli stvaraju privlačne sile u rešetki. Ugljični dioksid i parafin su tipični primjeri elemenata s molekularnom rešetkom.
Metalne kristalne rešetke
Metalna veza je fleksibilnija i plastičnija od ionske, iako se može činiti da se obje temelje na istom principu. Tipovi kristalnih rešetki metala objašnjavaju njihova tipična svojstva - kao što su, na primjer, mehanička čvrstoća, toplinska i električna provodljivost i topljivost.
Posebnost metalne kristalne rešetke je prisutnost pozitivno nabijenih metalnih iona (kationa) na mjestima ove rešetke. Između čvorova su elektroni koji su izravno uključeni u stvaranje električnog polja oko rešetke. Broj elektrona koji se kreću unutar te kristalne rešetke naziva se elektronski plin.  U odsutnosti električnog polja, slobodni elektroni izvode kaotično gibanje, nasumično interagirajući s rešetkastim ionima. Svaka takva interakcija mijenja moment i smjer gibanja negativno nabijene čestice. Elektroni u svom električnom polju privlače katione za sebe, uravnotežujući svoj međusobni odboj. Iako se elektroni smatraju slobodnima, njihova energija nije dovoljna da napusti kristalnu rešetku, tako da su te nabijene čestice uvijek unutar njezinih granica.
U odsutnosti električnog polja, slobodni elektroni izvode kaotično gibanje, nasumično interagirajući s rešetkastim ionima. Svaka takva interakcija mijenja moment i smjer gibanja negativno nabijene čestice. Elektroni u svom električnom polju privlače katione za sebe, uravnotežujući svoj međusobni odboj. Iako se elektroni smatraju slobodnima, njihova energija nije dovoljna da napusti kristalnu rešetku, tako da su te nabijene čestice uvijek unutar njezinih granica.
Prisutnost električnog polja daje dodatnu energiju elektronskom plinu. Veza s ionima u kristalnoj rešetki metala nije trajna, pa elektroni lako napuštaju njezine granice. Elektroni se kreću duž vodova, ostavljajući iza sebe pozitivno nabijene ione.
nalazi
Kemija posvećuje veliku pozornost proučavanju unutarnje strukture materije. Vrste kristalnih rešetki različitih elemenata određuju gotovo cijeli spektar njihovih svojstava. Djelujući na kristale i mijenjajući njihovu unutarnju strukturu, moguće je postići poboljšanje željenih svojstava tvari i ukloniti nepoželjne, konvertirajuće kemijske elemente. Stoga, proučavanje unutarnje strukture okolnog svijeta može pomoći u spoznavanju suštine i načela strukture svemira.