Aldehidi i ketoni. Formula, priprema, primjena
Od organskih spojeva koji sadržavaju kisik dvije su vrste tvari od iznimne važnosti, koje se uvijek proučavaju zajedno radi sličnosti u strukturi i manifestiranih svojstava. To su aldehidi i ketoni. Upravo te molekule su temelj mnogih kemijskih sinteza, a njihova je struktura dovoljno zanimljiva za proučavanje. Razmotrimo detaljnije što su te klase spojeva.

Aldehidi i ketoni: opće značajke
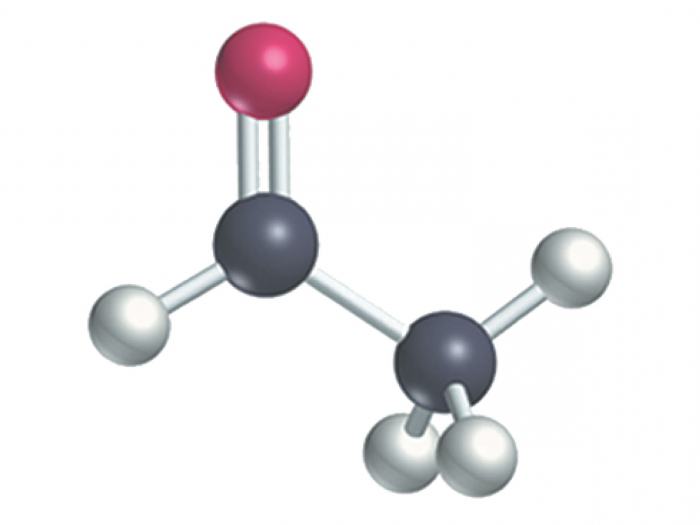
S točke gledišta kemije, klasa aldehida trebala bi uključivati organske molekule koje sadrže kisik u funkcionalnoj skupini -SON, nazvanu karbonil. Opća formula u ovom slučaju će izgledati ovako: R-COH. Po svojoj prirodi, to mogu biti i ograničavajući i nezasićeni spojevi. Među njima su i aromatični predstavnici, zajedno s alifatskim. Broj atoma ugljika u radikalnom lancu varira u prilično širokim granicama, od jednog (formaldehid ili metan) do nekoliko desetaka.
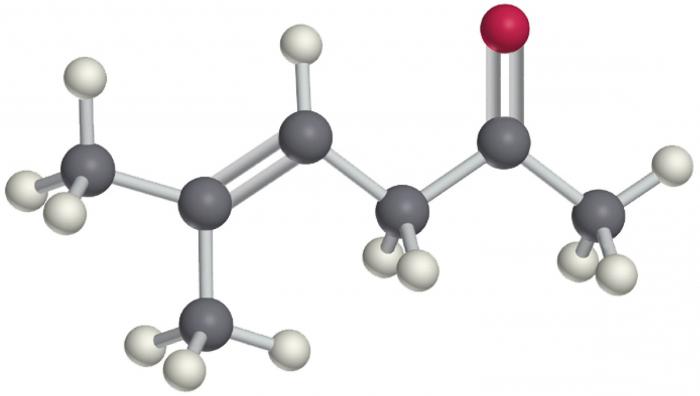
Ketoni također sadrže karbonilnu skupinu -CO, ali ona nije povezana s kationom vodika, već s drugim radikalom koji je različit ili identičan onome što ulazi u lanac. Opća formula je kako slijedi: R-CO-R ,. Očigledno je da su aldehidi i ketoni slični u prisutnosti funkcionalne skupine ovog pripravka.
Ketoni također mogu biti ograničavajući i nezasićeni, a manifestirana svojstva slična su srodnoj klasi. Postoji nekoliko primjera koji ilustriraju sastav molekula i odražavaju prihvaćene oznake formula tvari koje se razmatraju.
- Aldehidi: metanal-HCl, butanal-CH3-CH2-CH2-COH, fenilacetat - C6H5-CH2-COH.
- Ketoni: aceton ili dimetil keton - CH3-CO-CH3, metil etil keton - CH3-CO-C2H5 i drugi.
Očito je da se naziv ovih spojeva formira na dva načina:
- prema racionalnoj nomenklaturi prema radikalima i sufiksu klase -al (za aldehide) i -on (za ketone);
- trivijalno, povijesno.
Ako damo opću formulu za obje klase tvari, postat će jasno da su oni izomeri jedni od drugih: C n H 2n O. Za sebe su karakteristični sljedeći tipovi izomerije:
- za ketone, strukturu ugljikovodičnog lanca radikala i položaj -CO skupine;
- za aldehide - samo raspored atoma u lancu.

Da bi se razlikovali predstavnici oba razreda, koristiti kvalitativne reakcije većina nam dopušta identificiranje aldehida. Budući da je kemijska aktivnost ovih tvari nešto veća, zbog prisutnosti kationa vodika.
Molekularna struktura
Razmotrite kako aldehidi i ketoni izgledaju u svemiru. Struktura njihovih molekula može se odraziti u nekoliko točaka.
- Ugljikov atom izravno uključen u funkcionalnu skupinu ima sp2 hibridizaciju, koja omogućava da dio molekule ima ravan prostorni oblik.
- U tom slučaju, polarnost veze C = O je jaka. Budući da je elektronegativniji, kisik uzima većinu svoje gustoće, koncentrirajući na sebe djelomično negativan naboj.
- U aldehidima, OH veza je također visoko polarizirana, što čini atom vodika pokretnim.
Kao rezultat toga, ispada da takva struktura molekula omogućuje da se predmetni spojevi oksidiraju i reduciraju. Formula aldehida i ketona s redistribuiranom elektronskom gustoćom omogućuje predviđanje reakcijskih produkata u kojima te tvari sudjeluju.
Povijest otkrića i proučavanja
Poput mnogih organski spojevi tek u 19. stoljeću ljudi su uspjeli izolirati i proučavati aldehide i ketone, kada su se vitalistički pogledi potpuno srušili i postalo je jasno da se ti spojevi mogu oblikovati sintetičkim, umjetnim sredstvima, bez sudjelovanja živih bića.
Međutim, 1661. R. Boyle je uspio dobiti aceton (dimetil keton), kada je kalcij acetat podvrgnuo zagrijavanju. Ali nije mogao detaljno proučiti tu tvar i imenovati je, odrediti sustavnu poziciju među ostalima. Tek 1852. Williamson je uspio privesti kraju ovo pitanje, a zatim je započela povijest detaljnog razvoja i akumulacije znanja o karbonilnim spojevima.

Fizička svojstva
Uzmite u obzir fizikalna svojstva aldehida i ketona. Počnimo s prvim.
- Prema stanju agregacije, prvi predstavnik je metan, sljedećih jedanaest je tekućina, više od 12 atoma ugljika su dio čvrstih aldehida normalne strukture.
- Točka vrenja: ovisi o broju C-atoma, što su više, to je veća. Štoviše, što je lanac razgranati, to je niža vrijednost temperature.
- Za tekuće aldehide, viskoznost, gustoća i indeks loma također ovise o broju atoma. Što ih je više, tako su i više.
- Plinoviti i tekući aldehidi se vrlo dobro otapaju u vodi, međutim krutine to praktički ne mogu učiniti.
- Miris predstavnika je vrlo ugodan, često su to mirisi cvijeća, parfema, voća. Samo oni aldehidi, u kojima je broj ugljikovih atoma 1-5, su jako i neugodno mirisne tekućine.
Ako odredite svojstva ketona, možete odabrati i one glavne.
- Agregatna stanja: donji predstavnici su tekućine, a masovniji su čvrsti spojevi.
- Miris je oštar, neugodan za sve predstavnike.
- Topivost u vodi dobra je za niže, izvrsna je za sve u organskim otapalima.
- Hlapljive tvari, ovaj pokazatelj premašuje one u kiselinama, alkoholima.
- Točka ključanja i točka taljenja ovise o strukturi molekule, uvelike varira od broja ugljikovih atoma u lancu.
To su glavna svojstva razmatranih spojeva, koji pripadaju skupini fizičkih.
Kemijska svojstva
Najvažnije je što aldehidi i ketoni reagiraju s kemijskim svojstvima tih spojeva. Stoga ih smatramo nužno. Prvo, bavite se aldehidima.
- Oksidacija u odgovarajuće karboksilne kiseline. Opći pogled na jednadžbu reakcije: R-COH + [O] = R-COOH. Aromatični predstavnici još lakše ulaze u takve interakcije, a također mogu oblikovati estere industrijske važnosti. Kao oksidirajuća sredstva koriste se: kisik, Tollens reagens, bakar (II) hidroksid i drugi.
- Aldehidi se manifestiraju kao jaka redukcijska sredstva, dok se pretvaraju u ograničavajući monohidrični alkoholi.
- Interakcija s alkoholima u obliku produkata acetala i poluacetala.
- Posebne reakcije - polikondenzacija. Kao rezultat, formiraju se fenolformaldehidne smole koje su važne za kemijsku industriju.
- Nekoliko specifičnih reakcija sa sljedećim reagensima:
- vodeno-alkoholne lužine;
- Grignardov reagens;
- hidrosulfiti i drugi.
Kvalitativna reakcija na ovu klasu tvari je reakcija "srebrnog ogledala". Kao rezultat, on formira metalno reducirano srebro i odgovarajuću karboksilnu kiselinu. Potrebna je otopina amonijaka srebrnog oksida ili reagensa Tollins.
Kemijska svojstva ketona
Alkoholi, aldehidi, ketoni su po svojim svojstvima slični, jer svi sadrže kisik. Međutim, već u fazi oksidacije postaje jasno da su alkoholi najaktivniji i lako osjetljivi spojevi. Ketoni su najteže oksidirati.
- Oksidirajuća svojstva. Kao rezultat, formiraju se sekundarni alkoholi.
- Hidrogenacija također dovodi do gore navedenih proizvoda.
- Keto-enolni tautomerizam je specifično specifično svojstvo ketona za uzimanje beta oblika.
- Reakcije aldolne kondenzacije s formiranjem beta-ketospirtova.
- Također, ketoni su u mogućnosti komunicirati sa:
- amonijak;
- hidrocianična kiselina ;
- hidrosulfitom;
- hidrazin;
- ortosilikatna kiselina.
Očito je da su reakcije takvih interakcija vrlo složene, osobito one koje su specifične. Sve su to glavne značajke koje izlažu aldehidi i ketoni. Kemijska svojstva su temelj mnogih sinteza važnih spojeva. Stoga je poznavanje prirode molekula i njihovog karaktera tijekom interakcija izuzetno važno u industrijskim procesima.
Reakcije adhezije aldehida i ketona
Već smo pregledali ove reakcije, ali im nismo dali takvo ime. Sve interakcije mogu se pripisati dodavanju, zbog čega je karbonilna skupina pokazala aktivnost. Ili bolje rečeno, pokretni atom vodika. Upravo zato u ovom slučaju prioritet imaju aldehidi, zbog njihove bolje reaktivnosti.
Koje su tvari moguće reakcije aldehida i ketona za nukleofilnu supstituciju? Ovo je:
- Hidrocianična kiselina, cijanhidrin se formira - sirovina u sintezi aminokiselina.
- Amonijak, amini.
- Alkoholi.
- Voda.
- Natrijev hidrosulfat.
- Grignardov reagens.
- Tioli i drugi.
Ove reakcije su od velike industrijske važnosti, budući da se proizvodi koriste u različitim područjima ljudske djelatnosti.

Načini za dobivanje
Postoji nekoliko osnovnih metoda kojima se sintetiziraju aldehidi i ketoni. Dobivanje u laboratoriju i industriji može se izraziti na sljedeće načine.
- Najčešća metoda, uključujući u laboratorijima, je oksidacija odgovarajućih alkohola: primarno u aldehide, sekundarne u odnosu na predstavnike ketona. Kromati, bakreni ioni, kalijev permanganat mogu djelovati kao oksidirajuće sredstvo. Opći pregled reakcije: R-OH + Cu (KMn04) = R-COH.
- U industriji se često koristi metoda koja se temelji na oksidaciji alkena - oksosinteza. Glavno sredstvo je sintetski plin, smjesa CO2 + H2. Rezultat je aldehid s velikim brojem atoma po lancu ugljika. R = RR + CO2 + H2 = RRR-COH.
- Oksidacija alkena ozonom - ozonoliza. Rezultat također sugerira aldehid, ali osim toga, keton je također u smjesi. Ako su proizvodi mentalno povezani, uklanjajući kisik, postaje jasno što je izvorni alken uzet.
- Kucherova reakcija - hidratacija alkina. Obavezno sredstvo - živine soli. Jedna od industrijskih metoda za sintezu aldehida i ketona. R2RR + Hg2 + + H20 = RR-COH.
- Hidroliza dihalogenskih derivata ugljikovodika.
- Redukcija karboksilnih kiselina, amida, nitrila, kiselinskih klorida, estera. Kao rezultat, formiraju se i aldehid i keton.
- Piroliza smjese karboksilnih kiselina preko katalizatora metalnih oksida. Smjesa treba ispariti. Dno crta je eliminacija između molekula ugljičnog dioksida i vode. Rezultat je aldehid ili keton.
Aromatski aldehidi i ketoni priređeni su na drugi način, budući da ti spojevi imaju aromatski radikal (fenil, na primjer).
- Prema Friedel-Craftsu: u početnim reagensima postoji aromatski ugljikovodik i keton supstituiran dihalogenom. Katalizator - ALCL 3 . Rezultat je aromatski aldehid ili keton. Drugi naziv za proces je acilacija.
- Oksidacija toluena različitim agensima.
- Dobivanje aromatskih karboksilnih kiselina.
Naravno, industrija pokušava koristiti one metode u kojima su sirovine što jeftinije, a katalizatori su manje toksični. Za sintezu aldehida je oksidacija alkena kisikom.

Industrijske primjene i značenje
Upotreba aldehida i ketona provodi se u industrijama kao što su:
- lijekovi;
- kemijska sinteza;
- lijek;
- područje parfumerije;
- prehrambena industrija;
- proizvodnja boja i lakova;
- sinteza plastike, tkanina i još mnogo toga.
Možete odrediti više od jednog područja, jer se godišnje sintetizira samo formaldehid oko 6 milijuna tona godišnje! Njegova 40% -tna otopina naziva se formalin i koristi se za pohranu anatomskih objekata. On također ide na proizvodnju lijekova, antiseptika i polimera.
Octeni aldehid, ili etanal, također masovno proizveden proizvod. Godišnja potrošnja u svijetu iznosi oko 4 milijuna tona, što je temelj mnogih kemijskih sinteza na kojima se stvaraju važni proizvodi. Na primjer:
- octena kiselina i njen anhidrid;
- celulozni acetat;
- lijekove;
- butadien - baza gume;
- etil alkohol ;
- acetatna vlakna.
Aromatski aldehidi i ketoni sastavni su dio mnogih okusa, hrane i parfema. Većina njih ima vrlo ugodne cvjetne, citrusne, biljne arome. Na temelju toga možete proizvesti:
- razni osvježivači zraka;
- toalet i parfemska voda;
- razna sredstva za čišćenje i deterdžente.
Neki od njih su aromatizirani dodaci hrani dopušteni za konzumaciju. Njihov prirodni sadržaj u eteričnim uljima, voću i smolama dokazuje mogućnost takve uporabe.
Pojedinačni predstavnici
Takav aldehid, kao citral, je tekućina visoke viskoznosti i jake arome limuna. U prirodi se nalazi u eteričnim uljima potonjeg. Također u sastavu eukaliptusa, sirka, kebaba.
Dobro poznata područja primjene:
- pedijatrija - snižavanje intrakranijalnog tlaka;
- normalizacija krvnog tlaka u odraslih;
- komponenta lijeka za organe vida;
- dio mnogih mirisa;
- protuupalni i antiseptički;
- sirovine za sintezu retinola;
- okus za prehrambene svrhe.