Automatizacija srca - opis, mehanizam i značajke
Srce živog organizma zanimljiv je proizvod evolucije, orgulje čiji se rad temelji na interakciji humoralnog i živčanog sustava uz zadržavanje vlastite autonomije. I neka danas znanstvenici znaju praktički sve što se tiče njegove strukture i aktivnosti, teško je upravljati njime. Međutim, to treba naučiti, što će biti polazna točka za povećanje životnog vijeka. Automatizacija srca, njegov metabolizam i povezanost kontrakcije s membranskim potencijalom vrlo su važni za medicinu. Njihovo proučavanje i ispravno razumijevanje omogućuje odabir kompetentnijeg tretmana za vaše pacijente.
Automatizacija pejsmejkera
Automatizacija srca je njezina sposobnost samostalnog stvaranja akcijskog potencijala u dijastolnoj fazi. To je temelj autonomije ovog tijela, zbog čega ne ovisi o aktivnosti mozga. Štoviše, evolucijsko visoko kvalitetno srce razvilo se mnogo ranije od mozga i središta kardiovaskularnog tona.
Supstrat i uzrok automatizma srca sadržani su u najosnovnijim mehanizmima povezanim s djelovanjem ionskih kanala. Oni tvore razliku struja na suprotnim stranama membrane, koja se s vremenom mijenja, stvarajući impulsnu električnu struju. Njeno provođenje u posebnim stanicama do potencijalno ovisnih tkiva temelj je srčane aktivnosti.
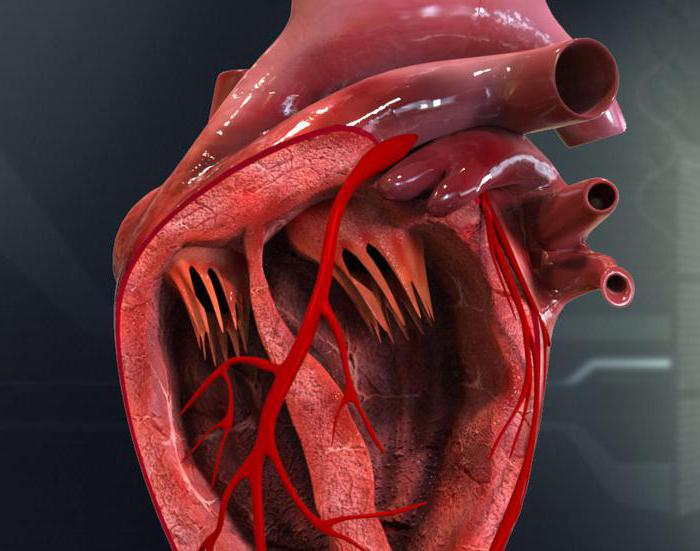
Struktura sustava srčane provodljivosti
Osim mišićnog tkiva, srce ima svoj vlastiti sustav generiranja ritma, zbog čega organ ne ovisi o kontroli mozga i kralježnične moždine. Ovaj je sustav autonoman i ovisi samo o funkcioniranju ionskih kanala atipičnih kardiomiocita. Oni su podijeljeni u 3 vrste ovisno o značajkama strukture i funkcija. Prvi tip - pejsmejker atipične stanice P-cardiomyocytes. Druga vrsta stanica su vodljive prijelazne stanice, treći tip su stanice Purkinyeja i Hisovih vlakana lociranih subendokardijalno.
P-kardiomiociti su ovalne ili okrugle stanice, pejsmejkeri, zbog kojih se ostvaruje srčani automatizam. Oni su u velikom broju u samom središtu sinusnog čvora. Njihova mala količina nalazi se u atrioventrikularnom čvoru provodnog sustava.
Srednji kardiomiociti su duguljasti, izduženi, razlikuju se malim brojem miofibrila, ali su manje veličine od kontraktilnih kardiomiocita. Nalaze se na periferiji sinusnog i atrioventrikularnog čvora. Njihova je zadaća provesti impuls prema njegovom snopu i vlaknima koji leže između endokardija i površinskih slojeva miokarda.
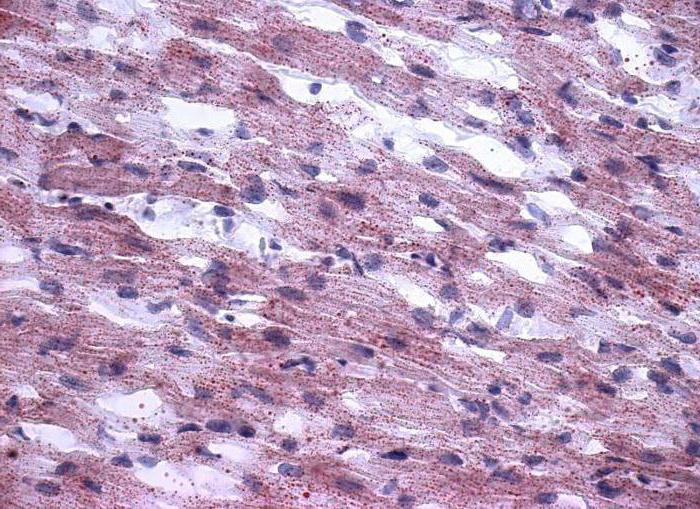
Stanice provodnog sustava, lokalizirane u snopu vlakana His i Purkinje, imaju posebnu strukturu i karakterizirane su niskom glikoliznom učinkovitošću zbog prevladavanja anaerobne varijante. Oni su spljošteni i duži od srednjih kardiomiocita, a njihova veličina je nešto veća od kontraktilnih stanica. U citoplazmi postoji mala količina mišićnih vlakana. Njihov zadatak je povezivanje čvorova automatskog srca i kontraktilnog miokarda, tj. Provođenje pulsa od pejsmejkera do srčani mišić.
Normalni ritam i širenje pulsa u srcu
Kontrakcija srca je rezultat generiranja srčanog impulsa, akcijskog potencijala stanica pejsmejkera sinusnog čvora. Ovdje je maksimalni broj pejsmejkera, koji stvaraju ritam s frekvencijom od 60-100 puta u minuti. Prenosi se kroz vodljive stanice u atrioventrikularni čvor, čija je glavna zadaća odgoditi ritam. Ekscitacija doseže AV čvor preko snopova provodnih kardiomiocita, koji također posjeduju automatizam. Međutim, oni mogu generirati ritam s učestalošću od 30-40 puta u minuti.
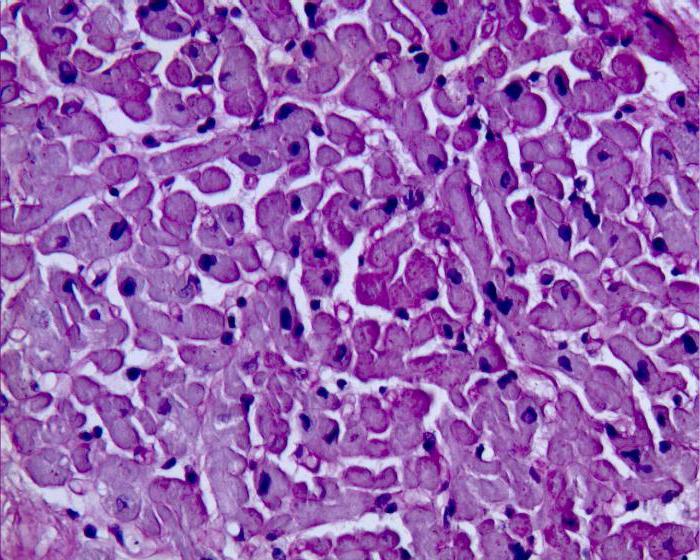
Nakon AV čvora, ritam se normalno širi provođenjem atipičnih kardiomiocita na njegov snop, čiji je automatizam izuzetno nizak - do 20 impulsa u minuti. Tada ekscitacija doseže konačni element provodnog sustava - Purkinjeva vlakna. Njihova sposobnost generiranja ritma je čak i niža - do 10 u minuti. Štoviše, glavni pejsmejker, tj. Sinusni čvor, stvara češće impulse. I svako sljedeće širenje akcijskog potencijala potiskuje ritam nižih podjela.
Smanjenje sposobnosti sustava srčane provodljivosti da generira visokofrekventni ritam od sinusnog čvora do Purkinjevih vlakana naziva se gradijent automatizma. Ovaj proces se objašnjava smanjenjem brzine depolarizacije membrane: u sinusnom čvoru spontana polagana dijastolička depolarizacija je što je moguće viša, a kako se kreće u distalne dijelove to je najmanje. Gradijent automatizacije usmjeren je prema dolje, što je znak normalno funkcionirajućeg sustava srčane provodljivosti.
Promjena membranskog potencijala pejsmejkera
U dijastoli srca, u stanicama pejsmejkera, uočava se sljedeći ionski obrazac: količina kalijevih kationa iznad natrijevih iona značajno prevladava u stanici. Izvan stanice koncentracija kationa je upravo suprotna. Istovremeno, potencijal mirovanja ćelije pejsmejkera je -60 mV. Kalijeve struje u mirovanju imaju nisku učinkovitost, budući da na membrani ima vrlo malo ionskih kanala za kalij. To ih razlikuje od kontraktilnih miocita, gdje je potencijal mirovanja približno -90 mV.

Rad HCN kanala i lansiranje SMDD
Spontana polagana dijastolička depolarizacija (SMDD), karakteristična za svaki atipični kardiomiocit, dovodi do promjene membranskog potencijala i proces je odgovoran za automatsko funkcioniranje srca. SMDD započinje s radom HCN-ionskih kanala. To su tzv. Kationski kanali aktivirani hiperpolarizacijom koje pokreću ciklički nukleotidi. CAMP ih aktivira u vrijeme hiperpolarizacije, tj. U mirovanju od -60 mV. To znači da nakon svake repolarizacije, čim se stanica "napuni" i njezin membranski potencijal dosegne vrijednost od -60 mV, otvara se HCN kanal. Kao rezultat, kationi ulaze u stanicu, uglavnom kroz natrijeve kanale.
Zbog malog dotoka natrija, membranski potencijal će se povećati na oko -57 mV. Ovo je signal za aktiviranje kalcijev kanal T-tip, namijenjen opskrbi kationa Ca2 +. Aktiviraju se slabom depolarizacijom i nazivaju se pod-pragom. To znači da će povećanje membranskog potencijala na -55-57 mV dovesti do otvaranja transportnih kanala za daljnju depolarizaciju. Ovi ionski kanali se aktiviraju natrijevim ionima koji se nalaze u stanici, ubrizgavaju u kalup malo kalcija i povećavaju potencijal do -50 mV, nakon čega se brzo zatvaraju.
Rad izmjenjivača natrij-kalcij
Prisutnost kalcija u citoplazmi je signal za otvaranje mehanizma izmjenjivača natrij-kalcij. Smisao njegova rada je sljedeći: aktivnim transportom, kalcijevi ioni s nabojem 2+ oslobađaju se u izvanstanični prostor, a ioni Na + ulaze u stanicu. Jedan natrijev kation u citoplazmi prima 3 natrijeva iona, što dovodi do povećanja naboja membrane i rasta membranskog potencijala do -40 mV.
Generiranje akcijskih potencijala
Nakon dostizanja potencijala od -40 mV, otvara se kalcijev kanal ovisan o potencijalu. Mogu dugo raditi i dovesti do naglog povećanja koncentracije kalcijevih iona unutar stanice. To je najvažniji proces u djelovanju ionskih kanala, jer zbog njega dolazi do lavinskog rasta membranskog naboja, koji tvori akcijski potencijal (AP). Taj ionski proces podiže membranski potencijal na vrhunac na razini od +30 mV, nakon čega je stanica potpuno depolarizirana i generira potreban impuls za rad srca.
Depolarizacija membrane je aktivator ne samo kalcijeve struje, nego i kalija. Međutim, ionski kanali koji oslobađaju ione kalija izvana rade s odgodom. Stoga se njihov odabir javlja na vrhuncu formiranja PD. Istovremeno, kalcijska struja kroz L-kanale potpuno se zaustavlja, a membranski potencijal se ponovno smanjuje uklanjanjem kalijevih iona u odnosu na koncentracijski gradijent aktivnim transportom. Naboj membrane se ponovno spušta na -60 mV, započinjući proces SMDD nakon uravnoteženja početnih koncentracija kalcija i natrija.
Priroda automatizma i njegova regulacija
Atipični kardiomiocit može obavljati svoju funkciju zbog kalcijeve struje kroz spore ionske kanale, zbog čega se stvara akcijski potencijal. Ovaj proces je osnova ekscitabilnosti miokarda. Nasuprot tome, SMDD ima drugačiju svrhu. Njegova je zadaća automatski pokrenuti početak depolarizacije s određenom frekvencijom. Prisutnost SMDD faze je priroda automatizma srca, sposobnost spontanog stvaranja pobuđenja u stanicama pejsmejkera.
Stopa razvoja SMDD-a izravno je regulirana somatskim autonomnim živčanim sustavom. U mirovanju je minimalan zbog inhibicijskog učinka vagusni živac. Međutim, to ne znači da se automatizacija srca zaustavlja. Jednostavno, SMDD će trajati duže, što će osigurati dulju dijastolu. Smanjuje se intenzitet metaboličkih procesa u miokardiju i srčanom provodnom sustavu, a organ je pod manjim stresom.
Učinak ubrzavanja spontane sporije dijastoličke depolarizacije postiže se djelovanjem simpatičkog živčanog sustava i njegovog posrednika adrenalina. Zatim se povećava brzina DMDD, što osigurava ranu aktivaciju izmjenjivača natrij-kalcij i otvaranje kalcijevih kanala sporog tipa. Rezultat je ubrzanje učestalosti ritma, povećane frekvencije srca, povećanje potrošnje energije.
Farmakološki učinci na automatiku srčanog stimulatora
Inhibirati mehanizam automatskog srca i farmakološku metodu. Pomoću nekih ljekovitih, opojnih i otrovnih tvari moguće je ubrzati stvaranje ritma, usporiti ga ili ga potpuno blokirati. Naravno, zbog etičkih razloga, otrovne i opojne tvari u ovoj publikaciji neće se razmatrati.
Sljedeće skupine lijekova mogu usporiti brzinu stvaranja ritma: blokatori adrenergičnih lijekova i blokatori kalcijevih kanala. To su sigurni lijekovi, osobito selektivni beta-1-blokatori. Njihov mehanizam djelovanja svodi se na inaktivaciju receptora, na koji je normalno vezan adrenalin.
Blokiranjem receptora, lijek eliminira aktivirajući učinak adrenalina na brzinu generiranja pulsa, štiteći miokard od prekoračenja energije i neučinkovitog otpada. To je vrlo delikatan i djelotvoran mehanizam, a beta-blokatori su značajno povećali životni vijek mnogih bolesnika sa srčanim bolestima.
Blokatori kalcijevih kanala
Druga skupina tvari ima suptilniji mehanizam djelovanja, iako vrlo učinkovit. Oni blokiraju spore kanale ulaska kalcija, zbog čega nastaje akcijski potencijal. Na membrani atipičnog kardiomiocita oni su izraženi u velikom broju, pa je stoga njihova potpuna blokada, koja bi se pretvorila u nemogućnost razvoja automatske funkcije srca, nemoguća.
Korištenjem lijeka postiže se tek neznatno usporavanje stope stvaranja akcijskog potencijala, što pomaže u smanjenju učestalosti ritma. Takav mehanizam je vrlo pouzdan i omogućuje liječenje aritmija, pri čemu se ne koristi supstrat automatske funkcije srca, već akcijski potencijal. To jest, blokatori kalcijevih kanala ne utječu na spontanu polaganu dijastoličku depolarizaciju.
Komunikacija automatizma srca i vitalne aktivnosti
Srce se sastoji od mišićnog tkiva, vezivnog i nervoznog. Potonja ima u njoj najmanju vrijednost, jer je zastupljena samo vagusnim živcem. Vezivno tkivo osigurava prisutnost ventila i održava strukturu tijela, dok je za sve ostalo odgovoran mišić. Derivati mišićnih stanica su atipični kardiomiociti. To znači da su automatizacija srca, provodni sustav srca i njegov mišićni dio funkcionalna cjelina. Oni tvore autonomno tijelo koje se može regulirati, ali ne isključuje utjecaj drugih tjelesnih sustava.
Koncepti kao što su automatika srca, priroda automatizma, gradijent automatike međusobno su povezani i čuvaju zdravlje. Oni podržavaju život u tijelu, osiguravajući stalnu opskrbu krvi tkivima. Krv u arterijama je transportni medij za hranjive tvari i vezani kisik. Time se ostvaruje proces staničnog disanja i razmjene energije. To je temelj funkcioniranja višestaničnog organizma, čije je neizbježna smrt neizbježna.