Benzojeva kiselina: povijest otkrića, svojstva, priprema, uporaba reagensa
Razmatra se najopsežnija klasa kemijskih spojeva organska tvar. Njihova raznolikost povezana je s jedinstvenom sposobnošću ugljika da stvori atomske lance visoke stabilnosti. Jedan od predstavnika organskih spojeva s benzenskim prstenom je benzojeva kiselina. U ovom članku će biti opisana zanimljiva povijest otkrića, širok raspon primjena, metode proizvodnje, koristi i štetnosti tvari za ljude.
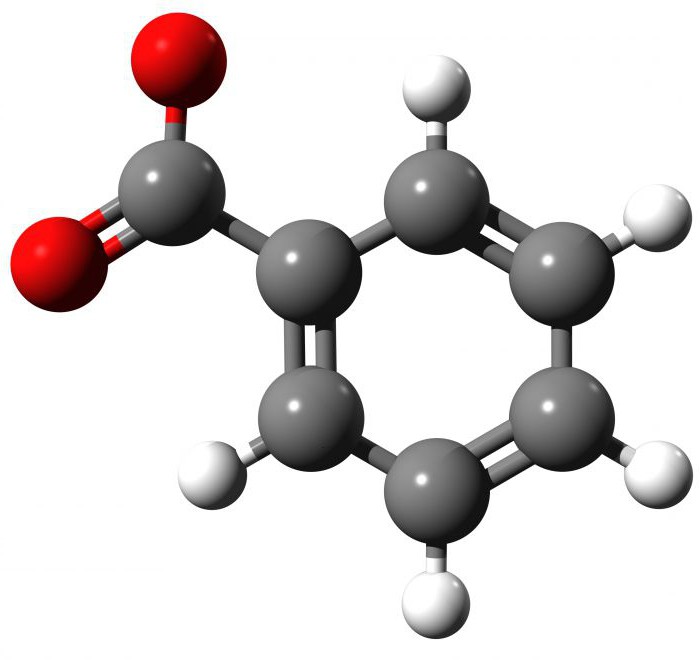
Opis, fizička svojstva spoja
Na sobnoj temperaturi benzojeva kiselina izgleda kao bijeli prah. Ako ga pregledate pod mikroskopom, vidjet ćete da su kristali u obliku igala ili ljusaka (tableta). Spoj ima jak miris. Kemijska formula ove karboksilne (organske) kiseline je C6H5COOH ili C7H6O2. Kada se zagrije na 122,4 ° C, počinje se topiti, a na 249 ° C - do vrenja, daljnje povećanje temperature na 370 ° C će dovesti do toplinske razgradnje. Lako je izračunati molarnu masu spoja, ona je 122,12 g / mol. Reagens je vrlo slabo topljiv u vodi, te u etanolu i eterima - dobro. Reagens C6H5COOH je slaba kiselina, njegova konstanta disocijacije je 4.202.

sublimacija
Reagens se lako sublimira. U tom slučaju, kristali sublimiraju iz pare, zaobilazeći tekuću fazu. Takvu tranziciju lako je slijediti kroz iskustvo "zime u čaši" ili "umjetnog snijega". Da bi se to postiglo, mala količina reagensa i grančice smreke stavljaju se u kemijski pripremljene kemikalije. Na vrhu se stavlja tikvica okruglog dna s vodom, koja će poslužiti kao hladnjak i poklopac. Dizajn postavljen na tronožac i podvrgnut grijanju. U tom slučaju reagens počinje sublimirati. Parovi, koji ulaze u bočice hladnom vodom, kristaliziraju i pretvaraju se u "snijeg". Nalaze se na grani smreke i zidovima stakla u obliku tankih igala. Strašan prizor! On ima praktičnu primjenu - sublimacija se koristi za dobivanje benzojeve kiseline.
Povijest otkrića
Benzojeva kiselina dobila je svoje ime zbog prirodnog spoja iz kojeg je prvi put izoliran, taman. Taj je proces opisao Nostradamus 1556. godine, a malo kasnije francuski alkemičar Blaise de Vigener. Benzoinska smola dugo se smatrala jedinim izvorom sinteze karboksilne kiseline, za koju se nazivala snijegom. Veliki doprinos proučavanju strukture i sastava spoja dali su J. Liebig i A. Kolbe. Godine 1875. proučavana su antiseptička i antimikotička svojstva benzojeve kiseline. Otkriće pripada njemačkom fiziologu E. L. Zalkowskom. To je omogućilo uporabu reagensa u medicini.
Tipične kemijske reakcije
Benzojeva kiselina, čija kemijska svojstva izravno ovise o prisutnosti aromatskog prstena, ulazi u reakciju elektrofilne supstitucije. Štoviše, oni su osjetljiviji na treći ugljikov atom, koji se nalazi na jednakoj udaljenosti od karboksilne skupine. Zamjena u —COOH odvija se mnogo sporije. Za C6H5COOH, iste interakcije su karakteristične kao za karboksilne kiseline. Tijekom reakcije esterifikacije (s alkoholima) esteri imaju ugodnu aromu. Kao i svi drugi organski spojevi benzojeva kiselina gori s otpuštanjem CO 2 i vode. Interakcije s bazama i metalima odvijaju se kroz karboksilnu skupinu s nastankom soli - benzoata. Dehidracija rezultira cikloalkanima. Karakteristična kemikalija reakcija (kvaliteta) na C6H5COOH je oslobađanje željezo (III) benzoata. Pojavljuje se kao žućkasto-ružičasti talog zbog interakcije benzojeve kiseline s FeCl3.
Primanje i čišćenje
Kao što je već gore opisano, benzojeva kiselina je prvi put izolirana iz rosnog tamjana. Ta prirodna smjesa je stiraksna smola. Za to je drobljena sirovina zagrijana u pješčanoj kupelji i sakupljeni su sublimirani kristali u maloj kutiji prekrivenoj papirom. Dobiveni proizvod je imao ugodnu aromu zbog prisutnosti eteričnih ulja u rosnom tamjanu - cimeta i vanilije.

Također je korištena metoda interakcije hipurne kiseline s klorovodičnom kiselinom s jakim zagrijavanjem. Prvi je dobiven isparavanjem urina biljojeda, zatim je pročišćen kristalizacijom sve dok karakteristični miris nije nestao. Ali što je s modernom sintezom takve tvari kao što je benzojeva kiselina? To je vrlo jeftino, jednostavno i ekološki. Provodi se industrijskom oksidacijom metilbenzena KMnO 4 ili djelomičnom interakcijom početnog reagensa s O2. Pročišćavanje sirovina temelji se na fizičkim svojstvima reagensa - niskoj topljivosti benzojeve kiseline u hladnoj vodi i visokoj vrućoj vodi, te se naziva rekristalizacija.
Neophodan konzervans
Kada pregledavate oznake na hrani, često se susrećete s E-kodiranim komponentama. Pod ovom oznakom su različita bojila, arome, emulgatori, konzervansi i pojačivači okusa. Benzojeva kiselina nalazi se pod kodom E210. Ovaj dodatak prehrani je prirodni konzervans koji se proizvodi u mliječnim proizvodima na prirodan način. U prirodi, spoj se može naći u različitim dijelovima biljaka, smolama, potoku dabrova. E210 se koristi u proizvodnji prehrambenih proizvoda - umaka, juha, želea, konzervirane hrane, pića. Budući da je komponenta slabo topiva u vodi, češće uzimaju soli benzojeve kiseline, na primjer, natrijev benzoat s kodom E211.

Učinak spoja na ljudsko tijelo
Konzervans E210, ulazeći u ljudsko tijelo, on reagira s proteinima, formirajući hipuričnu kiselinu, koja se izlučuje putem bubrega. Ovu komponentu odobrava Udruga WHO, ali samo u koncentraciji ne većoj od 5 mg / kg dnevnog unosa. U velikim dozama benzojeva kiselina može uzrokovati oštećenje jetre i bubrega. Osim toga, trebate se čuvati proizvoda u kojima je konzervans prisutan zajedno s vitaminom C. Interakcija ovih komponenti dovodi do stvaranja slobodnog benzena, koji je najjači kancerogen.
primjena
Benzojeva kiselina nije našla primjenu samo u prehrambenoj industriji. Koristi se u medicini kao dezinfekcijsko i antifungalno sredstvo, dodano lijekovima za iskašljavanje i masti za kožne bolesti. Reagens je sirovina za kemijsku sintezu fenola, plastifikatora i bojila. Od velike važnosti za parfumeriju su esteri benzojeve kiseline. Koriste se kao fikseri za arome. Da ne bi bili otrovani, trebate koristiti zaštitu kože i pluća, jer ulazak reagensa u tijelo dovodi do opeklina, iritacije sluznice, mučnine.