Eradikacijska terapija peptičkog ulkusa, gastritis u djece: indikacije, sheme. Terapija za iskorjenjivanje je ...
Infekcija Helicobacter pylori, koju su 1982. otkrili australski B. Marshall i R. Warren, krivac je za ulcerozne bolesti u raznim dijelovima želuca i crijeva. Za borbu protiv toga, međunarodna medicinska zajednica razvila je različite sheme eradikacijske terapije.
Opasan susjed
Trenutno nema sumnje u visok stupanj povezanosti peptičkog ulkusa s vitalnom aktivnošću Helicobacter pylori u sluznici želuca. Za liječenje se koristi kompleksna eradikacijska terapija - to su radnje usmjerene na potpuno oslobađanje od infekcije, koje smanjuju vjerojatnost recidiva ulkusa.
U godinama nakon otkrića N. pylori zabilježeno je da je ova bakterija etiološki čimbenik brojnih drugih bolesti: kroničnih antralni gastritis (tip B), atrofični gastritis (tip A), ne-srčani karcinom, MALT-limfom, idiopatska anemija nedostatka željeza, idiopatska trombocitopenijska purpura i anemija zbog nedostatka vitamina B12. Nastavlja se proučavanje odnosa spiralnih bakterija s alergijskim, respiratornim i drugim ekstragastričnim bolestima.
Eradikacijska terapija u djece
Potreba za iskorjenjivanjem infekcije H. pylori kod djece pokazala se u brojnim kliničkim studijama i njihovim meta-analizama, što je poslužilo kao osnova za sastavljanje i redovito ažuriranje međunarodnog sporazuma, što je dobro poznato gastroenterolozima kao maastrichtski konsenzus. Trenutno su pitanja dijagnoze i liječenja bolesti povezanih s Helicobacterom regulirana četvrtim maastrichtskim konsenzusom usvojenim 2010. godine.
U razvijenim zemljama Europe, Amerike i Australije, gdje su od otkrića etiološke uloge N. pylori sustavno razvijeni i primijenjeni načini dijagnosticiranja i liječenja ove infekcije, zabilježen je pad učestalosti peptičkog ulkusa i kroničnog gastritisa. Osim toga, u tim stanjima po prvi put u desetljećima postoji tendencija smanjenja učestalosti raka želuca, što također doprinosi eradikacijskoj terapiji.
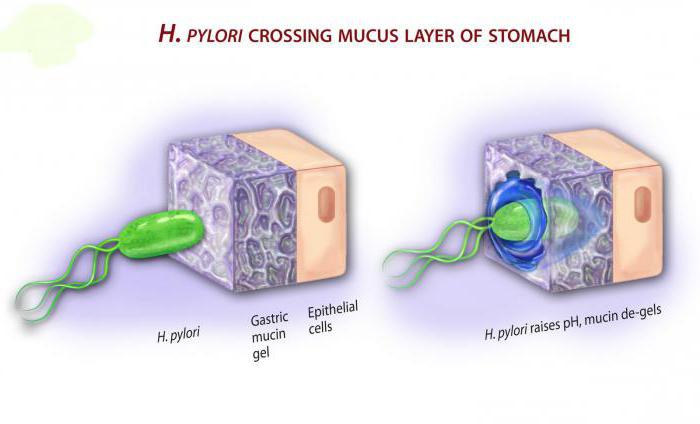
Tajanstvena bakterija
Na temelju rezultata brojnih randomiziranih placebo i komparativnih studija utvrđena je učinkovitost probiotičkih sredstava u različitim kliničkim situacijama, uključujući infekciju Helicobacter pylori kod djece. Međutim, unatoč određenom napretku u razumijevanju djelovanja probiotika na bakteriju H. pylori, njeni osjetljivi mehanizmi ostaju slabo shvaćeni.
Glavni inhibitorni i baktericidni faktor Lactobacillusa je mliječna kiselina, koju proizvode u velikim količinama. Mliječna kiselina inhibira aktivnost H. pylori ureaze i vjeruje se da vrši svoje antimikrobno djelovanje snižavanjem pH vrijednosti u prostoru lumena želuca. Međutim, utvrđeno je da mliječna kiselina koji se proizvode stanicama želučane sluznice (SOSH), potiče rast kolonije H. pylori. Osim mliječne kiseline, laktobacili i neki drugi probiotički sojevi proizvode antibakterijske peptide.
Kompleksna terapija
Koncept eradikacijske terapije temelji se na kombinaciji lijekova. IPP (inhibitori protonske pumpe) blokiraju enzim ureazu i akumulaciju energije unutar H. pylori, kao i povećavaju pH na sluznici želuca, stvarajući uvjete za djelovanje antibakterijskih lijekova. Bismutove soli, koje se gomilaju u bakterijama, ometaju enzimski sustav patogena, omogućujući dječjem imunološkom sustavu da se učinkovitije nosi s "invazijom". Konačno, najraznolikija je skupina antibakterijskih lijekova.
Eradikacijska terapija u peptičkom ulkusu kod djece (kao i kod gastritisa) često uključuje upotrebu nitroimidazola, makrolida, laktama, tetraciklina i nitrofurana. Helicobacter proizvodi otpornost na antibakterijske sastojke, što smanjuje učinkovitost eradikacijske terapije. I hitnost ovog problema raste sa svakim desetljećem.
Otpornost na antibiotike
Razvoj rezistencije na antibiotike uobičajena je karakteristika svih patogenih mikroorganizama. To je evolucijski mehanizam koji osigurava njihov opstanak u promjenjivim uvjetima. Otpornost na N. pylori podijeljena je na:
- Primarna (posljedica prethodnog liječenja).
- Sekundarna (stečena mutacija mikroorganizma, koji "potiče" eradikacijsku terapiju).
Uzroci otpora liječenju
Među glavnim razlozima za nastanak stečene rezistencije H. pylori, znanstvenici nazivaju:
- Rast recepta antibakterijskih lijekova iste skupine prema drugim indikacijama.
- Nekontrolirano uzimanje lijekova antibioticima u zemljama u kojima se prodaju bez recepta.
- Neodgovarajuća propisana eradikacijska terapija gastritisa ili čireva (propisivanje niskih doza antibiotika, smanjenje liječenja, pogrešna kombinacija u režimu lijekova).
- Neuspjeh liječničkih recepata od strane pacijenata.
- Pojava na farmaceutskim tržištima niskokvalitetnih lijekova.
Kao rezultat svega navedenog, povećanje rezistencije H. pylori smanjuje ionako ograničen broj antibiotika aktivnih protiv ovog mikroorganizma.
Problem rezistencije na antibiotike posebno je važan za djecu koja su pokazala eradikacijsku terapiju peptičkog ulkusa. Najčešće su zaraženi primarnim rezistentnim mikroorganizmima od roditelja i bliskih srodnika.
Osim toga, u pedijatrijskoj populaciji, nerazumna uporaba antibiotika za liječenje drugih bolesti, najčešće respiratornih infekcija, osobito je česta, što također doprinosi odabiru primarno rezistentnih sojeva. Kršenje načina eradikacijske terapije, kao i kod odraslih, dovodi do stvaranja sekundarne otpornosti. Razvoj otpornosti patogena također je povezan s mutacijama različitih helikobakterijskih gena.

dijagnostika
Eradikacijska terapija adolescenata počinje nakon sveobuhvatne dijagnoze. Primarna svrha ispitivanja djeteta s gastrointestinalnim simptomima je utvrditi uzrok tih simptoma, a ne samo prisutnost H. pylori. Istodobno se testiranje za otkrivanje Helicobactera ne preporučuje u djece s funkcionalnom boli u trbuhu. Možete razmotriti izvedivost ispitivanja za utvrđivanje patogena:
- pacijenti čija obiteljska anamneza ima rak želuca u odnosu na prvog stupnja;
- s vatrostalnim nedostatak željeza (ako su isključeni drugi uzroci bolesti).
Postoji nedostatak dovoljno praktičnih dokaza o uključenosti H. pylori u otitis media, VDP infekcije, parodontitis, alergije na hranu, sindrom iznenadne smrti dojenčadi, idiopatsku trombocitopenična purpura, kratkog stasa. Ali postoje sumnje.
Dijagnostički testovi
Dijagnostičkim testovima određuje se terapija uklanjanja peptičkog ulkusa i gastritisa. Metodologija testiranja ovisi o mnogim čimbenicima:
- Za dijagnozu Helicobactera pri obavljanju ezofagogastroduodenoskopije preporuča se provesti biopsiju želučanog antruma za daljnju histološku analizu.
- Preporučuje se da se početna dijagnoza H. pylori temelji na sljedećim podacima: pozitivnom histološkom pregledu i pozitivnom testu ureaze (alternativno pozitivni rezultati iz kulture).
- C-ureazni test disanja je pouzdana neinvazivna metoda za utvrđivanje je li H. pylori iskorijenjena.
- Enzimski imunotest Cala je također pouzdan neinvazivni test kako bi se utvrdilo jesu li bakterije izumrle.
- Testovi koji se temelje na otkrivanju antitijela na Helicobacterium u serumu, punoj krvi, mokraći i slini, naprotiv, nisu pouzdani.
svjedočenje
Koje su indikacije za terapiju eradikacije:
- U prisutnosti peptičkog ulkusa i infekcije Helicobacter.
- Ako nema peptičkog ulkusa, a H. pylori infekcija je otkrivena prema rezultatima istraživanja uzoraka uzetih biopsijom, iskorjenjivanje patogena nije potrebno, već je moguće.
Usput, u odnosu na djecu nije preporučljivo primjenjivati načelo "dijagnosticirati i liječiti", potreban je određeni oprez.
epidemiologija
Određivanje razine otpora u određenoj zemlji, regiji ili populaciji složen je zadatak koji zahtijeva velike materijalne i ljudske resurse. Još je teže usporediti podatke dobivene u različitim zemljama zbog razlika u metodologiji istraživanja. Na primjer, na temelju dugoročnih studija u Europi (2003.-2011.), Otpornost patogena na klaritromicin kretala se od 2 do 64% u različitim zemljama. Prema ruskim autorima, otpornost na klaritromicin varira od 5,3 do 39%.
Od lijekova koji se koriste u shemama iskorjenjivanja, amoksicilin tvori najmanju otpornost na otpornost, a Metronidazol čini najveći. Rezistencija klaritromicina na N. pylori nastavlja rasti.
Problemi korištenja "metronidazola" i "furazolidona"
Terapija eradikacije često se provodila gore navedenim preparatima. Međutim, rast prilagodljivosti bakterija na metronidazol značajno je smanjio učinkovitost režima liječenja. "Metronidazol" iz tog razloga u mnogim je zemljama danas isključen iz režima liječenja.
Alternativa metronidazolu postali su lijekovi iz serije nitrofurana, posebno "Furazolidon". Učinkovitost eradikacije na temelju toga u kombinaciji s bizmutom iznosi 86%. Međutim, "Furazolidon" je otrovan - ne koristi se u mnogim klinikama u pedijatrijskoj terapiji. Među nedostacima "Furazolidona" su hepato-neuro-i hematotoksičnost, supresija mikroflore, loša organoleptička svojstva. Da bi se postigla potrebna koncentracija aktivne tvari u tijelu, ovaj lijek se mora uzimati četiri puta dnevno. Ove osobine Furazolidona značajno smanjuju blagotvoran učinak cjelokupnog režima liječenja i, kao rezultat toga, djelotvornost eradikacije.
Droga nove generacije
Mnogi farmaceutski laboratoriji razvijaju manje toksične, ali učinkovite lijekove protiv Helicobactera. Pravi proboj bio je lijek "McMiror", koji je sadržavao nifeurerat kao aktivnu tvar. Moderna alternativa furazolidonu razvila je i sintetizirala tvrtka za istraživanje i razvoj Polichem (Italija). McMiror ima širok spektar antibakterijskih, antifungalnih i antiprotozojskih učinaka. Terapija za iskorjenjivanje djece postala je sigurnija.
Upotreba McMiror-a omogućuje poboljšanje postojećih obrazaca eradikacije Helicobactera u djece, kako bi se povećala njihova učinkovitost i sigurnost. Nifuratel je uključen u ažurirane protokole liječenja za H. pylori, pridruženi kronični gastritis, gastroduodenitis i peptički ulkus kod djece.
Upotreba lijeka "McMiror" popraćena je visokom usklađenošću, budući da se zbog polu-života od dvanaest sati može primijeniti dva puta dnevno. Upotrebljava se u djece u dobi od šest godina, dnevna doza u liječenju Giardiasis i u režimu eradikacije Helicobactera je 30 mg dnevno po kilogramu djetetove mase.
Sheme terapije eradikacije
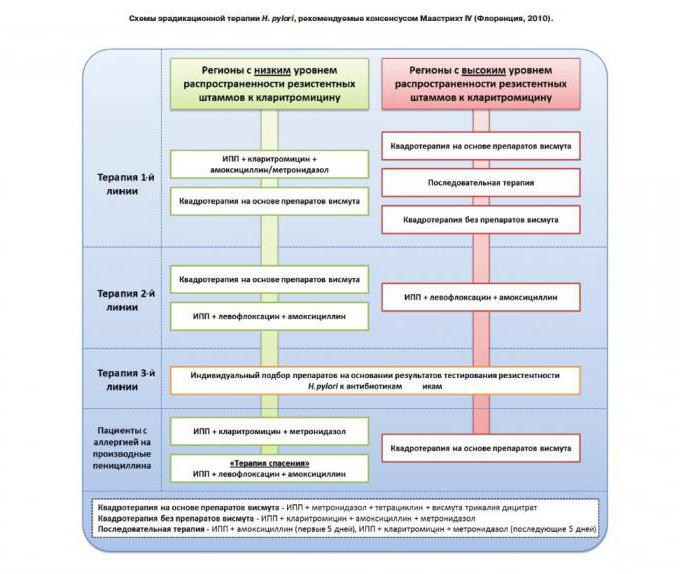
Primjeri terapije prve linije. Jednotjedni trostruki režim s pripravkom bizmuta:
- Bizmutni koloidni subcitrat (CWS) se nadopunjuje s „amoksicilinom“ („roksitromicinom“) ili „klaritromicinom” („azitromicinom”) plus „nifurerat” („furazolidon”).
- U drugoj shemi, Nifuratel je zamijenjen Famotidinom (Ranitidin), dok su ostali lijekovi isti.
Jednotjedno trostruko kolo s inhibitorima protonske pumpe:
- “Omeprazol” (“Pantoprazol”) je dopunjen amoksicilinom ili “klaritromicinom” plus “Nifuratel” (“Furazolidon”).
- Isto, ali “Nifuratel” zamjenjuje CWS.
Terapija eradikacije s četiri komponente koristi se kao tretman druge linije: CWS djeluje zajedno s omeprazolom (pantoprazol), amoksicilinom (ili klaritromicinom) i nifuratel (furazolidon).
doze
Protokoli također reguliraju doze lijekova koje treba koristiti u shemama iskorjenjivanja u djece (dnevno po kilogramu težine):
- CWS - 48 mg (maksimalno 480 mg dnevno).
- "Klaritromicin" - 7,5 mg (maksimalno 500 mg).
- "Amoksicilin" - 25 mg (najviše 1 g).
- "Roxithromycin" - 10 mg (najviše 1 g).
- "Furazolidon" - 10 mg.
- "Nifuratel" - 15 mg.
- "Omeprazol" - 0,5-0,8 mg (najviše 40 mg).
- "Pantoprazol" - 20-40 mg (isključujući težinu).
- "Ranitidin" - 2-8 mg (maksimalno 300 mg).
- "Famotidine" - 1-2 mg (maksimalno 40 mg).
Značajke liječenja
Koji tretman treba koristiti u datoj situaciji:
- Za djecu zaraženu H. pylori i obiteljsku anamnezu raka želuca u odnosu na prvog stupnja, može se propisati eradikacijska terapija.
- Preporučljivo je u različitim regijama pratiti prevalenciju sojeva Helicobactera rezistentnih na antibiotike.
- U regijama / populacijama u kojima je prevalencija Helicobacter otpornosti na "klaritromicin" visoka (> 20%), preporučuje se da se prije početka trostruke terapije pomoću "klaritromicina" odredi osjetljivost na ovaj antibiotik.
- Preporučeno trajanje trostruke terapije je 7-14 dana. Pri razmatranju ovog pitanja, trebali biste razmotriti troškove, pridržavanje liječenja i nuspojave.
- Za procjenu rezultata eradikacijske terapije preporuča se primjena pouzdanih neinvazivnih testova 4-8 tjedana nakon liječenja.
Ako ne pomogne
U slučaju neuspjeha liječenja, preporučuju se sljedeći pristupi:
- Esophagogastroduodenoscopy slijedi kultiviranje i određivanje osjetljivosti na antibiotike, uključujući alternativne, ako to nije učinjeno prije liječenja.
- Fluorescentna in situ hibridizacija (FISH) za određivanje otpornosti na "klaritromicin" korištenjem uzoraka uzetih na prvoj biopsiji i ugradnje u parafin, ako se određivanje osjetljivosti na ovaj antibiotik nije izvršilo prije tretmana.
- Modifikacija liječenja: dodati antibiotik, propisati drugi antibiotik, dodati bizmut i / ili povećati dozu i / ili povećati trajanje terapije.
zaključak
Eradikacijska terapija je djelotvoran (ponekad jedini) lijek za najopasnije bakterije Helicobacter pylori, koje mogu izazvati čireve, gastritis, kolitis i druge gastrointestinalne bolesti.
