Ugljikovodici su spojevi ugljika s vodikom koji ne sadrže druge elemente. Razvrstavanje ugljikovodika
Što su ugljikovodici? Kako su klasificirani? Koje značajke imaju? Pokušajmo zajedno pronaći odgovore na pitanja.
Ugljikovodici su organski spojevi koji sadrže vodik i ugljik. Smatraju se organskim spojevima u osnovnoj kemiji.
klasifikacija
Ovisno o stanju veze između ugljika glavnog lanca, uobičajeno je podijeliti sve C x H y na nekoliko tipova. Jednaki ugljični spojevi s vodikom su karakteristični za zasićene ugljikovodike.
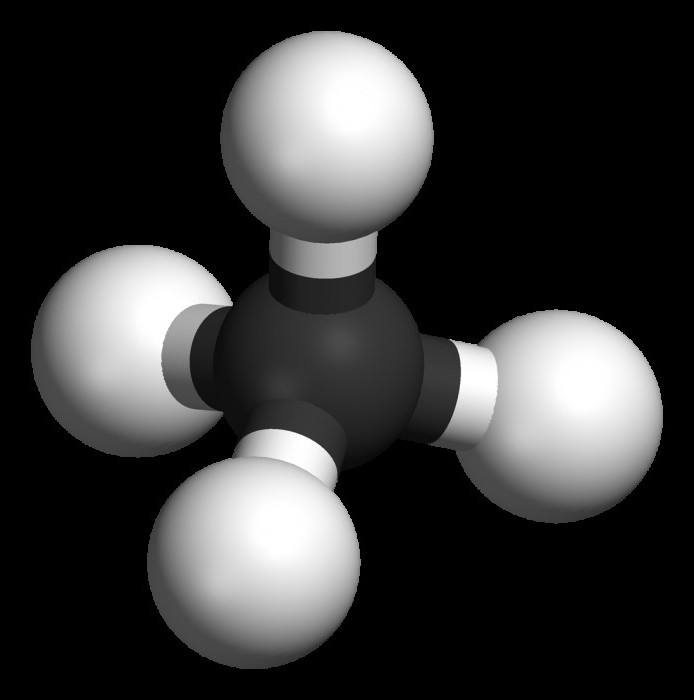
alkani
Granični ugljikovodici su spojevi opće formule CnH2n + 2 . Među njihovim obilježjima možemo spomenuti odsustvo zatvorene strukture, kao i pojedinačne (jednostavne) veze. U organskoj kemiji se nazivaju acikličkim spojevima.
Tipičan predstavnik ove klase je metan - CH4. On je taj koji započinje homolognu seriju alkana, posjeduje sva svojstva koja su svojstvena drugim predstavnicima parafina.
Prvi predstavnici ove klase ugljikovodika su plinovite tvari s niskom topljivošću u vodi, specifičnim mirisom.
Među osnovnim kemijskim svojstvima predstavnika homolognih nizova alkana izdvajamo radikalnu supstituciju.
Halogeniranje se događa na povišenim temperaturama ili u prisutnosti ultraljubičastog zračenja. Reakcija se odvija u nekoliko faza, karakteriziranih postupnom zamjenom atoma vodika s halogenom. Svojstva ugljikovodika određenog broja metana objašnjavaju se zasićenjem veze između ugljikovih atoma. Oni nisu sposobni za ulazak u reakcije dodavanja, dok dobro izgaraju u kisiku iz zraka, stvarajući ugljični dioksid, vodenu paru i oslobađajući dovoljno toplinske energije.
Među glavnim granama primjene predstavnika ove klase ugljikovodika izdvajamo uporabu kao gorivo, kao i opciju sirovina za proizvodnju mnogih drugih organskih spojeva.
alkeni
Nezasićeni ugljikovodici su spojevi koji imaju jednu ili više višestrukih (nezasićenih) veza između ugljikovih atoma. Alkeni imaju opću formulu CnH2n . Tipičan predstavnik ove klase je etilen.
Ovi prirodni ugljikovodici dio su ulja. S obzirom da molekula sadrži dvostruku vezu, reakcije adicije su karakteristične za alkene. Na primjer, mogu ući u halogenaciju, hidrataciju.
Ako je dvostruka veza smještena u prvom položaju, na primjer, u butenu-1, dodavanje vodikovog halida i hidratacije (reakcija s vodom) se odvija prema Markovnikovom pravilu. Njezina se suština sastoji u činjenici da je tijekom hidrohalogeniranja i hidratacije vodik vezan za ugljikov atom koji je s njim maksimalno zasićen.
Hidroksilna skupina ili atom halogena vezana je na C atom koji nije zasićen vodikom. Kvalitativna reakcija na nezasićenoj (dvostrukoj) vezi je izbjeljivanje bromove vode ili. t kalijev permanganat.

cikloalkane
Takvi ugljikovodici su ciklički spojevi koji su interklasni izomeri za alkenes. Oni imaju opću formulu C n H 2n , jednostruke veze. S obzirom da se ova klasa odlikuje zatvorenom strukturom, one ulaze u reakcije adicije, praćene uništenjem zatvorenog ciklusa, pretvarajući se u zasićene alkane. Glavni izvori takvih spojeva su prirodni i povezani plin, nafta. Unatoč cikličkoj strukturi, u sp3 hibridizacijskim molekulama, valentni kut je 109 ° 28 '.
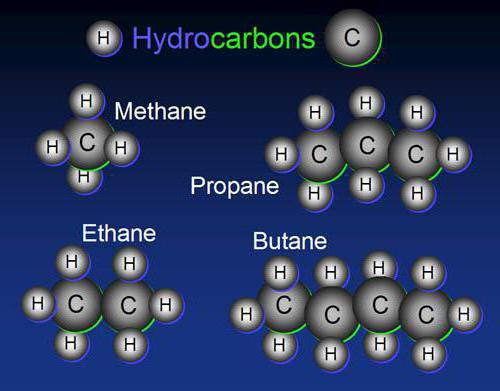
Alkadicncs
Što još karakterizira organska kemija? Ugljikovodici ove klase imaju opću formulu CpH2n-2 . Svi predstavnici dienskih ugljikovodika imaju dvije dvostruke veze. Nezasićenost diena određuje njihova osnovna kemijska svojstva. Analogno alkenima, dienski spojevi ulaze u reakciju adicije.
Kao oni kemijske reakcije koje su karakteristične za ove spojeve, uočavamo polimerizaciju. Početni monomer u postupku je predstavnik diena, a produkt interakcije je sintetička guma. Kada se sumpor doda dobivenom polimeru, javlja se vulkanizacija, praćena stvaranjem gume.
alkini
Za ove nezasićene organske spojeve karakterizirane općom formulom CnH2n-2 , može se uočiti prisutnost trostruke veze između ugljikovih atoma. Ako se nalazi iza prvog ugljikovog atoma, kvalitativna reakcija na njegovu prisutnost je zamjena sa složenim srebrom.
Kao i za alkene, diene, alkini se lako pridružuju trostrukoj vezi. Odlikuju se hidrogenacijom, hidrohalogenacijom, halogeniranjem, reakcijama hidratacije.

Aromatski spojevi
Benzen je prvi predstavnik ove klase. Ima opću formulu CnH 2n-6 . Za razliku od svih drugih ugljikovodika, ovaj spoj ima aromatski prsten. Slobodni elektroni svakog ugljikovog atoma sudjeluju u njegovom oblikovanju. Tri elektrona C formiraju hibridne oblake, a četvrti elektron se ne podvrgava hibridizaciji. Ona tvori aromatski prsten, koji je ravnomjerno raspoređen po molekuli. Ujednačena raspodjela prstena strukturom objašnjava njezinu kemijsku stabilnost. Benzen sam ulazi u zamjenu i dodavanje samo u otežanim uvjetima.
Toluen, koji je njegov homolog, karakterizira određeni pomak u gustoći elektrona, stoga ima veću sposobnost supstitucije. Ugljikovodični radikal je orijentir tipa 1, dolazeći supstituenti (halogen, nitro skupina) zauzimaju orto, para pozicije.
zaključak
Bez obzira na to koje su strukture u strukturi različiti predstavnici ugljikovodika, oni imaju određeni broj ugljikovih atoma i vodika u svom sastavu. Postoji određena tendencija promjene fizičkih svojstava C x H y predstavnika. Prvi predstavnici bilo koje klase imaju plinovito stanje, kako se relativna molekularna težina povećava, opaža se sustavni prijelaz u tekućini, zatim u čvrstom obliku.