Vodikova elektroda: definicija, uređaj, formula i svojstva
U tekstu koji slijedi definiramo značenje pojma "vodikova elektroda". Ne znaju svi što je to. Ovdje će se otkriti njegovo opće značenje. Također ćemo obratiti pozornost na reakcije oksidacije i redukcije, koje su povezane s vrstom rada sličnog objekta, a posebno ćemo govoriti o dijelovima koji ga tvore.
uvod
Standardna vodikova elektroda koja se zove referentna elektroda. Koriste se tijekom mjerenja elektrokemijske prirode. Također su pronašli njihovu uporabu u sastavu galvanskih stanica. Vodikova elektroda (EI) je metalna ploča ili žica koja apsorbira vodik u plinovitom obliku. Ploča je sama uronjena u vodene otopine zasićene s kisikom i sadrži njegove ione.

Ovaj element ima potencijal zbog koncentracije iona H + u debljini otopine. Elektroda se koristi kao referenca prema kojoj se određuje potencijal ispitivanih kemijskih reakcija. Ako je tlak vodika jednak jednoj jedinici atm., A koncentracija protona odgovara omjeru 1 mol / l, tada se potencijal VE smatra jednakim nuli. Ako koristite platinu kao površinu za određenu reakciju, kao i VE i definiranu elektrodu, tada možete promatrati zanimljivu reakciju tijekom koje se formira stabilni atom vodika:
2H + + 2e - = H2.
Drugim riječima, H atomi su reducirani ili oksidirani, a tip reakcije određen je potencijalom vodikove elektrode na kojoj se odvija reakcija.
Prilikom mjerenja EMF uređaja za galvanizaciju primjenom standardnih uvjeta (rješenja o kojima smo gore govorili), uvijek se koristi pojam standardnog elektrodnog potencijala. To je određeno vrsta kemijske reakcije.
Oksidacija i redukcija
Govoreći o vodikovim elektrodama, spomenuli smo pojam oksidacijske i redukcijske reakcije, koji se može dogoditi s atomima vodika pri korištenju odgovarajućih elektroda.
Oporavak u kemiji je fenomen u kojem:
- Atomska, ionska čestica ili molekula prihvaća (svaki) jedan ili više elektrona.
- Opaženo je smanjenje stupnja oksidacije pojedinih atoma u određenoj čestici.
- Organske tvari gube atome kisika i / ili dobivaju vodik.
Prije toga, samo se treća definicija smatrala restauracijom (od sredine devetnaestog stoljeća), dok se prva i druga počela primjenjivati tek dvadesetih godina prošlog stoljeća. Danas se vjeruje da se druga definicija može smatrati zajedničkom svim procesima redukcije u kemiji. Uz pomoć trećeg tipa opisa, redoks reakcije su često izolirane i prepoznate.

Razmotrite više. Pod oksidacijom se misli na proces koji je popraćen postepenim povećanjem atomske snage oksidacijska stanja određene tvari. To se događa putem "transporta" elektrona iz donornog atoma, koji je odgovoran za povratak e - , u akceptorni atom, koji će primiti e - .
Uvođenje pojma u znanstvenu i svakodnevnu cirkulaciju jezičnih jedinica obvezno je akademiku V. M. Severginu. Ta je inovacija nastala na prijelazu iz XVII. U XIX. Znanstvenik je koristio ovaj pojam za procese interakcije kisika (sadržanog u zraku) s drugim tvarima. Ponekad oksidacijske reakcije mogu dovesti do stvaranja nestabilnih čestica i njihovog naknadnog razlaganja na manje sastavne dijelove reakcije.
primjena
Za mjerenje standardnog elektrokemijskog potencijala najčešće se koriste vodikove elektrode. Također se koristi za određivanje razine koncentracije vodikovih iona i drugih vrsta iona. Čak i uz primjenu VE provodimo istraživanja koja pomažu znati produkt topljivosti u odnosu na navedenu konstantu brzine tijekom nekih elektrokemijskih reakcija.
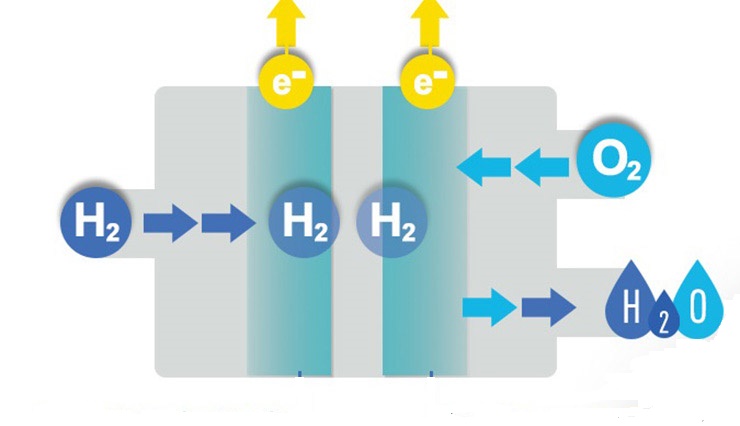
Najvažniji zahtjevi za referentnu elektrodu su:
- Sposobnost rada u temperaturnom rasponu.
- Stabilnost tijeka rada.
- Sposobnost reproduciranja rezultata reakcije i istraživanja.
- Kompatibilnost s istraživanom talinom.
- Nedostatak stacionarnog potencijala.
Mehanizam uređaja
Uređaj standardnih vodikovih elektroda uključuje:
- Platinska elektroda je element sustava koji ima sposobnost isključivanja kontaminacije otopine vanjskim nizom iona tijekom elektrolize. Takvi dijelovi nemaju čistu površinu (isključujući relativno uska potencijalna područja). Područje reakcije tvari naziva se dvoslojni. Karakterizira ga činjenica da su ovdje samo metal, ioni i otapala. A potonji je u posebnom stanju. Ovisno o vrijednosti potencijala, metal može biti obložen vodikom u apsorbiranom obliku (niska vrijednost) ili s oksidima (visoka vrijednost).
- Elektrolitički most je sredstvo za komuniciranje dvije polovice galvanske strukture mehanizma.
- Napajanje vodikovim plinom.
- Kisele otopine (obično HCl) s koncentracijom kationa vodika: H + = 1 mol / l.
- Opstrukcija prodiranja molekula kisika (iz zraka) zatvarača.

potencijal
Za izračunavanje potencijala vodikove elektrode pri nanošenju na jednu elektrodu nije moguće. Međutim, ova tvrdnja vrijedi samo za eksperimentalne načine.
Potenciometrijska sredstva, koja igraju važnu ulogu u pitanju potencijala elektroda, temelje se na definiciji elektromotorne sile (EMF):
E = E 1 -E 2 ;
Gdje je E definirana EMF, i E1 i E2 djeluju kao potencijal elektroda kruga koji se istražuje.
Kako izračunati? Potencijal vodikove elektrode jednak je broju koji se može odrediti pomoću Nernstove jednadžbe:
E = E 0 + RT / Nf u vol / a crvenoj = E 0 + RT / nF u [vol] y vol / [crvenom] y crvenom
gdje je:
- E 0 - standardna vrijednost potencijala redoks sustava;
- R je plinska konstanta jednaka 8,312 J / (K mol);
- T je apsolutna vrijednost temperature;
- F je Faradayova konstanta (96485Cl / mol);
- n je broj elektrona koji su sudionici u reakciji;
- vol i crveni su pokazatelji aktivnosti različitih oblika redoks sustava (oksidacija i redukcija);
- [ox] i [red] - molarna koncentracija tvari odgovornih za pojavu oksidacije ili redukcije;
- Gamma [ox] i [red] - veličina koeficijenta aktivnosti.

Povijesni podaci
CE karakterizira složenost procesa rada. Međutim, postalo je poznato i počelo se dugo koristiti.
VE je vlasnički dizajn P. P. L. Serensena. Koristio ih je kao središnji alat za svoja istraživanja, što je omogućilo pojavu moderne teorije pH-tvari.
JF McClendon koristio je HE u brojnim prvim pokusima na proučavanju pH-metrije unutar želuca. Kako se to dogodilo? Znanstvenik je koristio referentnu elektrodu u kojoj je postavljena vodikova elektroda. Potonji je uveden zajedno s pH sondom unutar ljudskog želuca.