Dušična kiselina: svojstva, priprema i uporaba
uvod
 Zainteresirani ste za cvjećarstvo i došli ste u dućan kupiti gnojivo za svoje cvijeće. Pregledavši različita imena i skladbe, primijetili ste bocu s natpisom "Dušikovo gnojivo". Čitamo njegov sastav: "Fosfor, kalcij, to-to ... Dušična kiselina? I što je to zvijer ?!". Obično se u takvoj situaciji upozna s dušičnom kiselinom. I mnogi od njih žele znati više o tome. Danas ću pokušati zadovoljiti vašu znatiželju.
Zainteresirani ste za cvjećarstvo i došli ste u dućan kupiti gnojivo za svoje cvijeće. Pregledavši različita imena i skladbe, primijetili ste bocu s natpisom "Dušikovo gnojivo". Čitamo njegov sastav: "Fosfor, kalcij, to-to ... Dušična kiselina? I što je to zvijer ?!". Obično se u takvoj situaciji upozna s dušičnom kiselinom. I mnogi od njih žele znati više o tome. Danas ću pokušati zadovoljiti vašu znatiželju.
definicija
Dušična kiselina (formula HNO 3 ) je jaka monobazična kiselina. U neoksidiranom stanju izgleda kao na fotografiji 1. Pod normalnim uvjetima je tekućina, ali se može pretvoriti u čvrsto agregatno stanje. I u njemu podsjeća na kristale s monoklinskom ili rombičkom rešetkom.
Kemijska svojstva dušične kiseline
 Ima sposobnost da se dobro miješa s vodom, gdje dolazi do gotovo potpune disocijacije ove kiseline u ione. Koncentrirana dušična kiselina ima smeđu boju (na slici). On se postiže razgradnjom u dušikov dioksid, vodu i kisik, što je posljedica sunčeve svjetlosti koja pada na njega. Ako se zagrije, doći će do iste razgradnje. Svi metali reagiraju s njom, osim tantala, zlata i platinoida (rutenij, rodij, paladij, iridij, osmij i platina). Međutim, njegova povezanost s klorovodična kiselina može čak i rastopiti neke od njih (to je takozvana "kraljevska votka"). Dušična kiselina, koja ima bilo koju koncentraciju, može se manifestirati kao oksidacijsko sredstvo. mnogo organska tvar u interakciji s njim može se spontano zapaliti. I neki će metali u ovoj kiselini biti pasivizirani. Kada su izloženi njima (kao i pri reakciji s oksidima, karbonatima i hidroksidima), dušična kiselina tvori njezine soli, nazvane nitrati. Potonji se dobro otope u vodi. Ali nitratni ioni u njemu se ne hidroliziraju. Ako se soli dane kiseline zagrijavaju, one će se nepovratno razgraditi.
Ima sposobnost da se dobro miješa s vodom, gdje dolazi do gotovo potpune disocijacije ove kiseline u ione. Koncentrirana dušična kiselina ima smeđu boju (na slici). On se postiže razgradnjom u dušikov dioksid, vodu i kisik, što je posljedica sunčeve svjetlosti koja pada na njega. Ako se zagrije, doći će do iste razgradnje. Svi metali reagiraju s njom, osim tantala, zlata i platinoida (rutenij, rodij, paladij, iridij, osmij i platina). Međutim, njegova povezanost s klorovodična kiselina može čak i rastopiti neke od njih (to je takozvana "kraljevska votka"). Dušična kiselina, koja ima bilo koju koncentraciju, može se manifestirati kao oksidacijsko sredstvo. mnogo organska tvar u interakciji s njim može se spontano zapaliti. I neki će metali u ovoj kiselini biti pasivizirani. Kada su izloženi njima (kao i pri reakciji s oksidima, karbonatima i hidroksidima), dušična kiselina tvori njezine soli, nazvane nitrati. Potonji se dobro otope u vodi. Ali nitratni ioni u njemu se ne hidroliziraju. Ako se soli dane kiseline zagrijavaju, one će se nepovratno razgraditi.
recepcija
Za dobivanje dušične kiseline, sintetički amonijak oksidira se pomoću katalizatora platine i rodija dok se ne pojavi mješavina dušičnih plinova, koji se zatim apsorbiraju u vodi. Također se stvara kada se miješa i zagrijava. kalijev nitrat i željeznog vitriola. 
primjena
Uz pomoć dušične kiseline proizvode mineralna gnojiva, eksplozive i neke otrovne tvari. Urezala je otisnute oblike (pločice za jetkanje, magnezijeve klišee, itd.), Kao i zakiseljena rješenja za toniranje fotografija. Boje i lijekovi proizvode se iz dušične kiseline, a koriste se i za određivanje prisutnosti zlata u legurama zlata.
Fiziološki učinak
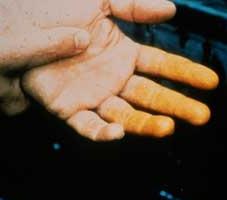
S obzirom na stupanj utjecaja dušične kiseline na tijelo, odnosi se na 3. stupanj opasnosti (umjereno opasan). Udisanje pare dovodi do iritacije respiratornog trakta. Kada se nanese na kožu, dušična kiselina ostavlja mnoge dugotrajne čireve. Područja kože na kojima je postala postala karakteristična žuta boja (fotografija). Znanstveno gledano, dolazi do reakcije ksantoproteina. Dušikov dioksid, koji nastaje zagrijavanjem dušične kiseline ili raspadanjem na svjetlu, vrlo je otrovan i može uzrokovati plućni edem.
zaključak
Dušična kiselina koristi osobi u razrijeđenom i čistom stanju. No, najčešće se nalazi u sastavu tvari, od kojih mnogi vjerojatno znate (na primjer, nitroglicerin).