Fizikalna svojstva sumporovodika i njegova primjena
Među svim kemijskim spojevima poznatim u suvremenom svijetu, postoji nekoliko koji se mogu razlikovati, možda čak i najneobrazovaniji znaju za njihovo postojanje. Zašto su ti elementi i spojevi toliko popularni? Jednostavno je - nalaze se posvuda. Ovi spojevi uključuju vodikov sulfid.
O vezi
Analiza bilo kojeg spoja započinje proučavanjem njegove strukture. Struktura određuje fizikalna i kemijska svojstva sumporovodika. Molekula ove tvari sadrži samo 3 atoma: 2 vodika i 1 sumpor. Komponente vezanja kovalentne polarne veze, zbog nemetalne prirode spoja. Struktura molekule odnosi se na kut, što su znanstvenici dokazali nakon kratkog istraživanja. Kut je 92 stupnja, što se malo razlikuje od strukture molekule vode.

Fizička svojstva
Svaka osoba, analizirajući novu tvar za sebe, najprije skreće pozornost na svoje fizičke osobine: fizičko stanje, boju, miris i tako dalje. Možda bi trebao početi s mirisom sumporovodika, poznat je svima - pokvarenim jajima. Naravno, nitko ga ne može nazvati ugodnim. Koja su fizikalna svojstva sumporovodika, unatoč njegovoj prevalenciji, poznata su samo onima koji rade s njim ili marljivo pohađaju školu. Pod standardnim uvjetima, tvar ima plinovitu strukturu. To bi bio veliki propust da se opišu fizikalna svojstva sumporovodika, a da ne spominjemo promjenu njegovih svojstava na temperaturama iznad 20 stupnjeva Celzija, jer je pod tim uvjetima moguće potpuno otapanje sumporovodika s vodom. Voda koja sadrži ovaj spoj ima blago kiselinska svojstva, disocijacija ima postupnu prirodu.

Za osobu je tvar prilično opasna - to je vrsta otrova, čak iu malim količinama. Desetina posto plina sumporovodika može dovesti do paralize ljudskog respiratornog trakta, što je fatalno za 8 minuta (to je vrijeme kada mozak može živjeti bez novog kisika).
Toksična svojstva sumporovodika primjenjuju se na sva stvorenja čija krv sadrži hemoglobin. Željezo, sadržano u velikim količinama u crvenim krvnim zrncima, vrlo lako reagira s molekulama sumporovodika u obliku sulfida, koji ne može nositi kisik.
Antidot za sumporovodik je vrlo jednostavan - samo trebate udahnuti zrak, zasićen kisikom i imati malu mješavinu klora, koji neutralizira djelovanje sumpora. Pokuse i istraživanja vezana za sumporovodik treba provoditi pod posebnim uvjetima.
Proizvodnja vodikovog sulfida
Reakcija dobivanja vodikovog sulfida najčešće se provodi u prisutnosti zatvorene dimne cijevi koja minimizira mogućnost trovanja znanstvenika. U ovoj reakciji, čisti vodik i sumpor međusobno djeluju, ne ostavljajući zaostale proizvode.

Proizvodnja vodikovog sulfida
U školama se sumporovodik češće koristi za stjecanje iskustva koje nije povezano s rizikom za zdravlje učenika. Reakcija se izvodi pomoću željeznog (II) sulfida i otopine jedne od kiselina, sumporne ili klorovodične. Da biste postigli zajamčeni rezultat, trebat će vam par komada sulfida veličine običnog graška. Sljedeći korak će biti punjenje epruvete otopinom kiseline do polovice, zatim cijev mora biti zatvorena. cijev za izlaz plina stavite ispod haube i zagrijte. Ako se reakcija nastavi, ispuštaju se mali mjehurići plina. Ovaj postupak dobivanja vodikovog sulfida djelotvoran je samo za proizvodnju male količine plina.
Tvar se također može dobiti uporabom metalnog željeza i kristalnog sumpora. Rezultirajući sulfid tijekom reakcije, za potpuno stjecanje fizikalnih svojstava sumporovodika, mora se pomiješati sa sumpornom kiselinom.
Kemijska svojstva
Vodikov sulfid reagira s kisikom, plamen dobiva plavu nijansu pri spaljivanju sumporovodika. Kod potpunog sagorijevanja nastaje proizvod sumporni oksid i vode. Nastali oksid je topljiv u vodi, a otopina dobiva slaba kiselinska svojstva. Pokazatelj tog procesa je lakmus papir koji je obojen kontaktom s tvari u plavoj boji. Stoga je uobičajeno primati sumpor u industrijskom mjerilu.
Pri interakciji s halogenima i solima pojavljuju se dovoljno jaka redukcijska svojstva tvari koja se odnose na kemijska i fizikalna svojstva. U laboratorijskim uvjetima za provođenje pokusa i praćenje reakcije interakcije vodikovog sulfida s halogenima koriste se brom i klor. Produkt ove reakcije bit će kristalni sumpor.
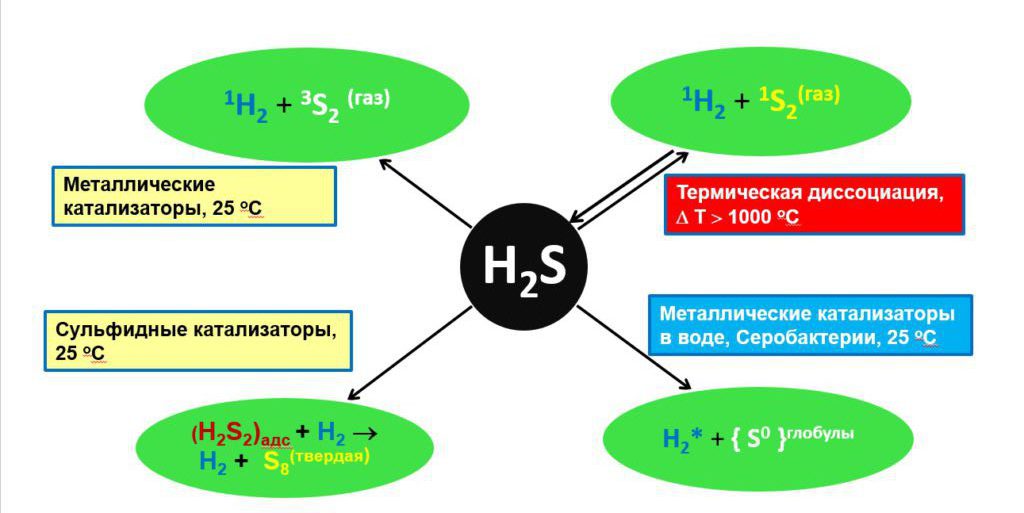
Reakcija vode i sumporovodika dovodi do stvaranja hidroksidnog kationa. Osim toga, spoj ima sposobnost stvaranja drugih tvari - sulfida i hidrosulfida. Spojevi zemno alkalijskih i alkalnih metala reagiraju s vodikovim sulfidom u obliku bezbojnih tvari, dok u isto vrijeme reakcija s teškim metalima izaziva pojavu crne tvari.
primjena
Sumpor - otkrivena je jedna od prvih tvari čije se svojstvo zapali. Supstanca se, između ostalog, dodaje običnom prirodnom plinu, koji se nalazi u svakoj kuhinji. Fizikalna svojstva sumporovodika i njegova uporaba prilično su opsežna, zbog čega su mnogi čuli za tu tvar. Vodikov sulfid je prethodno korišten kao otrov za insekte i štetočine, ali je uklonjen iz proizvodnje zbog mnogih slučajeva trovanja ljudi. Zbog toksičnosti spoja, s njime treba postupati s najvećom pažnjom.

U prirodi, supstanca se javlja vrlo često. To je rezultat truleži proizvoda raznih životinja, a plin se često nalazi u otopljenom obliku u prirodnim vodama. Vrlo je teško opisati sva fizikalna svojstva sumporovodika, jer ih je mnogo. Glavni su opisani gore. Upotreba sumporovodika u industriji također je vrlo opsežna. neki kemijski eksperimenti industrijski procesi zahtijevaju njegovu prisutnost.