Proizvodnja alkohola, primjena, svojstva. Postupci za proizvodnju alkohola
Alkoholi su česti u prirodi. Većina ljudi je upoznata etil alkohol (etanol) je aktivni sastojak alkoholnih pića, ali je samo jedan od obitelji organskih spojeva poznatih kao alkoholi. Njihovo dobivanje, prije svega etil (vino kao rezultat enzimske fermentacije soka od grožđa, bio je jedan od prvih kemijskih procesa koje je čovječanstvo savladalo.
Nomenklatura alkohola
Alkoholi predstavljaju organski spojevi hidroksilna (OH) funkcionalna skupina s alifatskim ugljikovim atomom. Kako je OH član molekula svih alkohola, oni su često predstavljeni kao derivati vode s općom formulom ROH, gdje R označava alkilnu skupinu.
Proizvodnja metanolskih alkohola (CH3OH) i etanola (CH3CH2OH), koja su prva dva člana njihovih homolognih serija, važan je zadatak kemijske industrije u mnogim zemljama. Kada sadrže od jednog do četiri ugljikova atoma, oni se često nazivaju zajedničkim imenima, u kojima iza imena alkilne skupine slijedi riječ alkohol: 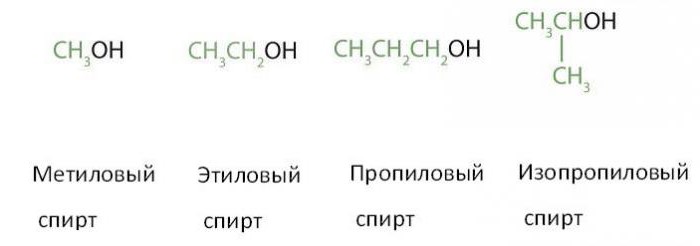
Može se vidjeti da sva četiri (posljednja dva su izomera jedne tvari) gore navedene molekule alkohola sadrže jednu hidroksilnu skupinu. Na temelju toga svi oni pripadaju klasi monohidričnih alkohola (postoje i dvije, tri, četiri i poliatomske). Osim toga, sve su to derivati zasićenih ugljikovodika iz niza alkana: metan, etan, propan (imena alkohola dobivaju se dodavanjem naziva alkena završetku "-ol"). Stoga ih nazivaju i marginalnim monohidričnim alkoholima.
Monohidrični alkoholi
Proizvodnja, svojstva (fizikalna i kemijska) ovih spojeva ovise o broju ugljikovih atoma vezanih za njegov atom, izravno vezanim za OH skupinu. Prema tome, monohidrični alkoholi mogu se na temelju toga grupirati u tri klase.
- Primarni alkoholi imaju molekulu u kojoj je jedan ugljikov atom vezan za OH skupinu vezan za drugi atom C. Njihova opća formula je RCH2OH. Na primjer, etanol je primarni alkohol.
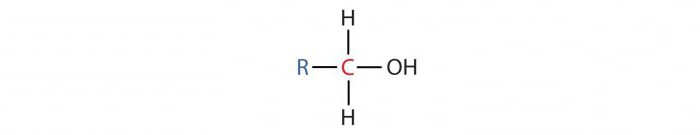
- Sekundarni alkoholi imaju u molekuli jedan ugljikov atom s OH skupinom vezanom za dva druga C atoma, a njihova opća formula je R2CHOH. Oni uključuju propil i izopropil alkohole.
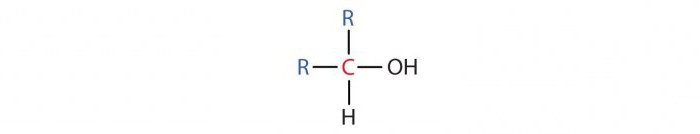
- Tercijarni alkoholi sadrže u molekuli ugljikov atom s OH skupinom vezanom za tri druga C-atoma, a njihova opća formula je R3COH.

Dobivanje monohidričnih alkohola u industriji je moguće na više načina, o čemu će biti riječi u nastavku.
Metanol kao proizvod prirodnog plina
Metanol se dobiva miješanjem plina vodika i ugljičnog monoksida pri visokim temperaturama i tlakovima (200 do 350 ° C). u prisutnosti katalizatora koji se sastoji od cinkov oksid (ZnO) i kromov oksid (Cr203) kao katalizator: 2H2 + CO → CH3OH. 
U ovom slučaju, sirovina za proizvodnju reagensa je prirodni plin i vodena para, pri čemu se miješa sintetski plin, koji je smjesa CO i H2.
Metanol je važno otapalo i koristi se kao gorivo za automobile, bilo kao čista tekućina - u nekim trkaćim automobilima, ili kao visoko oktanski dodatak benzinu. Proizvodnja i uporaba alkohola u svijetu, a posebno metanola, mjeri se u milijunima tona. Krajem 2013. u svijetu je potrošeno 66 milijuna tona metanola, od čega 65% u Aziji, 17% u Europi i 11% u SAD-u.
Dobivanje konačnih alkohola iz alkena
Mnogi jednostavni težinski alkoholi industrijske važnosti proizvode se hidratacijom (dodavanjem vode) alkena (etilen, propilen, buten). Ovim postupkom dobiva se etanol, izopropanol, butanol (sekundarni i tercijarni).
Poznati izravni i neizravni postupci proizvodnje alkohola hidratacijom. Izravno vam omogućuje da izbjegnete stvaranje stabilnih intermedijarnih proizvoda, obično uz pomoć kiselih katalizatora.
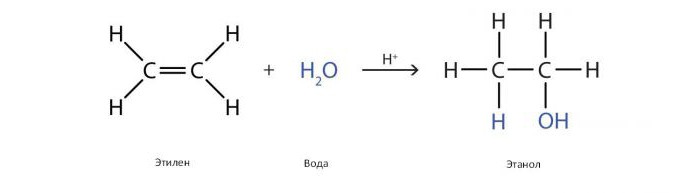
Katalizator je obično fosforna kiselina, adsorbirani na poroznom nosaču kao što je silikagel ili kieselguhr. Ovaj katalizator je prvi put korišten za proizvodnju etanola velikih razmjera u Sjedinjenim Državama od strane Shell-a 1947. Reakcija se provodi u prisutnosti pare pod visokim tlakom na 300 ° C, pri čemu se između etilena i pare održava omjer 1,0: 0,6.
Slična reakcija na proizvodnju izopropil alkohola s katalizatorima u obliku sumporna kiselina izgleda ovako 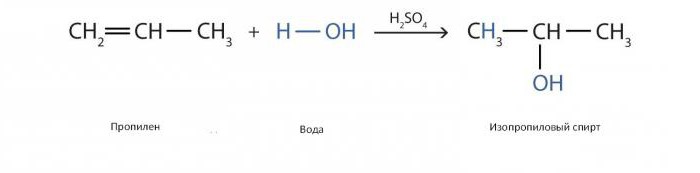
Indirektna metoda hidratacije etilena
Na indirektan način, u praksi prvi put primijenjeni u industrijskom mjerilu 1930., ali danas smatrani gotovo potpuno zastarjelim, reakcija za proizvodnju alkohola je pretvaranje alkena u sulfatne estere, koji se zatim hidroliziraju. Tradicionalno, alken se tretira sa sumpornom kiselinom da bi se proizveli alkilni sulfatni esteri. U slučaju proizvodnje etanola, ovaj korak se može napisati na sljedeći način: H2SO4 + C2H4 → C2H5-O-SO3H
Zatim se taj sulfatni ester hidrolizira dok se ne regenerira sumporna kiselina i oslobodi se etanol: C2H5-O-S03H + H20 → H2S04 + C2H5OH.
Metode za proizvodnju alkohola izuzetno su raznolike, ali dolje opisani postupak vjerojatno je poznat, barem po glasinama, svakom čitatelju.
Fermentacija alkohola
To je biološki proces u kojem se molekule, kao što su glukoza, fruktoza i saharoza, pretvaraju u staničnu energiju uz paralelnu proizvodnju etanola i ugljičnog dioksida kao proizvoda metabolizma. Fermentacija je katalizirana enzimima sadržanim u kvascu i odvija se kroz složeni višestupanjski mehanizam, koji općenito uključuje pretvorbu (u prvoj fazi) škroba sadržanog u biljnim zrncima u glukozu, nakon čega slijedi proizvodnja etanola iz njega. Budući da kvasac provodi ovu transformaciju u odsutnosti kisika, alkoholna fermentacija se smatra anaerobnim procesom.
Reakcije fermentacije alkohola mogu se prikazati kako slijedi: 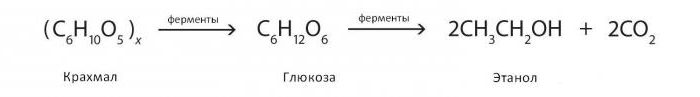
Načini kupnje alkoholnih pića
Sav etanol sadržan u alkoholnim pićima proizvodi se fermentacijom uzrokovanom kvascem.
Vino se dobiva fermentacijom prirodnih šećera prisutnih u grožđu; Jabukovača dobiva se analognom fermentacijom prirodnog šećera u jabukama odnosno kruškama; i druga voćna vina proizvode se fermentacijom šećera u bilo kojoj drugoj vrsti voća. Rakije i rakije (npr. Šljivovica) proizvode se destilacijom pića dobivenih fermentacijom voćnih šećera.
Medeni napitci se dobivaju fermentacijom iz prirodnih šećera prisutnih u medu. 
Pivo, viski i votka proizvode se fermentacijom zrna škroba, koji se pretvaraju u šećer djelovanjem enzima amilaze, koji je prisutan u zrnu jezgre koja je prošla klijanje. U smjesu se mogu dodati i drugi izvori škroba (na primjer, krumpir i zrna bez malta), budući da će amilaza djelovati i na njihov škrob.
Rižina vina (uključujući i sake) proizvode se fermentacijom žitnog škroba, pretvorenog u šećer Asugi Aspergillus ogugae.
Rum i neka druga pića dobivaju se fermentacijom i destilacijom šećerne trske. Rum se obično proizvodi od proizvoda šećerne trske - melase.
U svakom slučaju, fermentacija se mora odvijati u posudi koja omogućuje izlazak ugljičnog dioksida, ali sprečava ulazak vanjskog zraka. To je nužno jer učinak kisika sprječava stvaranje etanola, a nakupljanje ugljičnog dioksida stvara rizik od pucanja posude. 
Reakcija nukleofilne supstitucije
Alkoholi se proizvode u laboratorijima metodama koje koriste kemijske tvari raznih razreda, od ugljikovodika do karbonilnih spojeva, kao polazne proizvode za reakcije. Postoji nekoliko načina koji se svodi na nekoliko osnovnih reakcija.
Primarni halogenoalkani reagiraju s vodenim otopinama alkalnih NaOH ili KOH, formirajući, uglavnom, primarne alkohole u reakciji nukleofilne alifatske supstitucije. Kada, na primjer, metil bromid reagira s otopinom natrijevog hidroksida, hidroksilne skupine nastale tijekom disocijacije alkalija, zamjenjuju jone broma formiranjem metanola. 
U nastavku je navedeno nekoliko reakcija koje omogućuju proizvodnju alkohola u laboratorijima.
Nukleofilna adicija.
Grignardovi reagensi (spojevi magnezija s alkil halogenidima - jodidi ili bromidi), kao i organometalni spojevi bakra i litija reagiraju s karbonilnim skupinama (C = O) aldehida u obliku primarnih i sekundarnih alkohola, ovisno o mehanizmu dodavanja. , 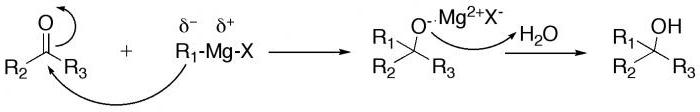
Barbier-ova reakcija odvija se između halogen-alkana i karbonilne skupine kao elektrofilni supstrat u prisutnosti magnezija, aluminija, cinka, indija, kositra ili njegovih soli. Produkt reakcije je primarni, sekundarni ili tercijarni alkohol. Njegov mehanizam je sličan Grignardovoj reakciji, s tom razlikom što je Barbier-ova reakcija sinteza u jednoj posudi, dok se Grignardov reagens priprema odvojeno prije dodavanja karbonilnog spoja. 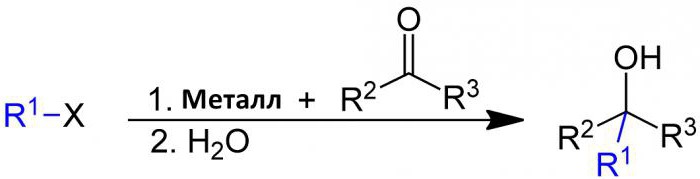 Kao nukleofilna reakcija adicije, ona se javlja kod relativno jeftinih i vodootpornih metala ili njihovih spojeva, za razliku od Grignardovih reagensa ili organolitijevih reagensa. Zbog toga je u mnogim slučajevima moguće voditi ga u vodi, što proces čini dijelom zelene kemije. Reakcija Barbier je nazvana po Philipu Barbieru, učitelju Victora Grignarda.
Kao nukleofilna reakcija adicije, ona se javlja kod relativno jeftinih i vodootpornih metala ili njihovih spojeva, za razliku od Grignardovih reagensa ili organolitijevih reagensa. Zbog toga je u mnogim slučajevima moguće voditi ga u vodi, što proces čini dijelom zelene kemije. Reakcija Barbier je nazvana po Philipu Barbieru, učitelju Victora Grignarda.
Reakcija oporavka
Aldehidi ili ketoni su reducirani do alkohola natrijevim borhidridom (NaBH4) ili (nakon obrade kiselinom) s litij aluminij hidridom (LiAlH).
U reakciji Meerwein-Pondorf-Wehrli (MPV), proizvodnja alkohola redukcijom iz ketona i aldehida odvija se upotrebom aluminijevog alkoksidnog katalizatora. Prednosti MPV-a su visoka kemoselektivnost i upotreba jeftinog, ekološki prihvatljivog metalnog katalizatora. Reakciju su otkrili Meerwein i Schmidt, a neovisno Verli 1925. Otkrili su da smjesa aluminijevog etoksida i etanola može reducirati aldehide u njihove alkohole. Ponndorf je primijenio reakciju na ketone i ažurirao katalizator na aluminij izopropilat (Al (Oi-Pr) 3 , gdje je i-Pr izopropilna skupina (CH (CH3) 2 ). kako bi se dobio izopropanol.
Opća jednadžba za dobivanje alkohola redukcijom ketona u alkoholima s MPV je kako slijedi:
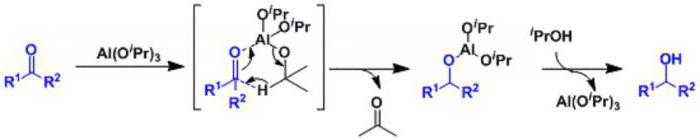
To, naravno, nije sve što se može reći o alkoholima i njihovim svojstvima, ali se nadamo da ste uspjeli dobiti opću ideju o njima.