Pojam, svojstva i naboj elektrona
Elektron je elementarna čestica, koja je jedna od glavnih jedinica u strukturi tvari. Napon elektrona je negativan. Najpreciznija mjerenja na početku dvadesetog stoljeća napravili su Milliken i Ioffe.
Napon elektrona je minus 1.602176487 (40) * 10 -1 9 Cl.
Kroz ovu vrijednost se mjeri električni naboj druge sitne čestice.

Opći pojam elektrona
U fizici elementarnih čestica se kaže da je elektron nedjeljiv i nestrukturiran. Ona je uključena u elektromagnetske i gravitacijske procese, pripada skupini leptona, kao i njegovoj antičestici - pozitronu. Među ostalim leptonima ima i najmanju težinu. Ako se elektroni i pozitroni sudaraju, to dovodi do njihovog uništenja. Takav par može nastati iz gama-kvantnih čestica.
Prije nego su neutrini izmjereni, elektron je bio smatran najsvjetlijom česticom. U kvantnoj mehanici se naziva fermionima. Također, elektron ima magnetski trenutak. Ako se pozitron također upućuje na njega, pozitron se dijeli kao pozitivno nabijena čestica, a elektron se naziva negatron, kao čestica s negativnim nabojem.
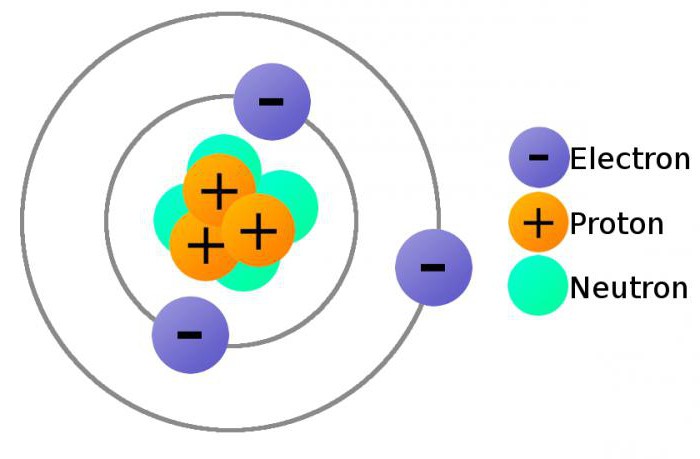
Odvojena svojstva elektrona
Elektroni pripadaju prvoj generaciji leptona, sa svojstvima čestica i valova. Svaka od njih ima kvantno stanje, koje se određuje mjerenjem energije, orijentacije spina i drugih parametara. Pripadnost fermionima u njoj otkriva se kroz nemogućnost da se u istom kvantnom stanju istovremeno nalaze dva elektrona (prema Paulijevom načelu).
Proučava se na isti način kao i kvazičestica u periodičnom kristalnom potencijalu, u kojoj se efektivna masa može značajno razlikovati od mase u mirovanju.
Kroz kretanje elektrona dolazi električna struja magnetizam i termo-emf. Punjenje elektrona u pokretu tvori magnetsko polje. Međutim, vanjsko magnetsko polje odbacuje česticu iz izravnog smjera. Tijekom ubrzanja, elektron stječe sposobnost apsorbiranja ili emitiranja energije kao fotona. Njegov skup sadrži elektroničke atomske ljuske, čiji broj i položaj određuju kemijska svojstva.
Atomska masa se uglavnom sastoji od nuklearnih protona i neutrona, dok masa elektrona To je reda veličine 0,06% ukupne atomske mase. Coulombova električna sila je jedna od glavnih sila koja može zadržati elektron blizu jezgre. Ali kada se molekule stvaraju iz atoma i nastaju kemijske veze elektroni se redistribuiraju u novoformiranom prostoru.
Pojava elektrona uključuje nukleone i hadrone. Izotopi s radioaktivnim svojstvima mogu emitirati elektrone. U laboratorijskim uvjetima, te se čestice mogu proučavati na posebnim uređajima, na primjer, teleskopi mogu detektirati zračenje iz njih u oblacima plazme.
otkriće
Elektron su otkrili njemački fizičari u devetnaestom stoljeću, kada su proučavali katodna svojstva zraka. Tada su ga drugi znanstvenici počeli detaljnije proučavati, dovodeći ga u rang jedne čestice. Proučavani su radijacijski i drugi srodni fizički fenomeni.
Na primjer, skupina koju je vodio Thomson procijenio je naboj elektrona i masu katodnih zraka, čiji odnos, kako je saznao, ne ovisi o izvoru materijala.
Becquerel je otkrio da sami minerali emitiraju zračenje, a njihove beta zrake mogu odstupati kroz djelovanje električnog polja, a masa i naboj zadržavaju isti omjer kao katodne zrake.
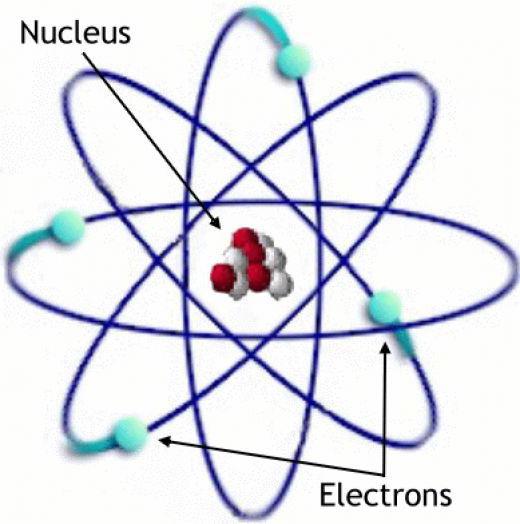
Atomska teorija
Prema toj teoriji, atom se sastoji od jezgre i elektrona oko nje, smještenih u kao oblak. Oni su u određenim kvantiziranim stanjima energije, čija je promjena popraćena procesom apsorpcije ili emisije fotona.
Kvantna mehanika
Na početku dvadesetog stoljeća formulirana je hipoteza prema kojoj materijalne čestice imaju svojstva i samih čestica i valova. Svjetlost se također može manifestirati u obliku vala (naziva se de Brogliejev val) i čestica (fotona).
Kao rezultat, formulirana je poznata Schrödingerova jednadžba, gdje je opisano širenje elektronskih valova. Ovaj se pristup naziva kvantna mehanika. Uz to su izračunata elektronička stanja energije u atomu vodika.
Temeljna i kvantna svojstva elektrona
Čestica pokazuje fundamentalna i kvantna svojstva.
Temeljni su masa (9.109 * 10 -31 kg), elementarni električni naboj (tj. Minimalni dio naboja). Prema dosadašnjim mjerenjima, u elektronu se ne nalaze elementi koji mogu otkriti njegovu podstrukturu. No, neki znanstvenici su mišljenja da je to čestica naboja. Kao što je naznačeno na početku članka, elektronički električni naboj iznosi -1.602 * 10 -19 Cl.
 Kao čestica, elektron može istovremeno biti i val. Eksperiment s dva proreza potvrđuje mogućnost istovremenog prolaska kroz njih. To je u sukobu sa svojstvima čestice, gdje je svaki put moguće proći samo kroz jedan prorez.
Kao čestica, elektron može istovremeno biti i val. Eksperiment s dva proreza potvrđuje mogućnost istovremenog prolaska kroz njih. To je u sukobu sa svojstvima čestice, gdje je svaki put moguće proći samo kroz jedan prorez.
Smatra se da elektroni imaju ista fizikalna svojstva. Stoga, njihova permutacija, sa stajališta kvantne mehanike, ne dovodi do promjene stanja sustava. Valna funkcija elektrona je antisimetrična. Stoga njegova rješenja nestaju kada isti elektroni padnu u isto kvantno stanje (Paulijev princip).