Zakon očuvanja mase u kemiji. Otkriće zakona
Zakon očuvanja mase temelj je za izračun fizičkih procesa u svim sferama ljudske aktivnosti. Njegovu pravdu ne osporavaju fizičari, kemičari ili predstavnici drugih znanosti. Ovaj zakon, kao strogi računovođa, prati usklađenost s točno određenom masom tvari prije i nakon interakcije s drugim tvarima. Čast otkrića ovog zakona pripada ruskom znanstveniku M. V. Lomonosovu.
Početno razumijevanje sastava tvari
Struktura materije stoljećima je ostala misterija za svaku osobu. Različite hipoteze uznemirile su umove znanstvenika i motivirale mudrace na dugotrajne i besmislene sporove. Jedna je tvrdila da se sve sastojalo od vatre, a drugo je branilo potpuno drugačije gledište. U masi teorija, teoriji drevnog grčkog mudraca Demokrita da se sve tvari sastoje od sitnih, sitnih čestica materije koje su nevidljive oku, nepravedno je zaboravljeno. Demokrit ih je nazvao "atomima", što znači "nedjeljivo". Nažalost, njegova je pretpostavka već 23 stoljeća zaboravljena.
alkemija
Većina znanstvenih podataka srednjeg vijeka temeljila se na predrasudama i raznim spekulacijama. Alkemija se javlja i rasprostranjena je zbirka skromnih praktičnih znanja, blisko ukrašenih najčudesnijim teorijama. Na primjer, poznati umovi tog vremena pokušali su olovo pretvoriti u zlato i pronaći kamen nepoznatog filozofa, koji liječi sve bolesti. U procesu traženja postupno nagomilanog znanstvenog iskustva, koje se sastoji od mnogih neobjašnjivih reakcija kemijskih elemenata. Na primjer, utvrđeno je da se mnoge tvari, koje se kasnije nazivaju jednostavnim, ne raspadaju. Tako je oživljena drevna teorija nedjeljivih čestica materije. Bio je to potreban sjajan um da bi se ova pohrana informacija pretvorila u koherentnu i logičku teoriju. 
Lomonosova teorija
Točna kvantitativna metoda istraživanja kemije obvezna je ruskom znanstveniku M. V. Lomonosovu. Za svoje briljantne sposobnosti i naporan rad dobio je zvanje profesora kemije i postao član Ruske akademije znanosti. Pod njim je organiziran prvi moderni kemijski laboratorij u zemlji, u kojem je otkriven čuveni zakon o očuvanju mase tvari. 
U procesu proučavanja toka kemijske reakcije Lomonosov je izvagao izvorne kemikalije i proizvode koji su se pojavili nakon reakcije. Istodobno je otkrio i formulirao zakon očuvanja mase tvari. U 17. stoljeću pojam masa često je bio pomiješan s pojmom "težina". Stoga se mase tvari često nazivaju "utezi". Lomonosov je utvrdio da je struktura materije izravno ovisna o česticama iz kojih je izgrađena. Ako sadrži čestice iste vrste, znanstvenik je takvu supstancu nazvao jednostavnom. S heterogenim sastavom krvnih zrnaca dobiva se kompleksna tvar. Ovi teoretski podaci omogućili su Lomonosovu da formulira zakon očuvanja mase.
Definicija prava
Nakon brojnih eksperimenata, MV Lomonosov je uspostavio zakon, čija je suština bila sljedeća: težina tvari koje su ušle u reakciju jednaka je težini tvari koje su rezultirale reakcijom. 
U ruskoj znanosti, ovaj postulat se zove "Zakon o očuvanju mise Lomonosovih tvari"
Ovaj zakon je formuliran 1748. godine, a najprecizniji eksperimenti s reakcijom spaljivanja metala u zatvorenim posudama provedeni su 1756. godine.
Lavoisierovi eksperimenti
Europska znanost otkrila je zakon konzervacije mase nakon objave opisa djela velikog francuskog kemičara Antoinea Lavoisiera.  Ovaj je znanstvenik u svojim eksperimentima hrabro primijenio teorijske ideje i fizikalne metode vremena, što mu je omogućilo da razvije kemijsku nomenklaturu i stvori registar svih poznatih kemikalija u to vrijeme.
Ovaj je znanstvenik u svojim eksperimentima hrabro primijenio teorijske ideje i fizikalne metode vremena, što mu je omogućilo da razvije kemijsku nomenklaturu i stvori registar svih poznatih kemikalija u to vrijeme.
Lavoisier je svojim eksperimentima dokazao da se tijekom bilo koje kemijske reakcije promatra zakon očuvanja mase tvari koje ulaze u spoj. Osim toga, proširio je distribuciju zakona očuvanja na masu svakog od elemenata koji su sudjelovali u reakciji kao dio složenih tvari.
Na pitanje o tome tko je otkrio zakon očuvanja mase tvari može se odgovoriti na dva načina. MV Lomonosov bio je prvi koji je proveo pokuse koji jasno demonstriraju zakon očuvanja i doveo ga pod teorijsku osnovu. A. Lavoisier, 1789., neovisno o ruskom znanstveniku, samostalno otkriva zakon masovnog očuvanja i proširuje svoj princip na sve elemente koji sudjeluju u kemijskoj reakciji.
Masa i energija
Godine 1905. veliki A. Einstein je pokazao vezu između mase tvari i njezine energije. Izražena je formulom:
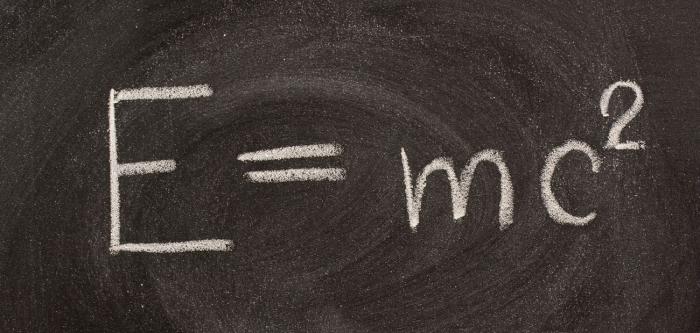
Einsteinova jednadžba potvrđuje zakon očuvanja mase i energije. Ta teorija tvrdi da svaka energija ima masu, a promjena te energije je promjena tjelesne mase. Potencijalna energija bilo koje tijelo je vrlo veliko i može se osloboditi samo pod posebnim uvjetima.
Zakon o očuvanju mase vrijedi za sva tijela mikro i makrokozmosa. Svaka kemijska reakcija je uključena u pretvorbu unutarnja energija tvari. Stoga bi pri izračunavanju mase tvari uključenih u kemijske reakcije bilo potrebno uzeti u obzir povećanje ili smanjenje mase uzrokovano otpuštanjem ili apsorpcijom energije u danoj reakciji. U stvari, u makrokozmosu, ovaj je učinak tako beznačajan da se takve promjene mogu zanemariti.