Najjača kiselina. Formula najjače kiseline
O tome koja je kiselina najjača, tvrdilo se više od jedne generacije kemičara. U različito vrijeme, ovaj naslov je dobio dušik, sumpor, klorovodična kiselina. Neki su vjerovali da ne može postojati spoj jači od fluorovodične kiseline. Nedavno su dobiveni novi spojevi s jakim kiselinskim svojstvima. Možda je među njima najjača kiselina na svijetu? U članku se raspravlja o karakteristikama najjačih postojanih kiselina našeg vremena i daje njihove kratke kemijske karakteristike.
Koncept kiseline 
Kemija je točna kvantitativna znanost. A naslov "Najjača kiselina" mora se razumno pripisati jednoj ili drugoj supstanci. Što može biti glavni pokazatelj koji karakterizira snagu bilo koje veze?
Prvo, zapamtimo klasičnu definiciju kiseline. U osnovi, ova riječ se koristi za složene kemijske spojeve koji se sastoje od vodikovog i kiselinskog ostatka. Broj vodikovih atoma u spoju ovisi o valenciji kiselinskog ostatka. Na primjer, u molekuli klorovodične kiseline postoji samo jedan atom vodika; i sumporna kiselina već ima dva H + atoma.
Kiselinska svojstva
Sve kiseline imaju određena kemijska svojstva koja se mogu nazvati zajedničkom ovom razredu kemijskih spojeva.
- Sposobnost interakcije s metalima uz oslobađanje vodika.
- Sposobnost interakcije s bazama, uz naglašavanje soli.
- Sposobnost promjene boje indikatora - na primjer, izazvati crvenilo lakmus papira.

U svim gore navedenim svojstvima očituje se još jedna “vještina” bilo koje poznate kiseline - sposobnost darovanja atoma vodika, zamjenjujući ga atomom druge kemikalije ili molekulom spoja. Upravo ta sposobnost karakterizira "snagu" kiseline i stupanj njene interakcije s drugim kemijskim elementima.
Voda i kiselina
Prisutnost vode značajno smanjuje sposobnost kiseline da oslobodi atome vodika. To je zato što vodik može oblikovati svoje kemijske veze između molekula kiseline i vode, pri čemu je njegova sposobnost odvajanja od baze manja od sposobnosti nerazrijeđenih kiselina.
superkiseli
Riječ "superkiselina" uvedena je u kemijski rječnik 1927. godine, uz laganu ruku poznatog kemičara Jamesa Conanta.
Standard čvrstoće ovog kemijskog spoja jest koncentrirana sumporna kiselina. Kemijska tvar ili bilo koja smjesa koja prelazi kiselost koncentrirane sumporne kiseline naziva se superkiselina. Vrijednost superkiseline određena je njezinom sposobnošću da daje pozitivno električni naboj iz bilo kojeg razloga. Za osnovni parametar za određivanje kiselosti usvojen je odgovarajući pokazatelj H2S04. Među jakim kiselinama postoje tvari s prilično neobičnim imenima i svojstvima.
Poznate jake kiseline
Najpoznatije kiseline iz tijeka anorganske kemije su hidrojodične (HI), bromovodične (HBr), klorovodične (HCl), sumporne (H2S04) i dušične (HNO3) kiseline. Svi imaju visok indeks kiselosti i mogu reagirati s većinom metala i baza. U ovoj seriji najjača kiselina je mješavina dušične i klorovodične kiseline, nazvane "aqua regia". Formula najjače kiseline u ovoj seriji jest HN03 + 3 HCl. Ovaj spoj može otopiti čak i plemenite metale kao što su zlato i platina.

Čudno je da fluorovodična kiselina, koja je spoj vodika s najjačim halogenom - fluorom, nije postala kandidat za naslov "Najjača kiselina u kemiji". Jedina značajka ove tvari je sposobnost otapanja stakla. Stoga se takva kiselina pohranjuje u polietilenski spremnik.
Jake organske kiseline
Kandidati za titulu "Najjača kiselina u organskoj kemiji" - mravlja i octena kiseline. Mravlja kiselina je najjači u homolognom rasponu ograničavajućih kiselina. Ime je dobila zbog činjenice da je dio toga sadržan u izlučevinama mrava.

Octena kiselina je malo slabija od mravlje kiseline, ali je njezin spektar raspodjele mnogo širi. Često se nalazi u sokovima biljaka i nastaje tijekom oksidacije raznih organskih tvari.
Nedavni razvoj u području kemije dopustio je sintezu nove tvari koja se može natjecati s tradicionalnim organskim tvarima. Trifluorometansulfonska kiselina ima indeks kiselosti veći od sumporne kiseline. U isto vrijeme, CF3SO3H je stabilna higroskopna tekućina s utvrđenim fizikalno-kemijskim svojstvima u normalnim uvjetima. Danas se ovom spoju može dodijeliti naslov „Najjača organska kiselina“.
Mnogi misle da stupanj kiselosti ne može biti značajno viši od stupnja sumporne kiseline. No nedavno su znanstvenici sintetizirali niz tvari čije su parametre kiselosti nekoliko tisuća puta veće od vrijednosti sumporne kiseline. Spojevi dobiveni interakcijom protonskih kiselina s Lewis-ovom kiselinom imaju abnormalno visoke vrijednosti kiselosti. U znanstvenom svijetu nazivaju se: složene protonske kiseline.
Magična kiselina
Da. U redu Magična kiselina. To se zove. Magična kiselina je smjesa vodikovog fluorida ili fluor sulfonske kiseline s antimon pentafluoridom. Kemijska formula ovog spoja prikazana je na slici: 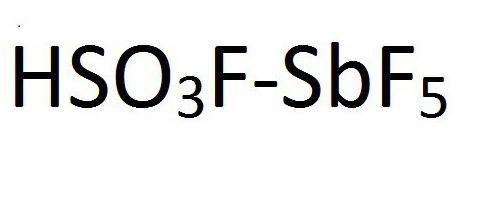
Taj čudan naziv magične kiseline primljen je na božićnoj zabavi kemičara, koja se dogodila početkom 1960-ih. Član istraživačkog tima, J. Olaha, pokazao je smiješan trik, rastvarajući voštanu svijeću u ovoj nevjerojatnoj tekućini. To je jedna od najjačih kiselina u novoj generaciji, ali je već sintetizirana supstanca koja ga nadilazi u snazi i kiselosti.
Najjača kiselina na svijetu
Karborska kiselina je karboranska kiselina, koja je daleko najjači spoj na svijetu. Formula najjače kiseline izgleda ovako: H (CHB11C11).
Ovo čudovište nastalo je 2005. godine na Kalifornijskom sveučilištu, u uskoj suradnji s Novosibirskim institutom za katalizu SB RAS.
Sama ideja sinteze pojavila se u umovima znanstvenika, zajedno sa snom o novim, nevidjenim molekulama i atomima. Nova kiselina je milijun puta jača od sumporne, dok je potpuno neagresivna, a najjača kiselina se lako može pohraniti u staklenoj bočici. Međutim, s vremenom se staklo još uvijek otapa, a povećanjem temperature brzina ove reakcije se značajno povećava. 
Ova nevjerojatna mekoća je zbog visoke stabilnosti novog spoja. Kao i sve kemikalije povezane s kiselinama, karboranska kiselina odmah reagira, odustajeći od svog jedinog protona. Baza kiseline je tako stabilna da kemijska reakcija ne ide dalje.
Kemijska svojstva karboranske kiseline
Nova kiselina je izvrstan donor protona H + . To je ono što određuje snagu ove tvari. Otopina karboranske kiseline sadrži više vodikovih iona nego bilo koja druga kiselina na svijetu. U kemijskoj reakciji SbF 5 - antimon pentafluorid, veže ion fluora. Istovremeno se oslobađaju novi i novi atomi vodika. Stoga je karboranska kiselina najjača na svijetu - suspenzija protona u otopini je 2 × 10 19 puta veća od suspenzije sumporne kiseline.
Međutim, kisela baza ovog spoja je iznimno stabilna. Molekula ove tvari sastoji se od jedanaest atoma broma i istog broja atoma klora. U svemiru, te čestice tvore složenu, geometrijski pravilnu figuru, koja se naziva ikosahedron. Taj raspored atoma je najstabilniji, a to objašnjava stabilnost karboranske kiseline. 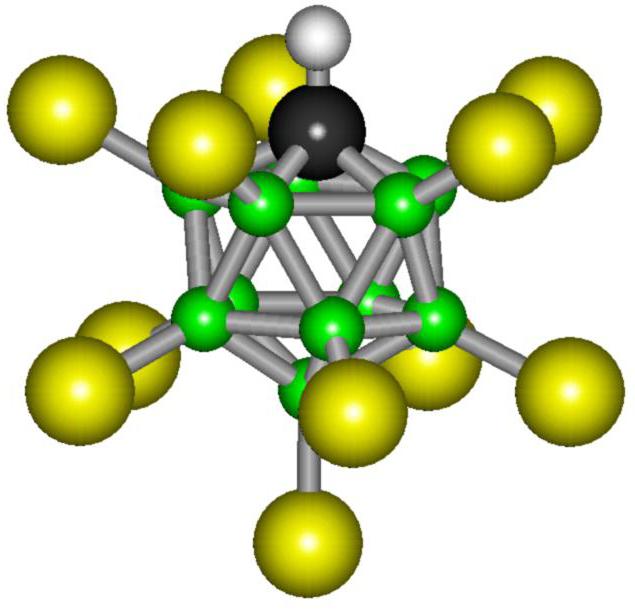
Vrijednost karboranske kiseline
Najjača kiselina na svijetu donijela je svojim tvorcima zaslužene nagrade i priznanja u znanstvenom svijetu. Iako sva svojstva nove tvari nisu u potpunosti shvaćena, već postaje jasno da značaj ovog otkrića nadilazi laboratorije i istraživačke institute. Karborna kiselina može se koristiti kao snažan katalizator u različitim industrijskim reakcijama. Osim toga, nova kiselina može komunicirati s najtvrdokornijim kemikalijama - inertnim plinovima. Trenutno je u tijeku rad, omogućujući mogućnost ulaska u reakciju ksenona.
Nesumnjivo, nevjerojatna svojstva novih kiselina naći će svoju primjenu u različitim područjima znanosti i tehnologije.