Što je sol? Formula, svojstva soli (kemija)
Da biste odgovorili na pitanje što je to sol, obično ne morate dugo razmišljati. Ovaj kemijski spoj u svakodnevnom životu je vrlo čest. Na uobičajenu kuhinjsku sol i ne mogu govoriti. Detaljna unutarnja struktura soli i njihovih spojeva proučava se anorganskom kemijom.
Određivanje soli
Jasan odgovor na pitanje što je sol može se naći u djelima M. V. Lomonosova. To je ime dao krhkim tijelima koja se mogu otopiti u vodi i ne zapaliti pod utjecajem visokih temperatura ili otvorenog plamena. Kasnija definicija nije izvedena iz njihovih fizičkih, već iz kemijskih svojstava tih tvari. 
Školski udžbenici anorganske kemije daju prilično jasan koncept o tome što je to sol. To je naziv supstitucijskih produkata kemijske reakcije, u kojima se vodikovi atomi kiseline u spoju zamjenjuju metalom. Primjeri tipičnih spojeva soli: NaCL, MgS04. Lako je vidjeti da se bilo koji od ovih zapisa može podijeliti na dvije polovice: metal će uvijek biti napisan u lijevoj komponenti formule, a kiselinski ostatak u desnoj komponenti. Standardna solna formula je kako slijedi:
Me n m Kiselinski ostatak m n .
Fizikalna svojstva soli
Kemija, kao egzaktna znanost, u ime tvari ulaže sve moguće informacije o svom sastavu i mogućnostima. Dakle, sva imena soli u suvremenoj interpretaciji sastoje se od dvije riječi: jedan dio ima naziv metalne komponente u nominativnom slučaju, drugi sadrži opis kiselinskog ostatka.
Ovi spojevi nemaju molekularnu strukturu, dakle, u normalnim uvjetima, to su krute kristalne tvari. Mnoge soli imaju kristalnu rešetku. Kristali tih tvari su vatrostalni, tako da su potrebne visoke temperature. Na primjer, barijev sulfid se tali na oko 2200 ° C. 
Prema topljivosti, sol se dijeli na topljive, slabo topljive i netopljive. Primjer prvog može poslužiti kao natrijev klorid, kalijev nitrat. Malo topljiv magnezijev sulfit, olovo klorid. Netopljiv je kalcijev karbonat. Informacije o topljivosti tvari sadržane su u referentnim knjigama.
Predmetni proizvod kemijske reakcije je obično bez mirisa i ima drugačiji okus. Pretpostavka da su sve soli slane je pogrešna. Čisti slani okus ima samo jedan element ove klase - našu staru poznatu kuhinjsku sol. Postoje slatke soli berilija, gorko-magnezijeve i neukusne - na primjer, kalcijev karbonat (obična kreda).
Većina tih tvari je bezbojna, ali među njima ima i onih koje imaju karakteristične boje. Na primjer, željezo (II) sulfat karakterizira karakteristična zelena boja, kalijev permanganat je ljubičasta, a kristali kalijevog kromata su svijetlo žute boje. 
Klasifikacija soli
Kemija dijeli sve vrste anorganskih soli na nekoliko osnovnih značajki. Soli koje su rezultat potpune supstitucije vodika u kiselini nazivaju se normalne ili srednje. Na primjer, kalcijev sulfat.
Sol koja se dobiva iz nepotpune supstitucijske reakcije naziva se kisela ili bazična. Primjer takve tvorbe može biti reakcija kalijevog hidrosulfata: 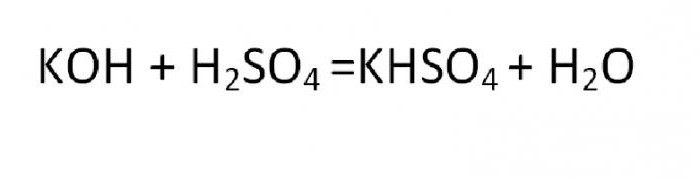
Bazična sol se dobiva reakcijom u kojoj hidroksilna skupina nije potpuno zamijenjena s kiselinskim ostatkom. Tvari ovog tipa mogu nastati od onih metala čija je valencija jednaka dva ili više. Tipična sol soli ove skupine može se izvesti iz ove reakcije:
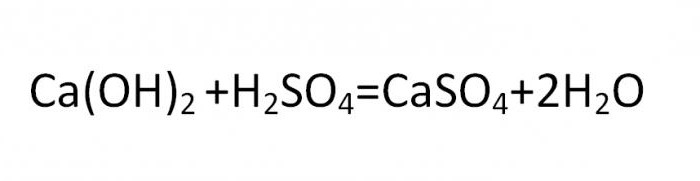
Normalni, srednji i kiseli kemijski spojevi tvore klase soli i standardna su klasifikacija tih spojeva.
Dvostruka i miješana sol
kemija anorganske tvari pokazuje da ovaj proizvod može biti formiran od dva metala i jedne kiseline. U ovom slučaju, kiselina mora imati bazičnost veću ili jednaku 2. Ovaj spoj se naziva dvostruka sol. Kemijske soli ove skupine su kalijevi alum, također se nazivaju kalijev aluminijev sulfat.
Primjer miješane kalcijeve soli je klorovodična i hipoklorična kiselina: CaOCl2 .
nomenklatura
Soli koje tvore metali s promjenjivom valencijom imaju dodatnu oznaku: iza formule u zagradama upisuju se valenca rimskih brojeva. Dakle, tu su željezni sulfat FeSO 4 (II) i Fe 2 (SO 4) 3 (III). U ime soli postoji prefiks hidro- ako u njegovom sastavu postoje nesupstituirani atomi vodika. Na primjer, kalijev hidrogen fosfat ima formulu K2HP04.
Svojstva soli u elektrolitima
teorija elektrolitička disocijacija daje vlastitu interpretaciju kemijskih svojstava. U svjetlu te teorije, sol se može definirati kao slab elektrolit koji se rastvara (raspadne) u vodi. Dakle, otopina soli može se predstaviti kao kompleks pozitivnih negativnih iona, pri čemu prvi nije atom vodika H + , a drugi ne atomi OH - hidroksi skupine. Ioni koji bi bili prisutni u svim vrstama otopina soli ne postoje, stoga ne posjeduju nikakve zajedničke osobine. Što su niže naboji iona koji tvore otopinu soli, to se bolje disociraju, to je veća vodljivost takve tekuće smjese.
Otopine kiselinskih soli
Kisele soli u otopini razgrađuju se u kompleksne negativne ione, koji su kiseli ostatak, i jednostavni anioni, koji su pozitivno nabijene metalne čestice.  Na primjer, reakcija otapanja natrijevog bikarbonata dovodi do razgradnje soli na natrijeve ione i ostatka HCO3-.
Na primjer, reakcija otapanja natrijevog bikarbonata dovodi do razgradnje soli na natrijeve ione i ostatka HCO3-.
Cjelovita formula izgleda ovako: NaHCO 3 = Na + + HCO 3 - , HC03 - = H + + CO;
Otopine glavnih soli
Disocijacija bazičnih soli dovodi do nastanka kiselih aniona i kompleksnih kationa koji se sastoje od metala i hidrokso skupina. Te kompleksne katione, pak, mogu se dezintegrirati u procesu disocijacije. Stoga u bilo kojoj otopini soli glavne skupine postoje OH - ioni. Na primjer, disocijacija hidroksomagnezijeva klorida odvija se kako slijedi: 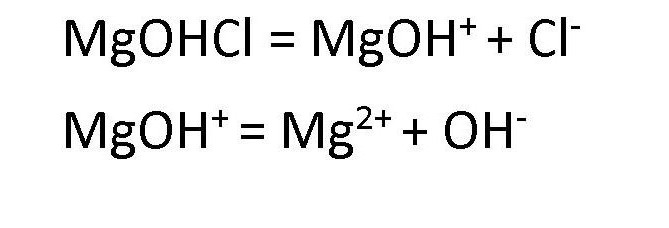
Raspodjela soli
Što je sol? Ovaj je element jedan od najčešćih kemijskih spojeva. Svi znaju sol, kreda (kalcijev karbonat) i tako dalje. Među karbonatnim solima najčešći je kalcijev karbonat. Sastavni je dio mramora, vapnenca, dolomita. Kalcijev karbonat također je osnova za formiranje bisera i koralja. Ovaj kemijski spoj je sastavni dio za stvaranje tvrdih komadića kod kukaca i kostura u akordima.
Sol nam je poznata od djetinjstva. Liječnici upozoravaju na prekomjernu uporabu, ali u umjerenim količinama, što je neophodno za provedbu vitalnih procesa u tijelu. I potrebno je održavati ispravan sastav krvi i proizvodnju želučanog soka. Saline, sastavni dio injekcija i kapaljki, nisu ništa slične otopini soli.