Arene: kemijska svojstva i metode proizvodnje
Aromatski kemijski spojevi ili arene su velika skupina karbocikličkih spojeva čije molekule sadrže stabilan ciklus od šest ugljikovih atoma. To se naziva "benzenski prsten" i uzrokuje posebne fizičke i kemijska svojstva arena.
Benzen i njegovi različiti homologi i derivati prvenstveno se odnose na aromatske ugljikovodike.
Molekule Arena mogu sadržavati nekoliko benzenskih prstena. Takvi spojevi nazivaju se aromatski spojevi s više jezgri. Na primjer, naftalen je dobro poznat lijek za zaštitu vunenih proizvoda od moljaca.
benzol
Ovaj najjednostavniji predstavnik arena sastoji se samo od benzenskog prstena. Njegova molekularna formula je C 6. 6 . Strukturna formula molekule benzena najčešće je predstavljena cikličkom formom koju je predložio A. Kekule 1865. godine.
Prednost ove formule je ispravan odraz sastava i ekvivalencije svih C i H atoma u prstenu. Međutim, nije mogla objasniti mnoga kemijska svojstva arena, stoga je tvrdnja o prisutnosti tri konjugirane dvostruke veze C = C pogrešna. To je postalo poznato tek s dolaskom moderne teorije komunikacije.
U međuvremenu je i danas pisanje formule benzena na način koji je predložio Kekule. Prvo, prikladno je pisati jednadžbe uz njegovu pomoć. kemijske reakcije. Drugo, moderni kemičari u njemu vide samo simbol, a ne stvarnu strukturu. Struktura molekule benzena danas se prenosi različitim tipovima strukturnih formula.
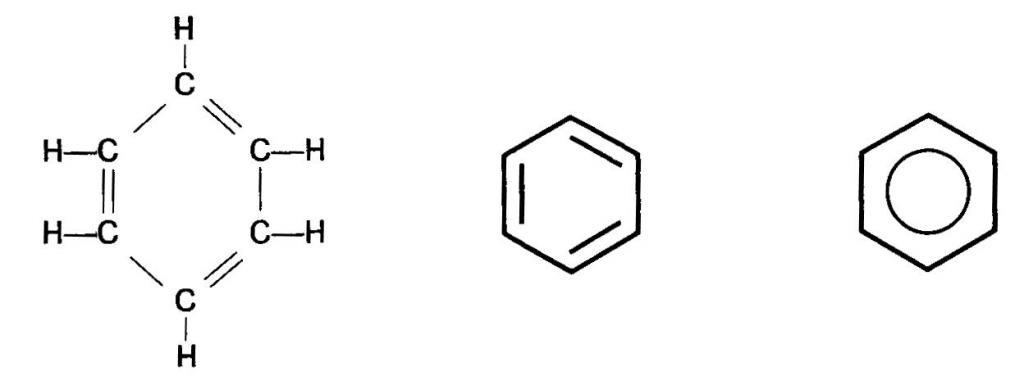
Struktura benzenskog prstena
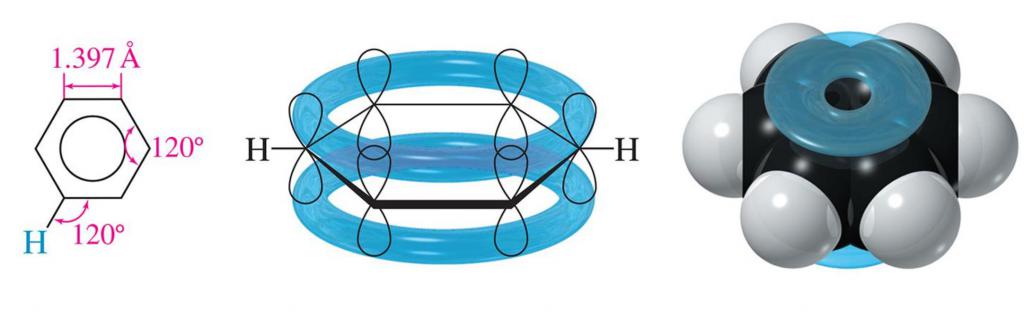
Glavna značajka benzenske jezgre je odsustvo jednostrukih i dvostrukih veza u njemu u tradicionalnom smislu. U skladu s modernim konceptima, molekula benzena čini se kao ravni šesterokut s duljinama stranica jednakim 0,140 nm. Pokazalo se da je dužina veze C - C u benzenu srednja vrijednost između jednog (njegova duljina je 0,154 nm) i dvostruke vrijednosti (0,134 nm). U istoj ravnini leže C-H veze, koje sa rubovima šesterokuta tvore kut od 120 °.
Svaki atom C u strukturi benzena je u sp2-hibridnom stanju. Povezana je kroz tri hibridne orbitale s dva C-atoma smještena u susjedstvu i jedan atom N. To jest, tvori tri s-veze. Druga, ali već ne-hibridizirana, 2p-orbitalna njezina, preklapa se s istim orbitalima susjednih C-atoma (desno i lijevo). Njegova je osa okomita na ravninu prstena, pa se preklapanje orbitala događa iznad i ispod njega. U ovom slučaju nastaje zajednički zatvoreni π-elektronski sustav. Zbog ekvivalentnog preklapanja 2p orbitala šest C-atoma dolazi do neke vrste "izjednačavanja" C-C i C = C veza.
Rezultat tog procesa je sličnost takvih "jedno-polnih" obveznica s dvostrukim i pojedinačnim obveznicama. To objašnjava činjenicu da arene pokazuju kemijska svojstva karakteristična za alkane i alkene.
Energija veze ugljik-ugljik u benzenskom prstenu je 490 kJ / mol. Što je također prosjek između energija jednostavnih i višestrukih dvostrukih veza.
Nomenklatura Arene
Temelj imena aromatskih ugljikovodika je benzen. Atomi u prstenu numerirani su višim supstituentom. Ako su supstituenti ekvivalentni, tada se numeriranje provodi najkraćim putem.
Za mnoge benzolne homologe često se koriste trivijalna imena: stiren, toluen, ksilen, itd. Da bi se odrazili relativni položaji supstituenata, uobičajeno je koristiti prefiksni orto, meta, par.
Ako u molekuli postoje funkcionalne skupine, na primjer karbonil ili karboksil, tada se molekula arene smatra aromatskim radikalom koji je s njom povezan. Na primjer, -C6_5-fenil, -C6_4-fenilen, C6.5-C2-2-benzil.
Fizička svojstva
Prvi predstavnici u. T homologne serije Benzen je bezbojna tekućina specifičnog mirisa. Njihova težina je lakša od vode, u kojoj se praktički ne rastapaju, već se dobro rastvaraju u većini organskih otapala.
Sve aromatski ugljikovodici oni izgaraju pojavom dimnog plamena, što se objašnjava visokim sadržajem C u molekulama. Točke taljenja i vrelišta se povećavaju s povećanjem vrijednosti molekulskih masa u homolognoj seriji benzena.
Kemijska svojstva benzena
Od različitih kemijskih svojstava arena, reakcije supstitucije treba spomenuti odvojeno. Vrlo značajne su i neke reakcije adicije koje se odvijaju pod posebnim uvjetima i oksidacijskim procesima.
Reakcije zamjene
Vrlo mobilni π-elektroni benzenskog prstena sposobni su vrlo aktivno reagirati s napadnim elektrofilima. Sama benzenska jezgra u benzenu i ugljikovodični lanac povezan s njom u svojim homologima sudjeluju u takvoj elektrofilnoj supstituciji. Mehanizam tog procesa detaljno je proučavan organskom kemijom. Kemijska svojstva arena povezanih s elektrofilnim napadom manifestiraju se kroz tri faze.
- Prva faza. Pojava π-kompleksa zbog vezanja π-elektronskog sustava benzenske jezgre na X + česticu, koja se veže na šest π-elektrona.
- Druga faza Prijelaz π-kompleksa u s, zbog oslobađanja para od šest π-elektrona u paru, tvoreći kovalentnu vezu C-X. Ostala četiri su preraspodijeljena između pet C-atoma u benzenskom prstenu.
- Treća faza. Uz brzu eliminaciju protona iz s-kompleksa.
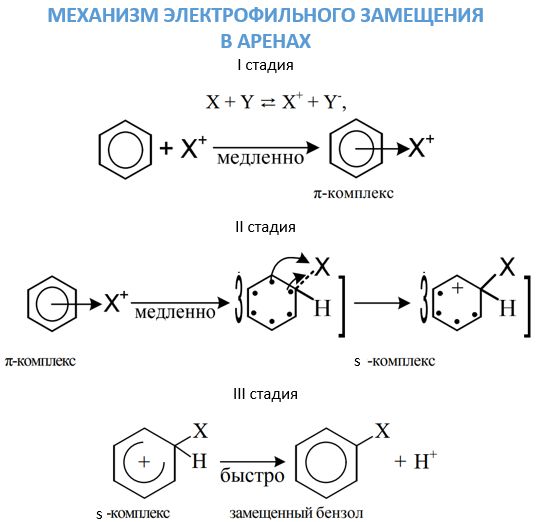
Bromiranje benzena u prisutnosti željeznih ili aluminijevih bromida bez zagrijavanja dovodi do proizvodnje bromobenzena:
C6 = 6 + Br2-> C6'5-Br + Br.
Nitriranje sa smjesom dušične i sumporne kiseline dovodi do stvaranja spojeva s nitro skupinom u prstenu:
C 6 + 6 + OONO 2 -> C 6 — 5 - NO 2 + 2 O.
Sulfoniranje se vrši pomoću bisulfonijevog iona koji nastaje reakcijom:
3Η2SO4 ⇄S033 + + Η3O + + 2ΗSO4-,
ili sumpor trioksid.
Odgovara ovom kemijskom svojstvu reakcije arena:
C6H6 + S03H + - C6H5 - S03H + H + .
Reakcije alkil i acil supstitucije, ili Friedel-Crafts-ova reakcija, provode se u prisutnosti bezvodnog AlCl3.
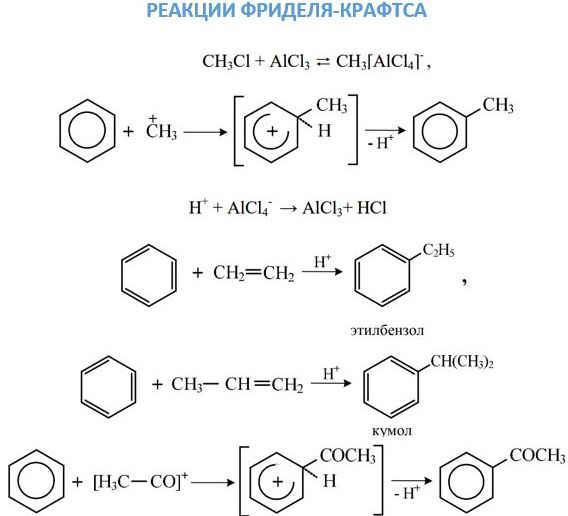
Te su reakcije malo vjerojatne za benzen i nastavljaju se s poteškoćama. Dodavanje vodikovih halogenida i vode benzenu se ne događa. Međutim, pri vrlo visokim temperaturama u prisutnosti platine moguća je reakcija hidrogenacije:
C6_6 + 3H2-> C6H12.
Pod ultraljubičastim zračenjem molekule klora mogu se pridružiti molekuli benzena:
C6_6 + 3Cl2-> C6'6Cl6.
Reakcije oksidacije
Benzen je visoko otporan na oksidirajuća sredstva. Dakle, ne mijenja boju ružičaste otopine kalijevog permanganata. Međutim, u prisutnosti vanadijevog oksida, može se oksidirati zrakom kisika do maleinske kiseline:
S 6 N 6 + 4O -> SOOΗ-SΗ = SΗ-SOOΗ.
U zraku, benzen gori s pojavom čađe:
2C 6 + 6 + 3O2 → 12C + 6Η2O.
Kemijska svojstva arena
- Zamjena.
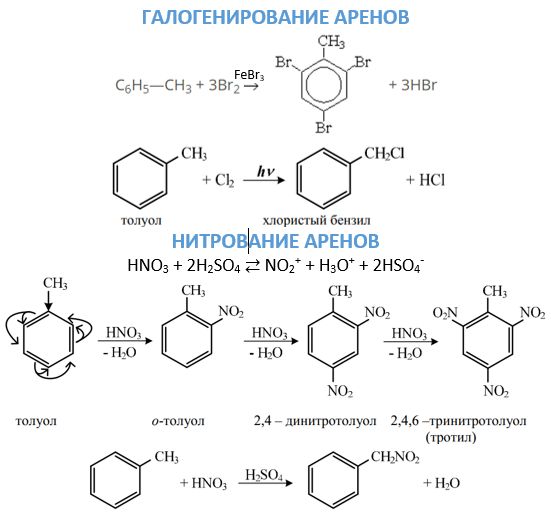
- Halogeniranje se može odvijati na različite načine, ovisno o uvjetima reakcije. U prisutnosti odgovarajućeg željeza ili aluminijevog halida, supstitucija će se nastaviti u prstenu prema mehanizmu koji je detaljno opisan gore. Za uvođenje atoma halogena u bočni lanac, reakcija se provodi zagrijavanjem bez katalizatora ili na svjetlu.
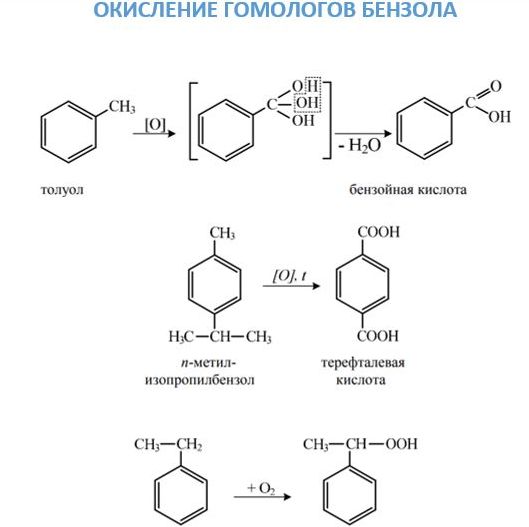
- Nitriranje aromatskih ugljikovodika s nitronijevim ionom, koji nastaje miješanjem sumporne i dušične kiseline, dovodi do povezivanja nitro skupine s benzenskom jezgrom. Veza nitro skupine s bočnim lancem je moguća za vrijeme Konovalove reakcije. 2. Oksidacija. Ovo kemijsko svojstvo arena može se promatrati s dvije točke gledišta. S jedne strane, oni se prilično lako oksidiraju, a bočni lanac je izložen djelovanju da formira karboksilnu skupinu. Ako su dva supstituenta povezana s prstenom u aromatskoj ugljikovodičnoj molekuli, tada se stvara dibazična kiselina. S druge strane, oni, poput benzena, izgaraju formiranjem čađe i vode.
Pravila orijentacije
Koji položaj (o-, m- ili p-) zamjenik će zauzeti tijekom interakcije elektrofilnog sredstva s benzenskim prstenom određen je pravilima:
- ako već postoji bilo koji supstituent u benzenskoj jezgri, on je taj koji usmjerava dolazeću skupinu na određeno mjesto;
- Svi orijentacijski supstituenti podijeljeni su u dvije skupine: Orijentanti prve vrste usmjeravaju ulaznu skupinu atoma na orto i para pozicije (—N2, -OΗ, -CΗ3, -C2H5, halogeni); Orijentanti druge vrste usmjeravaju dolazne supstituente na meta poziciju (-N02, -S03, -C02, -COO).
Orijentanti su ovdje navedeni prema redu padajuće sile.
Važno je napomenuti da je ovo razdvajanje skupina supstituenata uvjetovano, zbog činjenice da većina reakcija formira sva tri izomera u većini reakcija. Orijentanti utječu samo na to koji će se izomeri dobiti u većim količinama.
Dobijam Arenas
Glavni izvori arena su suha destilacija ugljena i rafiniranje nafte. Ugljeni katran sadrži veliku količinu svih vrsta aromatskih ugljikovodika. Neke vrste ulja sadrže do 60% arena, koje se lako izoliraju jednostavnom destilacijom, pirolizom ili pucanjem.
Sintetičke metode proizvodnje i kemijska svojstva arena često su međusobno povezane. Benzen, kao i njegovi homologi, dobiva se na jedan od sljedećih načina.
1. Reformiranje naftnih proizvoda. Dehidrogenacija alkana je najvažnija industrijska metoda za sintezu benzena i mnogih njegovih homologa. Reakcija se provodi propuštanjem plinova preko zagrijanog katalizatora (Pt, Cr 2 O 3 , oksidi Mo i V) pri t = 350–450 o C:
C6H14-> C6'6 + 4'2.
2. Reakcija Würz-Fittiga. Provodi se kroz fazu dobivanja organometalnih spojeva. Kao rezultat, reakcija može proizvesti nekoliko proizvoda.
3. Trimerizacija acetilena. Sam acetilen, kao i njegovi homologi, mogu formirati arene kada se zagrijavaju s katalizatorom:
3C 2 - 2 -> C 6. 6 .
4. Friedel-Craftsova reakcija. Gore je razmatrana kemijska svojstva arena, metoda proizvodnje i transformacije homologa benzena.
5. Priprema odgovarajućih soli. Benzen se može razlikovati destilacijom soli. benzojeva kiselina s alkalijama:
C6_5-COONa + Na02-C6_6 + Na2C03.
6. Oporavak ketona:
C6 – 5 - CO - CΗ 3 + Zn + 2ΗCl -> C 6 5 - C 2 2 - C 3 3 + 2 O + ZnCl 2 ;
CΗ 3 –C 6 – 5 –CO-CΗ 3 + NΗ 2 –NΗ 2 -> CΗ 3 –C 6 5 –CΗ 2 –CΗ 3 + 2 O.
Koristite arene
Kemijska svojstva i primjena arena izravno su međusobno povezani, jer se većina aromatskih spojeva koristi za daljnju sintezu u kemijskoj proizvodnji i ne koristi se u gotovom obliku. Iznimke su tvari koje se koriste kao otapala.
Benzen C6-6 se uglavnom koristi u sintezi etilbenzena, kumena i cikloheksana. Na temelju njega dobivaju se međuprodukti za proizvodnju raznih polimera: gume, plastike, vlakana, bojila, površinski aktivnih tvari, insekticida, lijekova.

Toluen C6H5-CH3 koristi se u proizvodnji boja, lijekova i eksploziva.
Kao otapalo ili kao početni pripravak za sintezu organskih tvari koriste se ksileni S 6 Η 4 (S 3 ) 2 u miješanom obliku (tehnički ksilen).
Izopropil benzen (ili kumen) C6-4C2 (C3 3 ) 2 je početni reagens za sintezu fenola i acetona.
Vinilbenzen (stiren) C 6 Η 5 -CΗ = Η 2 je sirovina za proizvodnju najvažnijeg polimernog materijala - polistirena.