Kemijska svojstva karboksilnih kiselina i metode dobivanja
Kemijski spojevi, koji se sastoje posebno od karboksilne skupine COOH, dobili su naziv karboksilne kiseline od znanstvenika. Postoji veliki broj imena tih spojeva. Oni su klasificirani prema različitim parametrima, na primjer, broj funkcionalnih skupina, prisutnost aromatskog prstena i tako dalje.
Struktura karboksilnih kiselina
Kako je već spomenuto, da bi kiselina bila karboksilna, ona mora imati karboksilnu skupinu, koja zauzvrat ima dva funkcionalna dijela: hidroksil i karbonil. Njihova interakcija je osigurana funkcionalnom kombinacijom jednog ugljikovog atoma s dva kisika. Kemijska svojstva karboksilnih kiselina ovise o strukturi ove skupine.
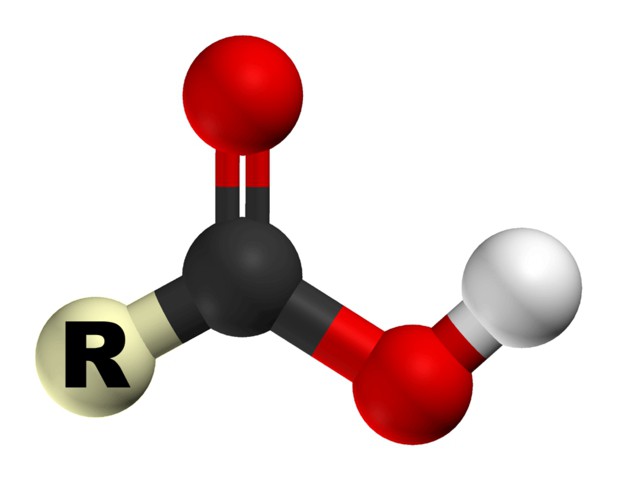
Zbog karboksilne skupine, ove organski spojevi može se nazvati kiselinama. Njihova svojstva su zbog povećane sposobnosti vodikovog iona H + da bude privučen kisikom, dodatno polarizirajući OH vezu. I zbog ove osobine, organske kiseline mogu disocirati u vodenim otopinama. Sposobnost otapanja smanjuje se obrnuto s povećanjem molekularne težine kiseline.
Vrste karboksilnih kiselina
Kemičari izlučuju nekoliko skupina organskih kiselina.
Klasifikacija karboksilne kiseline | |
Po broju funkcionalnih skupina | monokarboksilne |
dikarboksilna | |
polikarboksilne | |
Po prirodi radikalan | alifatski |
aromatičan | |
cikličan | |
Prema stupnju zasićenja radikala | nezasićen |
zasićen | |
Prisustvom funkcionalnih skupina u radikalu, to jest, supstitucijom jednog vodikovog atoma | Halogen (Cl2, F2, Br2, I2) |
Oxogroup (COH) | |
Hidroksi (OH) | |
Amino skupina (NH2 ) | |
Monobazične karboksilne kiseline sastoje se od ugljikova skeleta i samo jedne funkcionalne karboksilne skupine. Svaki student poznaje kemijska svojstva karboksilnih kiselina. Nastavni plan i program 10. razreda u kemiji uključuje izravno proučavanje svojstava monobazičnih kiselina. Dibazne i polibazične kiseline u svojoj strukturi imaju dvije ili više karboksilnih skupina.
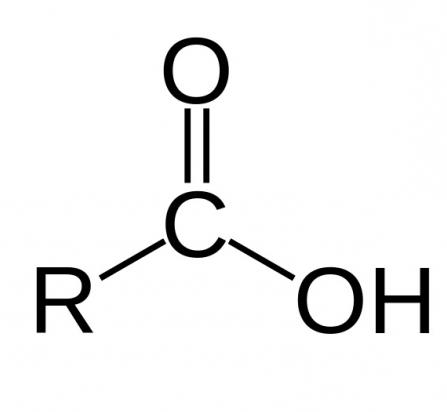
Također, zbog prisutnosti ili odsutnosti dvostrukih i trostrukih veza u molekuli postoje nezasićene i zasićene karboksilne kiseline. Kemijska svojstva i njihove razlike bit će razmotrene u nastavku.
Ako organska kiselina ima supstituirani atom u radikalu, tada njegovo ime uključuje naziv supstituentske skupine. Dakle, ako je atom vodika zamijenjen halogenom, tada će naziv kiseline sadržavati naziv halogena. Iste promjene proći će pod imenom, ako postoji zamjena aldehidom, hidroksilnom ili amino skupinom.
Izomerija organskih karboksilnih kiselina
Gotovo svi organska tvar imaju sposobnost izomerizacije. Karboksilne kiseline nisu iznimka. Razlikuju se sljedeće vrste izomerije:
- Ugljikov kostur.
- Interklasna izomerija.
- Prostorna izomerija;
Sposobnost izomerizacije izravno utječe na kemijska svojstva karboksilnih kiselina.
Izomerija kostura je moguća za kiseline čiji ugljikovodici sadrže najmanje četiri atoma ugljika. Interklasa je zauzvrat moguća za kiseline s dva ugljikova atoma u radikalu. Samo su karboksilne kiseline s pojedinačnim vezama u kosturu sposobne za prostor.
Navedite i bitne karboksilne kiseline
Imena i formule poznatih karboksilnih kiselina | ||
Sustavno ime kiseline | Trivijalno ime | Formula karboksilne kiseline |
Metanska kiselina | mravlja | HCOOH |
Etanoična kiselina | octena | CH2COOH |
Propanonska kiselina | propan | CH3CH2COOH |
Butanska kiselina | ulje | CH3CH2CH2COOH |
Pentanska kiselina | odoljen | CH3CH2CH2CH2COOH |
Pentenska kiselina | akril | CH2 = CH-COOH |
Benzen karboksilna kiselina | benzojeve | C6H5COOH |
heksadekanoilne | palmitinski | C15H31COOH |
Oksodekanovaya | stearinska | C17H35COOH |
oksalna | oksalnu | HOOC-COOH |
propionska | malonske | HOOC-CH2-COOH |
butan | jantar | HOOC-CH2-CH2-COOH |
Benzen dikarboksil | ftalnog | HOOC-C6H5-COOH |
2-hidroksi-propanska kiselina | mljekara | CH3CHOHCOOH |
Hidroksibutandionska kiselina | jabuka | HOOC-CH2CHOH-COOH |
2,3-dihidroksibutandioična kiselina | vino | HOOC- OHCH-OHCH-COOH |
3-karboksi-3-gidroksipentandiovaya | limunska | HOOC-CH2-CHOH-COOH-CH2COOH |
2-oksopropanska kiselina | piruvinsku | CH3COCOOH |
2-hidroksibenzojeva kiselina | salicilni | C6H5OHCOOH |
Karboksilne kiseline: kemijska svojstva
Za detaljnije razumijevanje suštine karboksilnih kiselina razmotrite njihova svojstva. U školskom kurikulumu, monobazične karboksilne kiseline smatraju se velikim volumenom, čija se kemijska svojstva manifestiraju u reakcijama između vodikovih halogenida, vode i drugih tvari. Sva ova vrsta kiseline:
- Odvojiti u otopini od vodikovih iona i radikala s karboksilom. S ovim mravlja kiselina odnosi se na elektrolite srednje čvrstoće, a octena slaba, tj. jačina disocijacije se smanjuje niz homologne serije.
- Obojite lakmus test u crveno.
- Provedite struju struje.
- Reagira s halogenima: 2RCOOH + Cl2 = 2RCOOCl + 2HCL.
- Oni ulaze u reakciju esterifikacije s alkoholima: R-COOH + R'OH = RCOOR '+ H20.
- Interakcija s nekim metalima: RCOOH + Mg = RCOOMg + H2.
- Reagirajte s osnovne okside tip i hidroksidi, tvoreći soli: RCOOH + NaOH = RCOONa + H2O.
- Reakcija sa solima: RCOOH + Na2CO3 = RCOONa + H2O + CO2.
Takva svojstva monobaznih kiselina objašnjavaju se promjenom karboksilne skupine, od hidroksila od kojeg se elektroni pomiču na najbliži atom ugljika, djelomično prigušujući njegov pozitivni naboj. Osim toga, karboksilne kiseline, čija su kemijska svojstva opisana gore, imaju dvosmjernu interakciju između atoma.
Kemijska svojstva drugih monobazičnih kiselina
Iz klasifikacije je poznato da su prisutne i monobazične nezasićene karboksilne kiseline, čija se kemijska svojstva razlikuju od onih graničnih.
Dakle, kiseline dvostruke veze u ugljikovodičnom radikalu su monobazične nezasićene karboksilne kiseline. Kemijske osobine takvih kiselina izražene su u reakcijama:
- S vodikovim halidom, ali mnogo sporijim od ograničavajućih i suprotno Markovnikovom pravilu, jer karboksilna skupina smanjuje elektronsku gustoću dvostruke veze: R = CH-COOH + HCl = RCl-CH2-COOH.
- S halogenima: Br2 + R = CH-COOH = RBr-CHBr-COOH.
- S vodikom, što rezultira prekidom dvostruke veze: H2 + R = CH-COOH = COOH-R-CH.
- Oprezna oksidacija, kao rezultat toga, formiranje hidroksi kiselina: R = CH-COOH + H20 [O] R (OH) -CH (OH) COOH.
- Radikalna oksidacija koja se javlja s rupturom molekula kiseline (na primjer, propenska kiselina): CH3-CH = C-COOH + H20 [O] CH3COOH + HOOC-COOH.
- Polimerizacija: n COOH- (CH = CH) -R = n (-COOH-CH-CH-R-)
Kemijske osobine bikarboksilnih kiselina
Dikarboksilne organske kiseline su dibazične karboksilne kiseline. Kemijska svojstva takvih kiselina razlikuju se od svojstava monokarboksilnih kiselina. To je zbog činjenice da je jačina dibazičnih kiselina veća od jačine monobazične zbog utjecaja druge skupine karboksila i hidroksila. Štoviše, taj se učinak smanjuje s udaljenosti od lanca ugljikovih atoma.
Dibazične kiseline pokazuju sljedeća svojstva:
- Dekarboksilacija kiseline (na primjer, etandin): HOOC-COOH (t) = HOOC + CO2. Važno je znati da oksalna i malonska kiselina prolaze dekarboksilaciju mnogo lakše od drugih.
- Nastajanje kiselih i srednjih soli: HOOC-RR-COOK ili HOOK-RR-COOK.
- Formiranje potpunih i nekompletnih etera.
- Malonska kiselina može ući u reakcije supstitucije: vodik iz CH2 skupine ugljikovodičnog radikala lako se zamjenjuje s atomima metala.
Soli koje tvore karboksilne kiseline
Soli su organski spojevi koji nastaju zamjenom atoma vodika i hidroksilne skupine karboksilne kiseline karboksilne kiseline s metalom. To jest, organske kiseline u reakcijama s bazama ili anorganskim solima mogu tvoriti soli karboksilnih kiselina. Kemijska svojstva kojima se dobivaju organski spojevi kao što su soli koriste se u kućanstvu za proizvodnju sapuna.
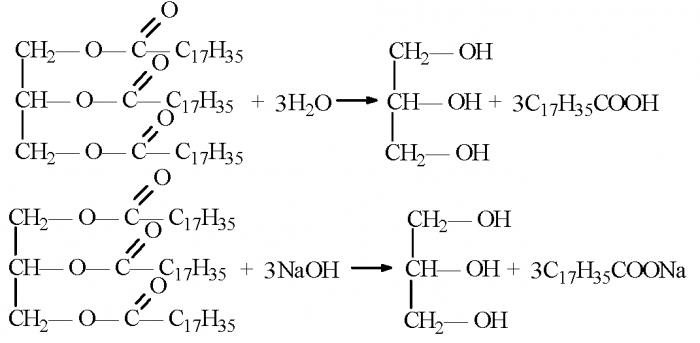
Za sintezu čvrstih i tekućih sapuna najprikladnije su stearinske (oktadekanoične) i palmitinske (heksadekanske) kiseline. Oleic (cis-9-oktadecen) ili miristik (tetradekan kiselina).
Osnova sapuna je reakcija sinteze estera gore navedenih kiselina s kalijevom ili natrijevom soli.
Postupci za proizvodnju karboksilnih kiselina
Postoje mnoge metode i metode za proizvodnju kiselina u skupini COOH, ali se najčešće koriste sljedeće:
- Ekstrakcija iz prirodnih tvari (masti i drugo).
- Oksidacija monoalkohola ili spojeva s COH-skupinom (aldehidi): ROH (RCOH) [O] R-COOH.
- Hidroliza trihaloalkana u alkalijama s međuproduktom mono-alkohola: RCl3 + NaOH = (ROH + 3NaCl) = RCOOH + H20.
- Saponifikacija ili hidroliza estera kiseline i alkohola (esteri): R-COOR '+ NaOH = (R-COONa + R'OH) = R-COOH + NaCl.
- Oksidacija alkana s permanganatom (tvrda oksidacija): R = CH2 [O], (KMnO4) RCOOH.
Vrijednost karboksilnih kiselina za ljude i industriju

Kemijska svojstva karboksilnih kiselina su od velike važnosti za ljudski život. Oni su izuzetno potrebni za tijelo, kao u velikim količinama koje se nalaze u svakoj ćeliji. Metabolizam masti, proteina i ugljikohidrata uvijek prolazi kroz fazu dobivanja jedne ili druge karboksilne kiseline.
Osim toga, karboksilne kiseline se koriste u stvaranju lijekova. Nijedna farmaceutska industrija ne može postojati bez praktične uporabe svojstava organskih kiselina.

Važnu ulogu igraju spojevi s karboksilnom skupinom u kozmetičkoj industriji. Sinteza masti za naknadnu proizvodnju sapuna, deterdženata i kućnih kemikalija temelji se na reakciji esterifikacije s karboksilnom kiselinom.
Kemijska svojstva karboksilnih kiselina odražavaju se u ljudskom životu. Oni su od velike važnosti za ljudsko tijelo, jer se nalaze u velikom broju u svakoj ćeliji. Metabolizam masti, proteina i ugljikohidrata uvijek prolazi kroz fazu dobivanja jedne ili druge karboksilne kiseline.