Kemijska svojstva monohidričnih i polihidroksilnih alkohola
Alkoholi su velika skupina organskih kemikalija. Obuhvaća podrazrede monohidričnih i polihidričnih alkohola, kao i sve tvari kombinirane strukture: aldehidnih alkohola, derivata fenola, bioloških molekula. Ove tvari ulaze u mnoge vrste reakcija i na hidroksilnu skupinu i na atom ugljika koji ga nosi. Ta kemijska svojstva alkohola treba detaljno proučavati.

Vrste alkohola
Supstance alkohola sadrže hidroksilnu skupinu vezanu za noseći ugljikov atom. Ovisno o broju ugljikovih atoma s kojima je povezan nosač C, alkoholi se dijele na:
- primarni (spojen na terminalni ugljik);
- sekundarni (vezan na jednu hidroksilnu skupinu, jedan vodik i dva ugljikova atoma);
- tercijarni (povezan s tri ugljikova atoma i jednom hidroksilnom skupinom);
- mješoviti (polihidrični alkoholi, u kojima postoje hidroksilne skupine u sekundarnim, primarnim ili tercijarnim atomima ugljika).
Također su alkoholi podijeljeni ovisno o količini hidroksilnih radikala na monomatskim i poliatomskim. Prvi sadrži samo jednu hidroksilnu skupinu na atomu koji nosi ugljik, na primjer, etanol. Polihidrični alkoholi sadrže dvije ili više hidroksilnih skupina različitih nosivih ugljikovih atoma.
Kemijska svojstva alkohola: tablica
Najpogodnije je da nam materijal koji nas zanima dostavi kroz tablicu koja odražava opća načela reaktivnosti alkohola.
Reakcijska veza, tip reakcije | reagens | proizvod |
OH komunikacija, supstitucija | Aktivni metal, aktivni metalni hidrid, lužine ili amidi aktivnih metala | alkoholata |
C-O i O-H veza, intermolekularna dehidracija | Alkohol se zagrijava u kiselom okruženju | Jednostavan zrak |
C-O i O-H veza, intramolekularna dehidracija | Alkohol se zagrijava preko koncentrirane sumporne kiseline | Nezasićeni ugljikovodik |
CO veza, supstitucija | Vodikov halogenid, tionil klorid, kvazifosfonijeva sol, fosforni halogenidi | haloalkane |
C-O veza - oksidacija | Donori kisika (kalijev permanganat) s primarnim alkoholom | aldehid |
C-O veza - oksidacija | Donori kisika (kalijev permanganat) sa sekundarnim alkoholom | keton |
Alkoholna molekula | Kisik (spaljivanje) | Ugljični dioksid i voda. |
Reaktivnost alkohola
Zbog prisutnosti u molekuli monohidratnog alkohola ugljikovodični radikal - C-O veza i OH veza - ova klasa spojeva ulazi u brojne kemijske reakcije. Oni određuju kemijska svojstva alkohola i ovise o reaktivnosti tvari. Potonji, pak, ovisi o duljini ugljikovodičnog radikala vezanog za noseći atom ugljika. Što je veća, to je niži polaritet O-H veze, zbog čega će se reakcije koje se odvijaju eliminacijom vodika iz alkohola odvijati sporije. To također smanjuje konstantu disocijacije tvari.
Kemijska svojstva alkohola također ovise o broju hidroksilnih skupina. Jedna smjena elektronske gustoće prema sebi duž sigma veza, što povećava reaktivnost u OH skupini. Budući da ovo polarizira C-O vezu, reakcije s njezinim rupturom su aktivnije u alkoholima, koji imaju dvije ili više OH skupina. Zbog toga je vjerojatnije da će reagirati polihidrični alkoholi, čija su kemijska svojstva brojnija. Također sadrže nekoliko skupina alkohola, zbog čega mogu slobodno reagirati na svaku od njih.
Tipične reakcije monohidričnih i polihidroksilnih alkohola
Tipična kemijska svojstva alkohola manifestiraju se samo u reakciji s aktivnim metalima, njihovim bazama i hidridima, Lewisovim kiselinama. Također su tipične interakcije s vodikovim halidima, fosfornim halidima i drugim komponentama za proizvodnju haloalkana. Alkoholi su također slabe baze, stoga reagiraju s kiselinama, tvoreći halogenide i estere anorganskih kiselina.
eteri se formiraju iz alkohola tijekom intermolekularne dehidracije. Iste tvari ulaze u reakcije dehidrogenacije s nastankom aldehida iz primarnog alkohola i ketona iz sekundarnog. Tercijarni alkoholi ne ulaze u takve reakcije. Također kemijska svojstva etil alkohol (i drugi alkoholi) ostavljaju mogućnost njihove potpune oksidacije kisikom. To je jednostavna reakcija sagorijevanja, praćena otpuštanjem vode ugljični dioksid i malo topline.

Reakcije na vodikovom atomu OH veze
Kemijska svojstva monohidričnih alkohola dopuštaju rupturu OH veze i eliminaciju vodika. Te se reakcije odvijaju u interakciji s aktivnim metalima i njihovim bazama (alkalijama), s hidridima aktivnih metala, kao is Lewisovim kiselinama.
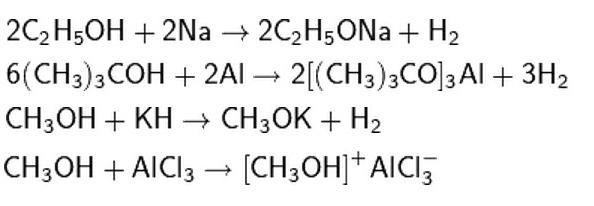
Također alkoholi aktivno reagiraju sa standardnim organskim i anorganskim kiselinama. U tom slučaju reakcijski produkt je ester ili halougljikovodik.
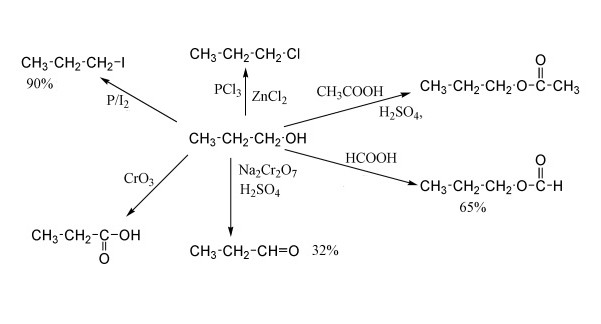
Reakcija sinteze halogen-alkana (pomoću C-O veze)
Haloalkani su tipični spojevi koji se mogu dobiti iz alkohola tijekom nekoliko vrsta kemijskih reakcija. Posebno, kemijska svojstva monohidričnih alkohola omogućuju interakciju s halogenidima, troslojnim i pentavalentnim fosfornim halidima, kvazifosfonijevim solima i tionil kloridom. Također, halogen-alkani iz alkohola mogu se dobiti intermedijarnim putem, to jest, sintezom alkil sulfonata, koji će kasnije ući u reakciju supstitucije.
Primjer prve reakcije s halogenidom vodika prikazan je na gornjoj grafičkoj aplikaciji. Ovdje butil alkohol reagira s klorovodikom u klorbutan. Općenito, klasa spojeva koji sadrže klor i zasićene ugljikovodične radikale naziva se alkil klorid. Nusprodukt kemijske interakcije je voda.
Reakcije s dobivanjem alkil klorida (jodid, bromid ili fluorid) su prilično brojne. Tipičan primjer je interakcija s fosfornim tribromidom, fosfornim pentakloridom i drugim spojevima ovog elementa i njegovih halogenida, perklorida i perfluorida. Oni teče mehanizmom nukleofilne supstitucije. Alkoholi također reagiraju s tionil kloridom kako bi nastali kloralkan i oslobađanje SO2.
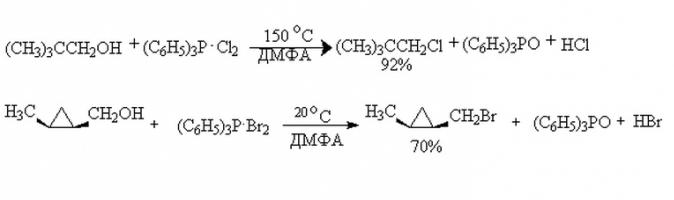
Jasno je da su kemijska svojstva monohidričnih zasićenih alkohola koji sadrže zasićeni radikal ugljikovodika prikazana kao reakcija na donjoj ilustraciji.
Alkoholi lako komuniciraju s kvazifosfonijskom soli. Međutim, ova reakcija je najkorisnija tijekom monomatskih sekundarnih i tercijarnih alkohola. Oni su regioselektivni, omogućuju vam da "ugrađujete" halogenu skupinu u strogo određeno mjesto. Produkti takvih reakcija su dobiveni s visokim masenim udjelom prinosa. A polihidrični alkoholi, čija su kemijska svojstva donekle različiti od onih monohidričnih, mogu se izomerizirati tijekom reakcije. Stoga je teško dobiti ciljni proizvod. Primjer reakcije na slici.
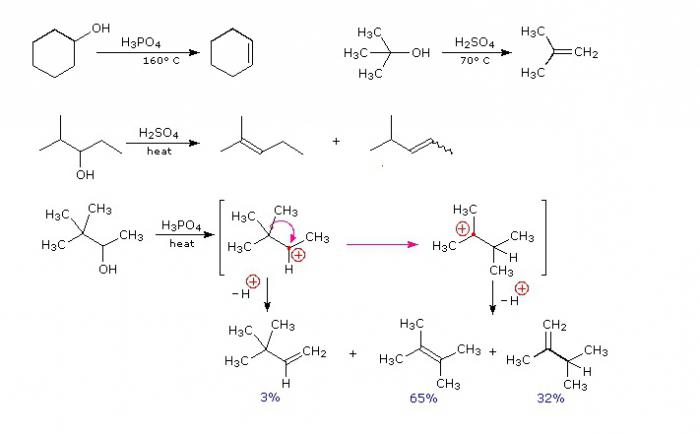
Intramolekularna i intermolekularna dehidracija alkohola
Hidroksilna skupina smještena na atomu koji nosi ugljik može se odcijepiti korištenjem jakih akceptora. Tako nastaju intermolekularne reakcije dehidracije. U interakciji jedne molekule alkohola s drugom u otopini koncentrirana sumporna kiselina molekula vode se odcjepljuje od obje hidroksilne skupine, čiji se radikali kombiniraju da formiraju molekulu etera. Kod intermolekularne dehidracije etanala može se dobiti dioksan - proizvod dehidracije u četiri hidroksilne skupine.
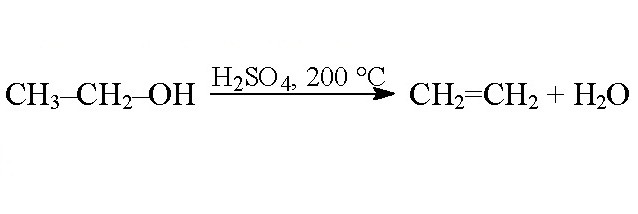
Za intramolekularnu dehidraciju, proizvod je alken.