Kristalna i amorfna tijela: struktura i svojstva
Postoji nekoliko agregatnih stanja u kojima se nalaze sva tijela i tvari. Ovo je:
- plin;
- tekućina;
- plazma;
- krutina.
Ako uzmemo u obzir ukupnu populaciju planeta i prostora, onda je većina tvari i tijela još uvijek u stanju plina i plazme. Međutim, na samoj Zemlji, sadržaj krutih čestica je također značajan. Ovdje ćemo govoriti o njima, saznati što su kristalne i amorfne krutine.
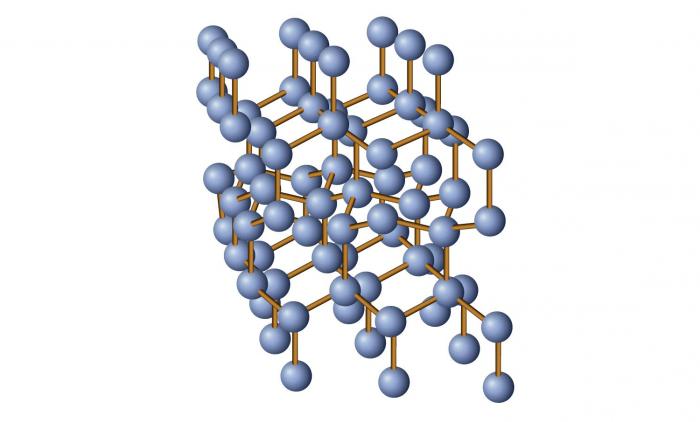
Kristalni i amorfna tijela: opći pojam
Sve krutine, tijela, predmeti se uvjetno dijele na:
- kristal;
- Amorfni.
Razlika između njih je ogromna, jer je osnova jedinice znakovi strukture i manifestiranih svojstava. Ukratko, čvrsti kristali su one tvari i tijela koja imaju određenu vrstu prostora kristalna rešetka to jest, oni imaju sposobnost promjene u određenom smjeru, ali ne u svemu (anizotropija).
Ako su, međutim, karakterizirani amorfni spojevi, tada je njihov prvi znak mogućnost promjene fizičkih karakteristika u svim smjerovima istovremeno. To se naziva izotropija.
Struktura, svojstva kristalnih i amorfnih tijela potpuno su različiti. Ako prva ima jasno ograničenu strukturu koja se sastoji od uređenih čestica u prostoru, onda ona nema red.

Svojstva krutih tvari
Kristalna i amorfna tijela ipak pripadaju jednoj grupi krutina, te stoga imaju sva obilježja tog agregatnog stanja. To znači da će njihova opća svojstva biti sljedeća:
- Mehanička - elastičnost, tvrdoća, sposobnost deformacije.
- Toplinsko - vrelište i tališta, koeficijent toplinskog širenja.
- Električna i magnetska - toplinska i električna vodljivost.
Dakle, razmatrane države posjeduju sva ova obilježja. Pojavljuju se samo u amorfnim tijelima, bit će malo drugačiji nego u kristalnim.
Važna svojstva za industrijske svrhe su mehanička i električna. Sposobnost oporavka od deformacije ili, naprotiv, raspadanja i mrvljenja važna je značajka. Veliku ulogu ima i činjenica da tvar može provesti električnu struju ili nije sposobna za nju.

Kristalna struktura
Ako opišemo strukturu kristalnih i amorfnih tijela, prije svega je potrebno naznačiti vrstu čestica koje ih sastavljaju. U slučaju kristali mogu postojati ioni atoma, atoma, iona (u metalima) (rijetko).
Općenito, ove strukture karakterizira prisutnost strogo uređene prostorne rešetke, koja se formira kao rezultat rasporeda čestica koje tvore tvar. Zamislite li strukturu kristala figurativno, dobijete nešto poput ovoga: atomi (ili druge čestice) su razmaknuti jedan od drugoga na određenim udaljenostima, tako da se dobije idealna ćelija buduće kristalne rešetke. Tada se ova stanica ponavlja mnogo puta i tako se oblikuje cjelokupna struktura.
Glavna značajka je da fizička svojstva u takvim strukturama variraju paralelno, ali ne u svim smjerovima. Ovaj fenomen naziva se anizotropija. To jest, ako djelujete na jedan dio kristala, druga strana možda neće reagirati na njega. Dakle, možete samljeti pola komada soli, ali drugi će ostati netaknut.
Tipovi kristala
Uobičajeno je označiti dvije varijante kristala. Prvi su monokristalne strukture, tj. Kada je sama rešetka 1. Kristalna i amorfna tijela u ovom su slučaju potpuno različita po svojstvima. Uostalom, jedan kristal je karakteriziran anizotropijom u svom čistom obliku. To je najmanja elementarna struktura.
Ako se pojedinačni kristali ponavljaju mnogo puta i kombiniraju se u jedan, onda govorimo o polikristalu. Tada nema govora o anizotropiji, jer orijentacija elementarnih stanica krši opće uređenu strukturu. U tom smislu, polikristali i amorfna tijela su blizu jedan drugome u smislu njihovih fizičkih svojstava.

Metali i legure
Kristalna i amorfna tijela su vrlo blizu jedna drugoj. U to se lako može uvjeriti, kao primjer uzimati metale i njihove legure. Po sebi, oni su pod normalnim uvjetima čvrste tvari. Međutim, na određenoj temperaturi počinju se topiti i dok ne dođe do potpune kristalizacije, ostaju u stanju rastezanja, guste, viskozne mase. A to je već amorfno stanje tijela.
Stoga, strogo govoreći, gotovo svaka kristalna tvar može, pod određenim uvjetima, postati amorfna. Baš kao i potonje tijekom učvršćivanja, ona postaje čvrsto s uređenom prostornom strukturom.
Metali mogu imati različite tipove prostornih struktura, od kojih su najpoznatije i istraživane sljedeće:
- Jednostavna kubična.
- Lice-centered.
- Obemotsentrirovannaya.
Struktura kristala može se temeljiti na prizmi ili piramidi, a njen glavni dio predstavlja:
- trokut;
- paralelogram;
- po kvadratu;
- šesterokut.
Tvar koja ima jednostavnu pravilnu kubičnu rešetku ima idealna izotropna svojstva.

Pojam amorfan
Kristalna i amorfna tijela izvana jednostavna za razlikovanje. Uostalom, potonji se često može zamijeniti s viskoznim tekućinama. Struktura amorfne tvari također se temelji na ionima, atomima, molekulama. Međutim, oni ne tvore uređenu strogu strukturu, pa se zbog toga njihove osobine mijenjaju u svim smjerovima. To jest, oni su izotropni.
Čestice su nasumce raspoređene nasumce. Samo ponekad mogu tvoriti male lokuse, što još uvijek ne utječe na prikazana opća svojstva.
Svojstva sličnih tijela
Oni su identični onima kristala. Razlike su samo u pokazateljima za svako pojedino tijelo. Tako, na primjer, možemo razlikovati takve karakteristične parametre amorfnih tijela:
- čvrstoća;
- gustoća;
- viskoznost;
- duktilnost;
- vodljivost i poluvodičnost.
Često možete ispuniti granične uvjete spojeva. Kristalna i amorfna tijela mogu postati poluamorfna.
Također je zanimljivo obilježje dotične države, koja se manifestira oštrim vanjskim utjecajem. Dakle, ako je amorfno tijelo podvrgnuto oštrom udaru ili deformaciji, tada je sposobno ponašati se kao polikristal i dijeliti se na male komade. Međutim, ako se tim vremenima daju ti dijelovi, oni će se uskoro ponovno ujediniti i pretvoriti u viskozno tekuće stanje.

Ovo stanje spojeva nema specifičnu temperaturu na kojoj dolazi do faznog prijelaza. Ovaj proces se uvelike proširuje, ponekad i desetljećima (npr. Razgradnja polietilena niskog tlaka).
Primjeri amorfnih tvari
Postoje mnogi primjeri takvih tvari. Odredimo neke najočiglednije i često zadovoljene.
- Čokolada je tipična amorfna tvar.
- Smole, uključujući fenol-formaldehid, sve plastike.
- Amber.
- Staklo bilo kojeg sastava.
- Bitumen.
- Tar.
- Vosak i drugi.
Amorfno tijelo nastaje kao rezultat vrlo sporog kristaliziranja, tj. Povećanja viskoznosti otopine pri smanjenju temperature. Često je takve tvari teško nazvati krutim, već se oni odnose na guste tekuće tekućine.
Spojevi koji uopće ne kristaliziraju tijekom solidifikacije imaju posebno stanje. Nazivaju se naočalama, a stanje - staklastim.
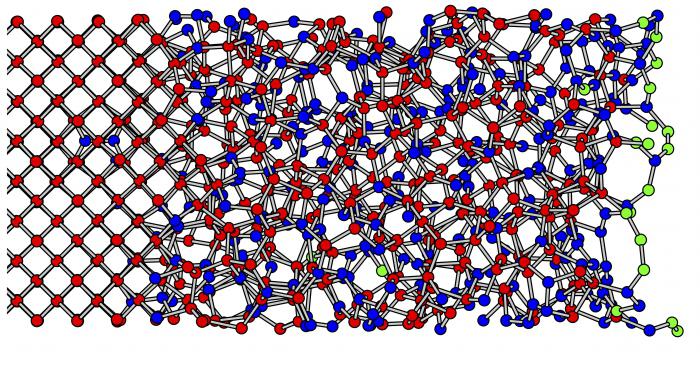
Staklene tvari
Svojstva kristalnog i amorfnog tijela slična su, kako smo saznali, zbog njihovog zajedničkog podrijetla i jedinstvene unutarnje prirode. Ali ponekad se zasebno smatraju posebnim stanjem tvari, nazvanim staklastim. To je homogena mineralna otopina koja kristalizira i stvrdnjava bez stvaranja prostornih rešetki. To jest, ona ostaje izotropna u smislu promjene svojstava uvijek.
Na primjer, uobičajeno prozorsko staklo nema točnu vrijednost točke taljenja. Samo s povećanjem ovog pokazatelja polako se topi, omekšava i pretvara u tekuće stanje. Ako je učinak zaustavljen, tada će se odvijati obrnuti proces i početi skrućivanje, ali bez kristalizacije.
Takve tvari su visoko cijenjene, staklo je danas jedan od najčešćih i najtraženijih građevinskih materijala širom svijeta.