Le Chatelierov princip u kemiji
U nekim slučajevima, tvari koje nastaju reakcijom ili međusobno djeluju ili se razgrađuju, a zatim se u sustavu istovremeno odvijaju dvije reakcije: izravne (nastaju reakcijski produkti) i obrnute (novije sintetizirane početne tvari). U slučaju podudaranja brzina izravnih i inverznih procesa u razmatranom sustavu, dolazi do ravnoteže, koja se naziva kemijska. To je dinamička ravnoteža, jer se sama reakcija ne zaustavlja, već se istu količinu tvari oblikuje i razgrađuje istovremeno. S konstantnom temperaturom i tlakom, ova situacija može potrajati duže vrijeme. U grafičkom obliku, prikazan je u nastavku. Pod ekvivalentnom brzinom podrazumijeva se određena konstanta, koja je istodobno jednaka brzini izravne i obrnute reakcije.
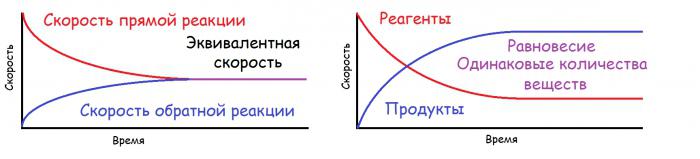
Princip pristranosti kemijske ravnoteže
Princip pomaka (pomaka) ravnoteže otkrio je Le Chatelier 1884. godine. Kasnije ga je sažeo Karl Ferdinand Brown (1887.). Dakle, sada ima ime blizanca - načelo Le Chatelier-Brown. Ovaj se zakon koristi kako u kemiji, tako iu termodinamici, elektrodinamici, ekologiji i biokemiji. Postoji mnogo formulacija, ali bit svakog od njih svodi se na sljedeće: "Kada se utjecaj vrši na sustav u ravnoteži, kemijska ravnoteža se pomiče kako bi se kompenzirala ta promjena (tj. Sustav će pokušati vratiti ravnotežu) ”. Opisano načelo može se jasno pokazati pomoću sljedećeg sustava. Na fiksni nosač je pričvršćena opruga. U mirovanju, ovaj sustav je u ravnoteži. Ako se opruga rastegne, tada će se ravnoteža pomaknuti prema vanjskom utjecaju. Međutim, sustav također povećava protivljenje. I u jednom trenutku sile opozicije i vanjskog utjecaja postaju jednake jedna drugoj, zbog čega nastaje novo stanje ravnoteže.
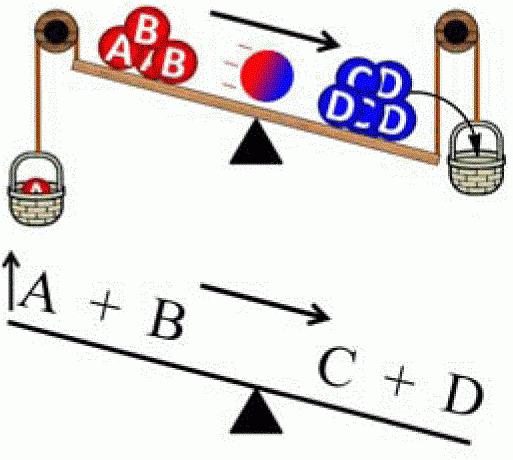
Načelo Le Chateliera može se koristiti samo za sustave u ravnoteži, inače će rezultati analize biti netočni. Postoje tri glavna parametra čija promjena uzrokuje pomak u kemijskoj ravnoteži: tlak, temperatura i koncentracija kemikalija.
temperatura
Promjena temperature je najčešći uzrok pomaka kemijske ravnoteže, što je i razumljivo, jer je taj faktor mnogo lakše utjecati nego, na primjer, tlak. Ovdje valja spomenuti da su reakcije podijeljene u dva tipa toplinskim učinkom. Među njima su: egzotermna (s toplinom) i endotermna (s apsorpcijom). Kako će se promijeniti kemijska ravnoteža u ovom slučaju? Princip Le Chateliera se u ovom slučaju svodi na sljedeće: s povećanjem temperature, ravnoteža se pomiče prema reakciji koja se odvija apsorpcijom topline, a kada se smanjuje, u suprotnom smjeru. Dakle, ako za reakciju prikazanu ispod za podizanje temperature, ravnoteža će se pomaknuti na desnu stranu.
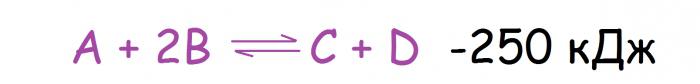
Većina izravnih reakcija su egzotermne, a reverzne reakcije su endotermne (to nije pravilo, već opažanje iz kojeg se mogu naći mnogi izuzeci).
tlak
Kako se tlak mijenja, sljedeći parametar sustava se transformira - njegov volumen (povećava se ili smanjuje), tako da učinak korištenja ovog parametra ima osobito jak učinak na sustave u kojima su prisutni plinovi. U ovom slučaju, načelo kemijska ravnoteža je kako slijedi. Ako se tlak u sustavu poveća, tada se ravnoteža pomiče prema smanjenju broja molekula plina, a kako se tlak smanjuje, ravnoteža se pomiče u suprotnom smjeru. Ako se broj molekula plina ne mijenja tijekom reakcije, tada se ravnoteža ne mijenja s promjenom tlaka, kao npr. U sljedećoj reakciji.
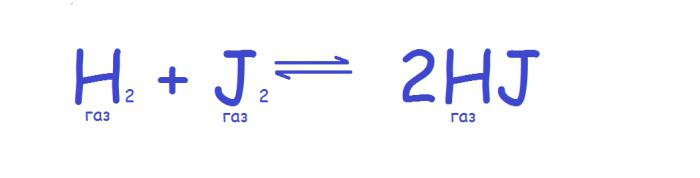
Međutim, u praksi se ovo načelo odnosi samo na idealne plinove, budući da svi stvarni plinovi imaju različitu stlačivost. Stoga, čak i ako broj molekula plina ostaje nepromijenjen, ravnoteža može ovisiti o tlaku. U praksi će to biti vidljivo kada visoki tlakovi. U slučaju tekućih i krutih tvari, promjena tlaka zapravo ne utječe na ravnotežu zbog malih količina koje zauzimaju takve tvari. Pri razmatranju mješovitih sustava uzimaju se u obzir samo molekule plina.
Ravnotežni pomak u sustavu kao rezultat promjene koncentracije bilo koje tvari uključene u reakciju
Prilikom promjene koncentracije tvari, načelo Le Chatelier funkcionira na sljedeći način. Povećanjem koncentracije produkata reakcije, ravnoteža se pomiče prema obrnutoj reakciji, a pri smanjenju količine nastalih tvari ravnoteža se pomiče u suprotnom smjeru.
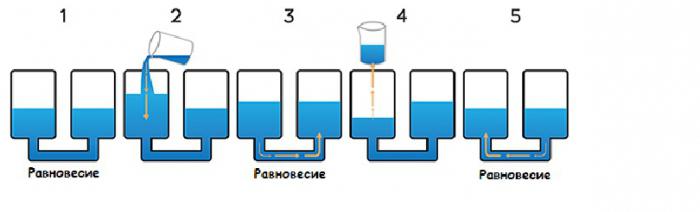
Što se događa ako dodate inertni plin
Možete mijenjati volumen sustava ne samo komprimiranjem ili slabljenjem tlaka, već i dodavanjem inertnog plina koji neće reagirati. Što će se dogoditi sa sustavom kada mu se doda helij? U stvari, najvjerojatnije, ništa se neće dogoditi, budući da se omjer tvari koje sudjeluju u reakciji neće promijeniti, a proces nije bitan za ukupni tlak sustava, već za djelomične za svaku komponentu.
Učinak katalizatora
Količina katalizatora i njegova prisutnost općenito nemaju učinka na pomicanje kemijske ravnoteže. To se događa s obzirom na činjenicu da ovaj element jednako ubrzava i izravnu i obrnutu reakciju, održavajući ravnotežu u sustavu nepromijenjenom.
Način proučavanja kemijske ravnoteže
Detaljno razmatranje kemijske ravnoteže vrlo je važno za potpuno razumijevanje procesa. Jedna od najčešće korištenih tehnika je tzv. Ravnotežna metoda zamrzavanja. Dakle, postoji brzina sustav hlađenja u uravnoteženom stanju. Ravnoteža jednostavno nema vremena za promjenu, a na niskim temperaturama brzina većine procesa usporava se gotovo do nule. Zbog toga je moguće potpuno analizirati sastav smjese na bilo kojoj temperaturi (koncentracija tvari uključenih u reakciju, pri nultom stupnju, će odgovarati broju komponenti na temperaturi na kojoj je počelo smanjenje). Ovo iskustvo se provodi nekoliko puta s reakcijama koje se odvijaju u oba smjera.
Postoji li potpuna nepovratnost?
Nemoguće je potpuno pomak kemijske ravnoteže u jednom smjeru. Čak i uz prividni apsolutni pomak, uvijek će postojati mali broj molekula koje će reagirati.

U praksi, gotovo sve reakcije su reverzibilne, i koliko će taj učinak biti vidljiv, često ovisi o temperaturi (često je ravnoteža jednostavno snažno pomaknuta u jednom smjeru, tako da postaje vidljiva tek kada se uvjeti promijene). To je zbog ove prevalencije reverzibilne kemijske reakcije proučavanje ravnoteže je posebno važno.
Primjeri sinteza u kojima se kemijska ravnoteža pomiče tijekom proizvodnje
U proizvodnji se kemijska ravnoteža obično pomiče u smjeru izravne reakcije da bi se dobili produkti reakcije. Postoje mnogi primjeri takvih sinteza: dobivanje amonijaka sumporni oksid (VI), dušikov oksid (II), itd.