Organske kiseline. Funkcionalna skupina organskih kiselina
Veliki broj spojeva poznatih suvremenom svijetu su organske kiseline. U prirodi se dobivaju uglavnom od šećera kao rezultat složenih biokemijskih reakcija. Njihova uloga u svim životnim procesima je neprocjenjiva. Na primjer, u biosintezi glikozida, amino kiselina, alkaloida i drugih biološki reaktivnih tvari; u metabolizmu ugljikohidrata, masti i proteina ... Postoji mnogo vitalnih procesa koji uključuju organske kiseline.

Što je u njima posebno? Organske kiseline postižu jedinstvene kemijske i biološke osobine zbog svog elementarnog i funkcionalnog sastava molekula. Određeni slijed kombinacije atoma različite prirode i specifičnosti njihove kombinacije daju supstanci individualne osobine i osobitosti interakcije s drugima.
Kvalitativni sastav organskih tvari
Glavna opeka, vrsta monometra svih živih bića, je ugljik, ili, kako se još naziva, ugljik. Iz njega su izgrađeni svi “kosturi” - osnovne strukture, kosturi - organskih spojeva i kiselina. Vodik je drugi po stupnju obilja, a vodik je još jedno ime elementa. On ispunjava karbonske valencije slobodnim od vezivanja s drugim atomima, dajući volumen i gustoću molekula.
Treći je kisik, ili kisik, kombinira se s ugljikom u skupinama atoma, dajući jednostavnim alifatskim ili aromatičnim tvarima sasvim nova svojstva, na primjer, oksidacijsku sposobnost. Nadalje, u nizu obilja - dušika, njegov je doprinos svojstvima organskih kiselina poseban, postoji posebna klasa spojeva koji sadrže amino. Također u organski spojevi sumpor, fosfor, halogene i neki drugi elementi prisutni su u mnogo manjim količinama.
U posebnoj klasi i druge su označene. organska tvar. Nukleinske kiseline su biološki polimeri koji sadrže fosfor i dušik i sastavljeni su od monomera - nukleotida - koji čine najsloženije strukture DNA i RNA.
Opravdanost kemijske individualnosti
Odlučujući čimbenik za razliku od drugih tvari je prisutnost u spoju takve asocijacije atoma, koja ima strogi slijed međusobnog vezivanja i nosi neku vrstu genetski kod klasa kao funkcionalna skupina organskih kiselina. Zove se karboksil, sastoji se od jednog ugljikovog atoma, vodika i dva kisika, te, zapravo, kombinira karbonilne (-C = O) i hidroksilne (-OH) skupine.
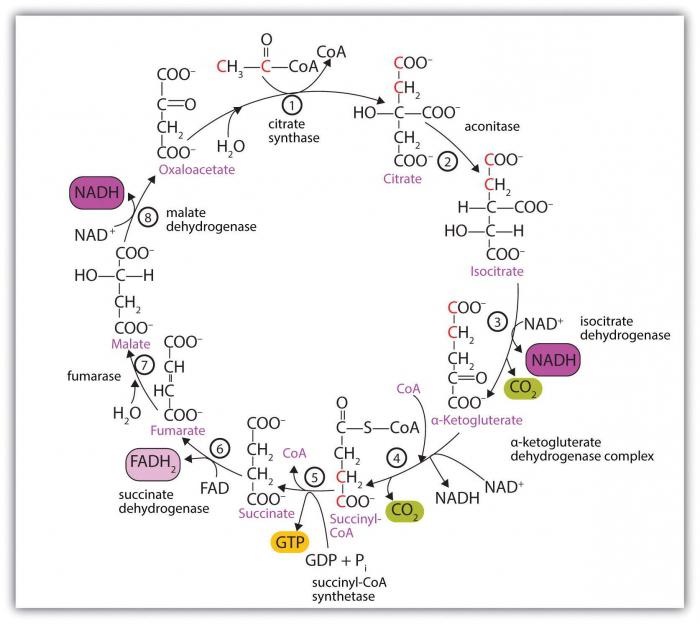
Komponente međusobno djeluju na elektroničkoj razini, generirajući pojedinačna svojstva kiselina. Konkretno, reakcije adicije karbonila nisu svojstvene njima, a sposobnost da se daje proton je nekoliko puta viša od one u alkoholima.
Strukturne značajke
Što se događa na elektroničkoj razini međusobnog utjecaja u funkcionalnoj skupini razreda organske kiseline? Ugljikov atom ima djelomično pozitivan naboj zbog povlačenja gustoće veze na kisik, čija je sposobnost držanja mnogo veća. Kisik iz hidroksilnog dijela ima nerazdvojeni par elektrona, koji sada počinje privlačiti ugljik. Time se smanjuje gustoća veze kisik-vodik, zbog čega vodik postaje mobilniji. Disocijacija kiselinskog tipa postaje moguća za spoj. Smanjenje pozitivnog naboja ugljika uzrokuje prekid protoka procesa spajanja, kao što je već spomenuto.
Uloga određenih fragmenata
Svaka funkcionalna skupina ima pojedinačna svojstva i daje im supstancu koja sadrži. Prisutnost nekoliko u jednoj isključuje mogućnost davanja jedne ili druge reakcije, koja se prethodno zasebno razlikovala od specifičnih fragmenata. To je važna značajka koja karakterizira organsku kemiju. Kiseline mogu imati skupine koje sadrže dušik, sumpor, fosfor, halogene itd.
Klasa karboksilne kiseline
Najpoznatija skupina tvari iz cijele obitelji. Ne biste trebali pretpostaviti da su samo spojevi ove klase sve organske kiseline. Predstavnici ugljika su najveća skupina, ali ne i jedina. Postoje, na primjer, sulfonske kiseline, one imaju drugi funkcionalni fragment. Od njih, poseban status obilježeni su aromatskim derivatima, koji su aktivno uključeni u kemijsku proizvodnju fenola.

Postoji još jedna značajna klasa koja pripada takvom dijelu kemije kao organska tvar. Nukleinske kiseline su odvojene i zahtijevaju individualno razmatranje i opis spoja. O njima je gore spomenuto.
Predstavnici ugljika organska tvar sadrže u svom sastavu karakterističnu funkcionalnu skupinu. To se naziva karboksil, specifičnosti njegove elektroničke strukture opisane ranije. Upravo funkcionalna skupina određuje prisutnost jakih kiselih svojstava, zahvaljujući protonu vodika koji se lako odvaja tijekom disocijacije. Slab od ovog raspona je samo acetat (octena).
Klasifikacija karboksilne kiseline
Prema tipu strukture ugljikovodičnog skeleta razlikuju se alifatski (pravocrtni) i ciklički. Na primjer, propionska, heptanska, benzojeva, trimetilbenzoična karboksilna organska kiselina. Prisutnošću ili odsutnošću višestrukih veza - ograničavajućih i nezasićenih - ulje, octena, akrilna, heksenska, itd. Ovisno o duljini kostura, postoje niže i više (masne) karboksilne kiseline, kategorija potonjeg počinje s lancem od deset ugljikovih atoma. 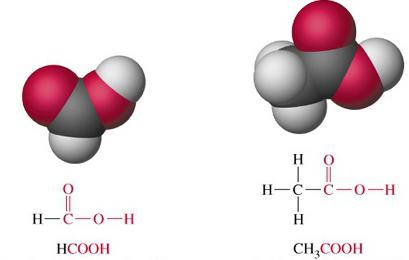
Kvantitativni sadržaj strukturne jedinice, kao što je funkcionalna skupina organskih kiselina, također je načelo klasifikacije. Postoje jedno-, dvo-, tro- i polibazične. Na primjer, mravlji ugljik kiselina, oksalna, limun i drugi. Predstavnici koji sadrže, osim glavne skupine, specifične skupine nazivaju se heterofunkcionalnima.
Moderna nomenklatura
Danas u kemijskoj znanosti postoje dva načina za imenovanje spojeva. Racionalna i sustavna nomenklatura ima, u velikoj mjeri, ista pravila, ali se razlikuju u pojedinostima sastavljanja imena. Povijesno gledano, prisutnost trivijalnih "imena" spojeva koji su dani supstancama, na temelju njihovih inherentnih kemijskih svojstava, biti u prirodi i drugim trenucima. Na primjer, butanska kiselina se naziva maslačna kiselina, propenska kiselina se naziva akrilna kiselina, diureidooctena kiselina se naziva alantoična kiselina, pentanska kiselina se zove valerijanska kiselina, itd. Neki od njih sada se mogu koristiti u racionalnoj i sustavnoj nomenklaturi.
Fazni algoritam
Način izgradnje naziva tvari, uključujući i organske kiseline, je sljedeći. Prvo morate pronaći najdulji lanac ugljikovodika i brojiti ga. Prvi broj bi trebao biti u neposrednoj blizini grananja kraja kako bi supstituenti vodikovih atoma u kosturu dobili najmanji lokant - brojeve koji ukazuju na broj ugljikovih atoma s kojima su povezani.
Zatim morate otkriti glavnu funkcionalnu skupinu, a zatim identificirati druge, ako ih ima. Dakle, ime se sastoji od: navedenih abecednim redom i supstituenata s odgovarajućom lokantom, glavni dio govori o duljini ugljikova skeleta i njegovoj zasićenosti vodikovim atomima; Na primjer, za karboksil je to "-s", a na kraju je napisana riječ acid. Etan, metandioična, propenska, butinska kiselina, hidroksi octena kiselina, pentandioid, 3-hidroksi-4-metoksibenzoeva, 4-metilpentan i tako dalje.
Glavne funkcije i njihovo značenje
Mnoge kiseline, organske i anorganske, od neprocjenjive su vrijednosti za ljude i njihove aktivnosti. Djelujući izvana ili nastali iznutra, oni pokreću mnoge procese, sudjeluju u biokemijskim reakcijama, osiguravaju ispravno funkcioniranje ljudskog tijela, te ga koriste iu mnogim drugim područjima.

Klorovodična (ili klorovodična kiselina) osnova je želučanog soka i neutralizator većine nepotrebnih i opasnih bakterija u gastrointestinalnom traktu. Sumporna kiselina je nezamjenjiva sirovina u kemijskoj industriji. Još je značajniji organski dio predstavnika ove klase - mliječni, askorbinski, octeni i mnogi drugi. Kiseline mijenjaju pH probavnog sustava u alkalnom smjeru, što je neophodno za održavanje normalne mikroflore. U mnogim drugim aspektima, oni imaju nezamjenjiv pozitivan učinak na ljudsko zdravlje. Predstaviti industriju bez uporabe organskih kiselina je apsolutno nemoguće. Sve to funkcionira samo zahvaljujući njihovim funkcionalnim skupinama.