Kisik: kemijska svojstva elementa
Jedan od najvažnijih elemenata na našem planetu je kisik. Kemijska svojstva ove tvari omogućuju joj sudjelovanje u biološkim procesima, a povećana aktivnost čini kisik značajnim sudionikom u svim poznatim kemijskim reakcijama. U slobodnom stanju ova tvar je prisutna u atmosferi. U vezanom stanju, kisik je uključen u sastav minerala, stijena, složenih tvari koje čine različite žive organizme. Ukupna količina kisika na Zemlji procjenjuje se na 47% ukupne mase našeg planeta.
Oznaka kisika
U periodičnom sustavu kisik zauzima osmu ćeliju ove tablice. Njezino međunarodno ime je oxigenium. U kemijskim zapisima označava se latiničnim slovom "O". U prirodnom okruženju, atomski kisik se ne pojavljuje, njegove se čestice kombiniraju tako da tvore par molekula plina, čija je molekularna težina 32 g / mol.
Zrak i kisik
Zrak je mješavina nekoliko plinova čestih na Zemlji. Najviše u zračnoj masi dušika - 78,2% po volumenu i 75,5% po masi. Kisik zauzima samo drugo mjesto po količini - 20,9%, a po težini - 23,2%. Treće mjesto zauzimaju plemeniti plinovi. Preostale nečistoće - ugljični dioksid, vodena para, prašina i tako dalje - zauzimaju samo dio postotka ukupne zračne mase. 
Cijela masa prirodnog kisika je mješavina triju izotopa - 16O, 17O, 18O. Postotak tih izotopa u ukupnoj masi kisika iznosi 99,76%, 0,04% i 0,2%.
Fizikalna i kemijska svojstva kisika
Jedna litra zraka u normalnim uvjetima teži 1,293 g. Kada temperatura padne na -140 ° C, zrak postaje bezbojna prozirna tekućina. Usprkos niskoj točki vrenja, zrak se može održavati u tekućem stanju čak i na sobnoj temperaturi. Da biste to učinili, tekućina se mora staviti u tzv Brod Dewar. Uranjanje u tekući kisik iz temelja mijenja uobičajena svojstva predmeta.  Etilni alkohol i mnogi plinovi postaju tvrdi predmeti, živa dobiva tvrdoću i savitljivost, a gumena loptica gubi svoju elastičnost i mrvi se pri najmanjem udaru.
Etilni alkohol i mnogi plinovi postaju tvrdi predmeti, živa dobiva tvrdoću i savitljivost, a gumena loptica gubi svoju elastičnost i mrvi se pri najmanjem udaru.
Kisik je topiv u vodi, iako u malim količinama - morska voda sadrži 3-5% kisika. Ali čak i tako mala količina tog plina označila je početak postojanja riba, školjki i raznih morskih organizama koji primaju kisik iz vode kako bi podržali svoje vlastite procese za održavanje života.
Struktura atoma kisika
Opisana svojstva kisika prvenstveno su posljedica unutarnje strukture ovog elementa. 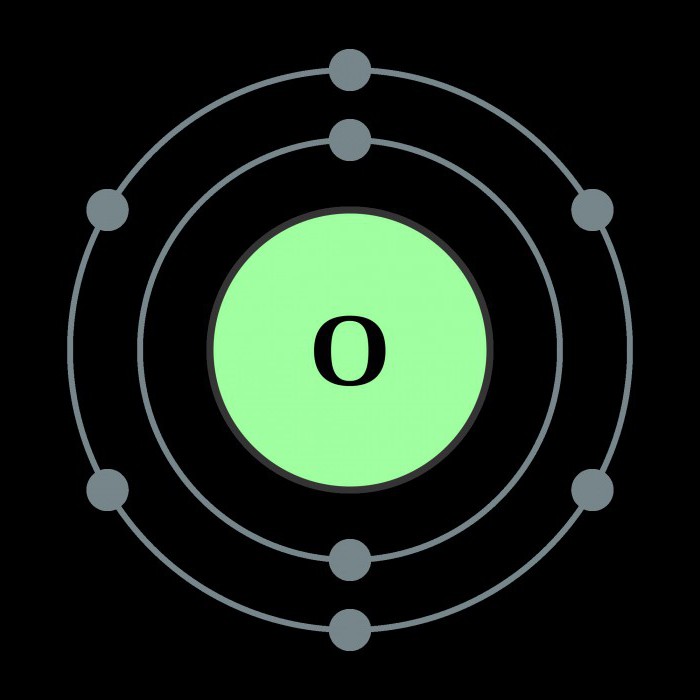
Kisik pripada glavnoj podskupini šeste skupine elemenata periodičkog sustava. U vanjskom elektronskom oblaku elementa nalazi se šest elektrona, od kojih četiri zauzimaju p-orbitale, a preostala dva su na s-orbitalima. Ta unutarnja struktura uzrokuje velike troškove energije, s ciljem razbijanja elektroničkih veza - atomu kisika lakše je posuditi dva nestala elektrona u vanjsku orbitu nego odustati od svojih šest. Stoga je kovalentnost kisika u većini slučajeva jednaka dva. Zahvaljujući dva slobodna elektrona, kisik lako stvara dijatomejske molekule koje karakterizira visoka čvrstoća veze. Samo pri primijenjenoj energiji većoj od 498 J / mol molekule se dezintegriraju, a nastaje atomski kisik. Kemijska svojstva ovog elementa omogućuju mu da reagira sa svim poznatim tvarima, osim helija, neona i argona. Brzina interakcije ovisi o temperaturi reakcije i prirodi tvari. 
Kemijska svojstva kisika
Kod različitih tvari kisik ulazi u reakciju stvaranja oksida, a te su reakcije karakteristične za metale i nemetale. Spojevi kisika s metalima nazivaju se osnovni oksidi - magnezij oksid i kalcijev oksid su klasičan primjer. Interakcija metalnih oksida s vodom dovodi do stvaranja hidroksida koji potvrđuju aktivna kemijska svojstva kisika. Kod nemetala ova tvar tvori kisele okside - na primjer, sumpor trioksid SO 3. Kada ovaj element stupa u interakciju s vodom, ispada da sumporna kiselina.
Kemijska aktivnost
S velikom većinom elemenata, kisik izravno djeluje. Iznimke su zlato, halogeni i platina. Interakcija kisika s određenim tvarima značajno se ubrzava u prisutnosti katalizatora. Na primjer, smjesa vodika i kisika u prisutnosti platine reagira čak i na sobnoj temperaturi. Uz zaglušujuću eksploziju, smjesa se pretvara u običnu vodu, od koje je važan dio kisika. Kemijska svojstva i visoka aktivnost elementa objašnjavaju oslobađanje velike količine svjetlosti i topline, tako da se kemijske reakcije s kisikom često nazivaju spaljivanjem. 
Izgaranje u čistom kisiku odvija se mnogo intenzivnije nego u zraku, iako će količina topline koja se oslobađa tijekom reakcije biti približno ista, ali zbog odsutnosti dušika, proces se odvija mnogo brže, a temperatura izgaranja postaje veća.
Proizvodnja kisika
Godine 1774, engleski znanstvenik D. Svećenik je pustio nepoznati plin iz reakcije razgradnje živinog oksida. No, znanstvenik nije povezao otpušteni plin s već poznatom tvari koja ulazi sastav zraka. Samo nekoliko godina kasnije, veliki Lavoisier je proučavao fizikalno-kemijska svojstva kisika dobivenog u ovoj reakciji i dokazao svoj identitet s plinom koji tvori zrak. U suvremenom svijetu kisik se dobiva iz zraka. U laboratorijima koristim industrijski kisik, koji se dobavlja pomoću cilindara pod tlakom od oko 15 MPa. Čisti kisik se također može dobiti u laboratorijskim uvjetima, a standardna metoda za njegovu proizvodnju je termička razgradnja kalijevog permanganata, koja se odvija prema formuli:
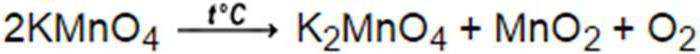
Proizvodnja ozona
Ako struja prolazi kroz kisik ili zrak, u atmosferi će se pojaviti karakterističan miris koji najavljuje pojavu nove tvari - ozona. Ozon se također može dobiti iz kemijski čistog kisika. Formiranje ove tvari može se izraziti formulom:
20 = 2O3
Ta se reakcija ne može odvijati samostalno - za njezin uspješan završetak potrebna je vanjska energija. No, obrnuto pretvaranje ozona u kisik dolazi spontano. Kemijska svojstva kisika i ozona uvelike se razlikuju. Ozon se razlikuje od gustoće kisika, točke tališta i točke vrenja. U normalnim uvjetima ovaj plin je plav i ima karakterističan miris. Ozon ima veću električnu vodljivost i topljiviji je u vodi nego kisik. Kemijska svojstva ozona objašnjavaju se procesom njegovog raspada - tijekom razgradnje molekule ove tvari formira se dijatomejska molekula kisika plus jedan slobodni atom tog elementa, koji agresivno reagira s drugim tvarima. Na primjer, poznata reakcija interakcije ozona i kisika: 6Ag + O3 = 3Ag2O
Ali obični kisik ne kombinira se sa srebrom, čak i na visokim temperaturama. 
U prirodi, aktivni raspad ozona je ispunjen formiranjem tzv ozonske rupe koji ugrožavaju životne procese na našem planetu.