Fizikalno-kemijska svojstva toluena, reakcijske jednadžbe
Toluen je metilbenzen, koji je bezbojna tekućina koja pripada klasi arena, koji su organski spojevi s aromatičnim sustavom u kompoziciji.
Ključna značajka ove tvari može se smatrati njezinim specifičnim mirisom. Međutim, to nije jedina "razlikovna značajka" tvari. Toluen ima mnoga svojstva i karakteristike, a sve ih treba ukratko opisati.

Malo povijesti
Kemijska svojstva toluena počela su se proučavati prije manje od 200 godina, kada su prvi put dobivena. Supstancu je 1835. godine otkrio francuski ljekar i kemičar Pierre Joseph Pelletier. Znanstvenici su tijekom destilacije smole bora dobili toluen.
Tri godine kasnije, francuski fizikohemičar Henri Saint-Claire Deville izolirao je tu tvar iz melema, koju je donio iz kolumbijskog grada Tolu. U čast ovog pića, zapravo, veza i dobio svoje ime.
Opće informacije
Što je s karakteristikama i kemijskim svojstvima toluena? Tvar je hlapljiva pokretna tekućina jakog mirisa. Ima blagi narkotički učinak. Reagira s neograničenom količinom ugljikovodika, u interakciji s eterima i esterom, s alkoholima. Ne miješa se s vodom.
Karakteristike su sljedeće:
- Tvar je označena formulom C7H8.
- Njegova molarna masa je 92,14 g / mol.
- Gustoća je 0,86694 g / cm3.
- Tališta i vrelišta su −95 i 110,6.
- Specifična toplina isparavanja je 364 kJ / kg.
- Temperatura kritičnog faznog prijelaza je 320 ° C.
Ova tvar je također zapaljiva. Izgorio je zadimljeni plamen.
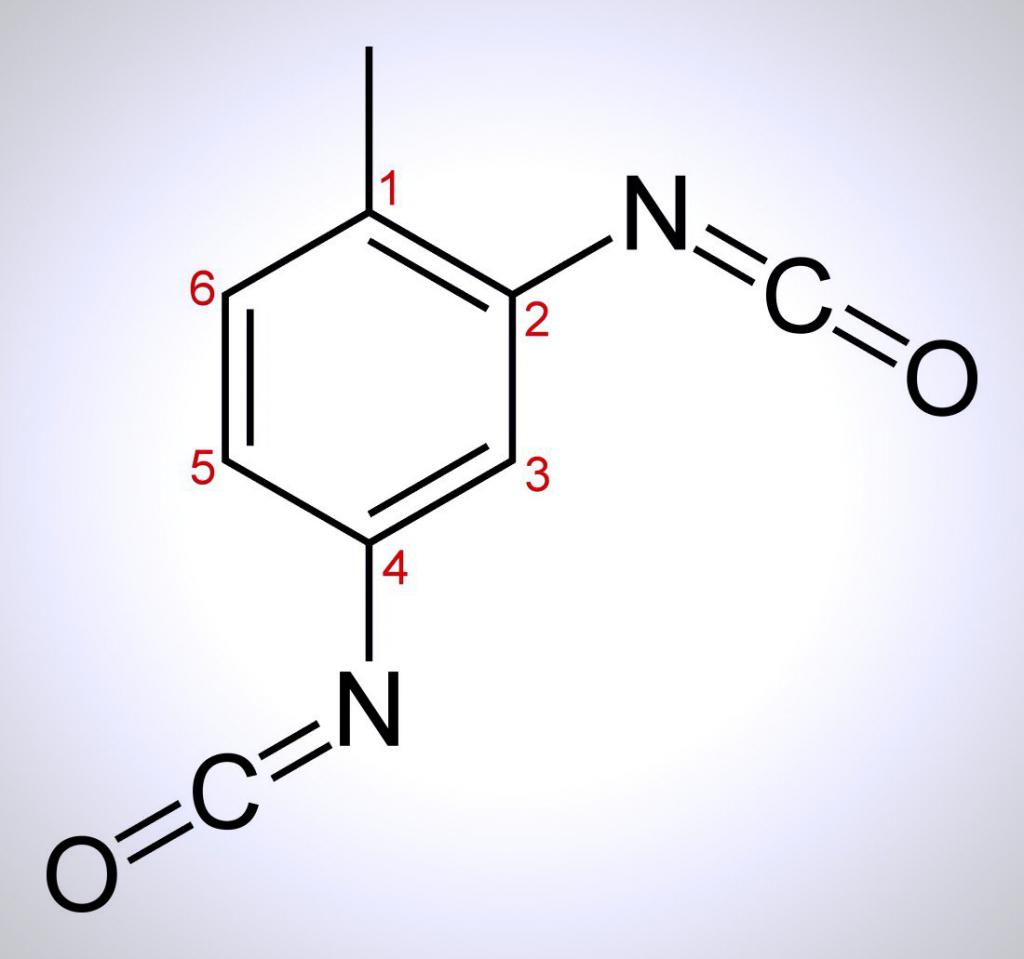
Osnovna kemijska svojstva
Toluen je tvar koja je karakterizirana reakcijama elektrofilne supstitucije. Pojavljuju se u tzv. Aromatskom prstenu, pokazujući abnormalno visoku stabilnost. Ove reakcije se odvijaju uglavnom u para i orto položajima u odnosu na metilnu skupinu -CH3.
Odnosi se na kemijska svojstva toluena, reakciju ozonolize i dodavanje (hidrogeniranje). Pod utjecajem određenih oksidacijskih sredstava, metilna skupina postaje karboksil. Najčešće se u tu svrhu koristi alkalna otopina kalijevog permanganata ili nekoncentrirana. dušična kiselina.
Također je vrijedno spomenuti da se toluen može spontano zapaliti. Za to je potrebna temperatura od 535 ° C. Bljesak se događa na 4 ° C.

Nastajanje benzojeve kiseline
Sposobnost tvari o kojoj se raspravlja da sudjeluje u tom procesu je također zbog njezinih kemijskih svojstava. Toluen, koji reagira s jakim oksidirajućim sredstvima, tvori najjednostavniju monobaznu benzojevu karboksilnu kiselinu koja pripada aromatičnoj seriji. Njegova formula je C6H5COOH.
Kiselina ima oblik bijelih kristala koji se dobro otapaju u dietil eteru, kloroformu i etanolu. Dobiva se sljedećim reakcijama:
- Toluen i kalijev permanganat međusobno djeluju u kiselom okolišu. Formula je kako slijedi: 5C6H5CH3 + 6KMnO4 + 9H2S04 → 5C6H5COOH + 6MnS04 + 3K2S04 + 14H2O.
- Toluen i kalijev permanganat međusobno djeluju u neutralnom okruženju. Formula je kako slijedi: C6H5CH3 + 2KMnO4 → C6H5COOK + 2MnO2 + KOH + H20.
- Toluen, interagirajući u svjetlu s halogenima, energetski oksidirajući agensi. Pojavljuje se prema formuli: C6H5CH3 + X2 → C6H5CH2X + HX.
Benzojeva kiselina dobivena kao rezultat ovih reakcija koristi se u mnogim područjima. Uglavnom se koristi za dobivanje reagensa - benzoil klorida, plastifikatora benzoata, fenola.
Također se koristi u konzerviranju. Aditivi E213, E212, E211 i E210 izrađeni su na bazi benzojeve kiseline. On blokira enzime i usporava metabolizam, inhibira rast kvasca, plijesni i bakterija.
A benzojeva kiselina se koristi u medicini za liječenje kožnih bolesti i kao ekspektorans.

Prijem tvari
Reakcijske jednadžbe koje pokazuju gore navedena kemijska svojstva toluena nisu sve što bih htio uzeti u obzir. Važno je govoriti o procesu dobivanja ove tvari.
Toluen je proizvod industrijske prerade benzinskih frakcija ulja. To se također naziva katalitički reforming. Tvar se izolira selektivnom ekstrakcijom, nakon čega se provodi destilacija - smjesa se odvaja protustrujnim prijenosom topline i mase između tekućine i pare.
Često se taj proces zamjenjuje katalitičkom dehidrogenacijom heptana. To je organski alkan s formulom CH3 (CH2) 5CH3. Dehidrogenacija se odvija preko metilcikloheksana - cikloalkana s formulom C7H14. To je monociklički ugljikovodik čija metilna skupina ima jedan supstituirani vodikov atom.
Toluen se pročisti na isti način kao i benzen. To je samo ako se primjenjuje sumporna kiselina potrebno je uzeti u obzir - ova se supstanca lakše sulfurira. To znači da je kod čišćenja toluena potrebno održavati nižu temperaturu. Točnije, ispod 30 ° C.

Toluen i benzen
Budući da su ove dvije tvari slične, vrijedi izvršiti usporedbu kemijskih svojstava. Benzen i toluen podliježu reakcijama supstitucije. Međutim, njihova brzina protoka je različita. Budući da metilna skupina u molekuli toluena utječe na aromatski prsten, on brže reagira.
Međutim, benzen pokazuje otpornost na oksidaciju. Tako, na primjer, kada to utječe kalijev permanganat, ništa se ne događa. No, toluen u ovoj reakciji tvori benzojevu kiselinu, kao što je već spomenuto.
Istodobno je poznato da zasićeni ugljikovodici ne reagiraju s otopinom kalijevog permanganata. Tako je oksidacija toluena posljedica djelovanja benzenskog prstena na metilnu skupinu. Ovu tvrdnju potvrđuje teorija Butlerova. U skladu s tim, atomi i njihove skupine u molekulama vrše uzajamni utjecaj.
Friedel-Craftsova reakcija
Mnogo je gore rečeno o formuli i kemijskim svojstvima toluena. Ali još nije spomenuto da se ova supstanca sasvim može dobiti iz benzena, ako provodite Friedel-Craftsovu reakciju. To je način acilacije i alkilacije aromatskih spojeva pomoću kiselih katalizatora. To uključuje bor trifluorid (BF3), cink klorid (ZnCl2), aluminij (AlCl3) i željezo (FeCl3).
To je samo u slučaju toluena, možete koristiti samo jedan katalizator. A to je željezni tribromid, koji je kompleksni binarni spoj anorganske prirode s formulom FeBr3. Reakcija je sljedeća: C6H6 + CH3 Br FeBr3C6H5CH3 + HBr. Tako se ne kombiniraju samo kemijska svojstva benzena i toluena, nego i sposobnost dobivanja jedne tvari iz druge.

Opasnost od požara
Da ne spominjem o tome, govorimo o kemijskim i fizičkim svojstvima toluena. Uostalom, to je vrlo zapaljiva tvar.
Spada u zapaljive tekućine klase 3.1. Dizelsko gorivo, plinsko ulje i desenzibilizirani eksplozivi uključeni su u ovu kategoriju.
Ne dopustite da se u blizini toluena pojave otvoreni plamenovi, iskre ili dim. Čak je i mješavina para te tvari s zrakom eksplozivna. Ako se izvode radovi na odvodnji, od najveće je važnosti poštivanje pravila zaštite od statičkog elektriciteta.
Proizvodni pogoni namijenjeni za rad u vezi s toluenom osigurani su dovodnom i odvodnom ventilacijom, a oprema - usisavanje. Zabranjena je uporaba alata koji mogu dati iskru. A ako se tvar zapali, treba je ugasiti samo vodenom maglom, zrakom mehaničkom ili kemijskom pjenom. Izliveni toluen se neutralizira pijeskom.
Opasnost za ljude
Karakteristike i kemijska svojstva toluena određuju njegovu toksičnost. Kao što je već spomenuto, njegovi parovi imaju narkotički učinak. Osobito je jaka u povišenim koncentracijama. Osoba koja je udisala isparenja ima jake halucinacije. Malo ljudi zna, ali do 1998. ova tvar je bila dio ljepila Moment. Zato je bio toliko popularan među ovisnicima.
Visoke koncentracije ove tvari također štetno djeluju na živčani sustav, sluznice očiju i kože. Funkcija stvaranja krvi je smanjena, jer je toluen vrlo otrovan otrov. Zbog toga se mogu pojaviti bolesti kao što su hipoksija i cijanoza.
Čak postoji i pojam toksuomanike toluena. Djeluje kancerogeno. Uostalom, par, koji prolazi kroz kožu ili dišne organe u ljudskom tijelu, utječe na živčani sustav. Ponekad se ti procesi ne mogu poništiti.
Osim toga, parovi mogu uzrokovati letargiju i poremetiti funkcioniranje vestibularnog aparata. Stoga ljudi koji rade s ovom tvari rade u dobro prozračenim prostorima, uvijek pod naprezanjem, i koriste posebne gumene rukavice.

primjena
Da bi se dovršila tema o fizikalno-kemijskim svojstvima toluena treba uzeti u obzir područja u kojima je ta tvar aktivno uključena.
Uglavnom se koristi kao sirovina za proizvodnju nitrotoluena, benzil klorida, benzojeve kiseline, kao i drugih organska tvar.
Ovaj spoj je također djelotvorno otapalo za mnoge polimere (amorfne kristalne tvari visoke molekulske mase). Često se dodaje u sastav komercijalnih otapala za boje i lakove, neke lijekove. Čak iu proizvodnji eksploziva ovaj spoj je primjenjiv. Trinitrotoluen i trotiltol nastaju s njegovim dodavanjem.