Kvantno-mehanički model atoma i njegove strukture
Planetarni kvantno-mehanički model Bohrovog atoma često se pamti po svojoj urednoj i poznatoj slici elektrona. Okreću se oko središnje jezgre, poput planeta oko sunca. Zbog toga je teško zamijeniti sliku one koja točnije predstavlja kvantno-mehanički model atoma koji koriste moderni fizičari.
Kako se atom kreće i kreće?
Atom ima malu jezgru i valove oštrih orbita. Položaj i gibanje elektrona opisuju valovi njihove tvari. Ove strukture predviđaju vjerojatnost pronalaženja elektrona u određenom području atoma. Ali odakle dolazi kvantno-mehanički model Bohrovog atoma?
Planetarni model pokrenuo je proces uvođenja kvantne teorije u strukturu atoma. Bohr je uveo ideju stacionarnih stanja u kojima je atom bio stabilan. Prijelazi između tih stanja objašnjavaju postojanje spektralnih linija. U slučaju vodika, on je mogao dobiti razine energije:
- Prijelazi između njegovih razina energije odgovarali su linijama u spektru vodika.
- Njegov model nije mogao predvidjeti razinu energije za bilo koje druge atome (iako bi se razine alkalijskih metala poput vodika mogle približiti istini).
Odvojeno, rad Heisenberga i Schrödingera proveden je kako bi se izmislili načini da se potpunije opišu kvantizirane razine energije atoma.
Analogije Heisenberga i Schrödingera: kako su dovele jednadžbu do dokaza o valu
Kvantno-mehanički model strukture atoma ima jedinstveni skup svojstava. Heisenberg je koristio matrice, a Schrödinger je razvio valnu jednadžbu kako bi dokazao apsolutnost razlike u ponašanju kvanta. Dvojnost čestica prikazana je detaljnije u videu.

Schrödingerove jednadžbe prikazuju gustoću vjerojatnosti elektrona oko jezgre atoma. Većina definicija kvantne teorije i kvantne mehanike nudi isti opis za oba. One u biti opisuju kvantnu teoriju, u kojoj i energija i materija imaju karakteristike valova u nekim uvjetima i karakteristike čestica u drugima.
Da bi ideja bila jasnija, ljudi su počeli provoditi eksperimente u smislu mentalnog obećanja.

- Kvantna teorija sugerira da energija dolazi u diskretnim paketima koji se nazivaju kvanti (ili, u slučaju elektromagnetskog zračenja, fotoni).
- Kvantna teorija ima neki matematički razvoj, često nazvan kvantna mehanika, koji nudi objašnjenja za ponašanje elektrona unutar oblaka elektrona atoma.
Glavne odredbe kvantno-mehaničkog modela strukture atoma je dualnost elektronskih valova u oblaku elektrona, što ograničava našu sposobnost istovremenog mjerenja energije i položaja elektrona.
Skrivene značajke elektrona
Što točnije mjerimo energiju ili položaj elektrona, to manje znamo o drugom. Ne možemo točno označiti položaj i zamah elektrona u isto vrijeme. Zbog toga je nemoguće predvidjeti putanju čestice. Prema tome, ponašanje elektrona opisano je drugačije nego ponašanje čestica normalne veličine. Trebate znati:
- Najčešći način opisivanja elektrona u atomima u skladu s kvantnom mehanikom jest rješavanje Schrödingerove jednadžbe za energetska stanja elektrona u ovom oblaku.
- Kada je elektron u tim stanjima, njegova energija je jasno definirana, a položaj nije.
- Položaj se opisuje zemljom raspodjele vjerojatnosti, nazvanom orbitalna.
Trajektoriju koju obično povezujemo s makroskopskim objektima zamjenjuju elektroni u oblacima elektrona, a statistički opisi ne ukazuju na put, već na područje u kojem se nalazi. Budući da elektron u atomskom elektronskom oblaku određuje njegovo kemijsko ponašanje, da bi razumio kemiju, potrebno je opisati konfiguraciju elektrona u ključu kvantno-mehaničkog modela atoma.
Heisenbergov princip nesigurnosti: područje unutar atoma
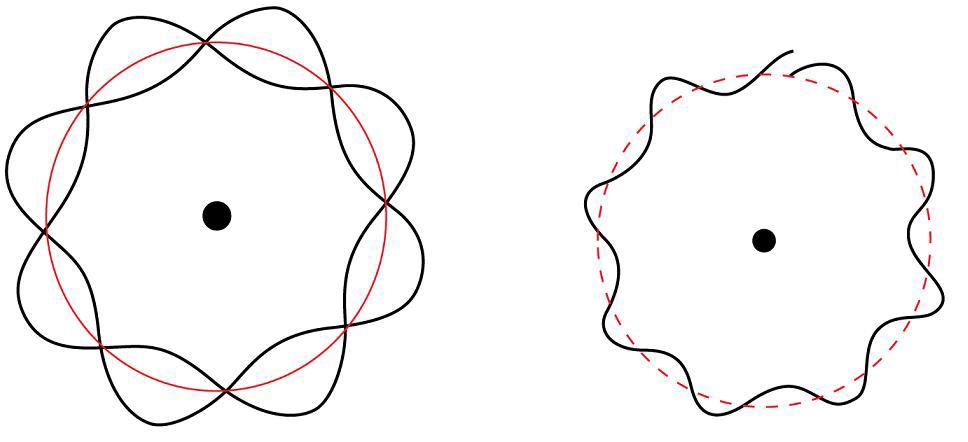
Louis de Broglie je predložio da se sve čestice mogu smatrati materijalnim valovima s valnom duljinom - lambda, definiranom sljedećom jednadžbom:
Lambda = stvarno vrijeme (sat) + milivoltni sat
Erwin Schrödinger je predložio kvantno-mehanički model atoma. Ukratko: elektrone tretira kao valove tvari.
Kvadrat funkcije vala predstavlja vjerojatnost pronalaženja elektrona u danoj regiji unutar atoma. Atomska orbita definirana je kao područje unutar atoma, gdje se nalazi elektron.
Heisenbergov princip nesigurnosti navodi da ne možemo znati ni energiju ni položaj elektrona. Stoga, kada više saznamo o položaju elektrona, znamo manje o njegovoj energiji, i obrnuto. Elektroni imaju unutarnje svojstvo koje se naziva spin. Bilo koja dva elektrona koja zauzimaju istu orbitu moraju imati suprotne spinove.
Luminiferous eter u kvantnom svijetu
Priroda svjetla bila je predmet istraživanja još od antike. U 17. stoljeću Isaac Newton provodio je pokuse s lećama i prizmama. Mogao je pokazati da se bijela svjetlost sastoji od pojedinačnih boja duge, spojenih zajedno. Newton je objasnio rezultate svoje optike s "corpuscular" pogledom na svjetlo, u kojem se svjetlo sastojalo od strujanja ekstremno malih čestica koje su se kretale velikom brzinom u skladu s Newtonovim zakonima gibanja. Vrijedi spomenuti:
Christian Huygens je pokazao da se optički fenomeni kao što su refleksija i refrakcija mogu jednako dobro objasniti sa stajališta svjetla kao valovi koji se kreću velikom brzinom kroz medij nazvan "svjetleći eter". Prožima cijeli prostor.
Na početku devetnaestog stoljeća, Thomas Young je pokazao da svjetlost koja prolazi kroz uske, usko razmaknute proreze stvara interferencijske obrasce koji se ne mogu objasniti sa stajališta newtonskih čestica, ali se mogu lako interpretirati s gledišta valova.
- Kasnije, u devetnaestom stoljeću, nakon što je James Clerk Maxwell razvio svoju teoriju elektromagnetskog zračenja i pokazao da je svjetlo vidljivi dio ogromnog spektra elektromagnetskih valova, pogled na česticu svjetlosti postao je potpuno diskreditiran.
Danas se ta područja nazivaju klasična mehanika i klasična elektrodinamika (ili klasični elektromagnetizam).
Kako je napredovala ideja uvođenja novih pojmova u fizici

Do kraja devetnaestog stoljeća, znanstvenici su vidjeli fizički svemir kao približno sastavljen od dva odvojena područja:
- materija formirana od čestica koje se kreću prema Newtonovim zakonima gibanja;
- elektromagnetsko zračenje koje se sastoji od valova pod kontrolom Maxwellovih jednadžbi.
Paradoksi su doveli do moderne strukture kvantno-mehaničkog modela Schrödinger-ovog atoma, koji usko povezuje čestice i valove na temeljnoj razini, a naziva se dvojnost valne čestice, koja je zamijenila klasični pogled.
Diskretni bohr val: kako se ponašaju emisijski spektri vodika
Prema Bohrovom modelu, emisijski spektri različitih elemenata sadrže diskretne linije. Vidljiva regija emisijskog spektra vodika može se prikazati pomoću tablice.
| Osnovni kvantni broj | Broj pod-razina | Broj elektrona |
| 1 | 1 | 2 |
| 2 | 2 | 8 |
| 3 | 3 | 18 |
| 4 | 4 | 32 |
To je shematski prikaz kvanta, gdje je poznat broj elektrona i razina. U životu u vakuumskim uvjetima nemoguće je sa sigurnošću reći da postoji ograničenje na pod-razinama, ali ne može biti više od 7. Kvantizirani emisioni spektri ukazuju da Bohr može postojati unutar atoma samo na određenim atomskim radijusima i energijama.

Konstruirajući model, Bohr je izveo jednadžbu koja je točno predvidjela različite razine energije u atomu vodika. Kvantno-mehanički model bio je prikladan samo za predstavljanje tog konkretnog slučaja. Razine su odgovarale emisijskim linijama u spektru tvari.
Bohrov model, koji je dokazao jednoelektronske vodikove sustave
Brzina elektrona na energetskoj razini osnovnog stanja vodika je 2,2 × 10 6 s, m, gdje je s dužina, m je masa. Možemo zamijeniti konstantu, kao i masu i brzinu elektrona u de Brogliejevu jednadžbu. Ali u isto vrijeme, nije mogao objasniti elektroničku strukturu u atomima koji su sadržavali više od jednog elektrona.
Ako se okrenemo kemiji, kvantno-mehanički model vodikovog atoma trebao bi se sastojati samo od protona. Kada se susreću s elektronima ili neutronima, čestica počinje se ponašati kao val. U drugim slučajevima, atomi druge tvari mogu se, bez obzira na strukturu, ponašati kao valovi ili čestice. Ukratko, kvantno-mehanički model vodikovog atoma je materijalni dualizam vala, ali ne i čestica.
Preklapanje valova jedan na drugi: kako se staze sjecišta atoma ne miješaju
Radio valovi s mobilnog telefona, rendgenski zraci koje koriste stomatolozi, energija koja se koristi za kuhanje u mikrovalnoj pećnici, zračenje topline iz vrućih objekata i svjetlo s TV zaslona svi su oblici elektromagnetskog zračenja koji pokazuju valovito ponašanje. Potrebno je zapamtiti:
- Val je oscilacija ili periodično gibanje koje može prenijeti energiju iz jedne točke prostora u drugu.
- Potresanje kraja užeta prenosi energiju iz vaše ruke na drugi kraj užeta; šljunak koji pada u ribnjak vodi do širenja valova duž površine vode; širenje zraka koje prati munju stvara zvučne valove (grmljavinu) koji mogu putovati nekoliko milja.
- U svakom od ovih slučajeva, kinetička energija se prenosi kroz tvar (konopac, voda ili zrak), dok tvar ostaje na mjestu.
Valovi ne smiju biti ograničeni na putovanje kroz materiju. Kao što je Maxwell pokazao, elektromagnetski valovi se sastoje od električnog polja koje osciliraju u vremenu s okomitim magnetskim poljem. Oni su okomiti na smjer kretanja. Ovi valovi mogu prolaziti kroz vakuum pri konstantnoj brzini od 2.998 × 108 m / s, gdje je c brzina svjetlosti.