Redox. Redoks reakcije: opis, primjeri
Redoks reakcije - redox - predstavljaju protuparalelnu interakciju. Tijekom tih fenomena mijenjaju se neke karakteristike komponenti. Ove interakcije ostvaruju se metodom elektronske redistribucije. Taj se proces odvija između oksidirajućih atoma i redukcijskih sredstava. 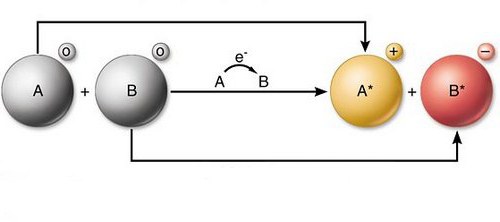
Svojstva komponente
Organska kemija uključuje uporabu širokog raspona sredstava za oksidaciju i redukcijskih sredstava. To vam omogućuje odabir specifičnog reagensa koji ima selektivnost. To znači da komponenta može selektivno utjecati na određene funkcionalne kategorije. Osim toga, zahvaljujući toj širini izbora, moguće je dobiti proizvode u određenom stupnju oksidacije. Tako, na primjer, borogid Na ne može stupiti u interakciju s estrima i amidima. Istovremeno, reducira aldehide ili ketone na alkohole. Od druge skupine komponenti postoje i visoko selektivni spojevi. Kao primjer, kompleks Cr03 i piridin. Ova struktura oksidira alkohole visokog prinosa do ketona. S tim u vezi ne utječe na CC komunikaciju. SeO2 je također visoko selektivan. Spoj oksidira aldehidi i ketoni alfa dikarbonil spojevima.
Opće informacije
Redoks reakcije upućuju na različitu promjenu svojstava ulaznih komponenti. To ovisi o prirodi interakcije. Tako se tijekom redukcije smanjuje, a tijekom oksidacije se povećava. oksidacijsko stanje elementi. U početku, termin se tumačio dovoljno jednostavno da bi ga se moglo razumjeti. Prema tome, oksidacija se smatrala dodavanjem kisika, a restauracija - uklanjanje. Nakon uvođenja elektroničkih koncepata u znanost, definicija je donekle proširena. Od tada se koncept proširuje na interakcije u kojima nije uključen kisik. 
Karakteristike procesa
Redoks reakcije formalno predstavljaju kretanje elektrona. Komponente iz atoma jednog reagensa prenose se na atom drugog. Dakle, oksidacija je, jednostavno rečeno, trzaj elektrona. U nekim slučajevima, proces u molekuli u izvornoj tvari može postati nestabilan. Kao rezultat, može se raspasti na manje komponente, ali s visokim stupnjem stabilnosti. Atomi oksidirajućih tvari obično se nazivaju donori elektrona, strukturni elementi oksidirajućeg agensa su prihvatljivi. Nastavlja se suprotan proces vezanja elektrona. To se naziva restauracija. U interakciji ove vrste mogu se uzeti različiti elementi. Na primjer, ugljik, vodik i drugo. Mogu se obnoviti različiti spojevi. Na primjer organske kiseline u alkohole i aldehide. 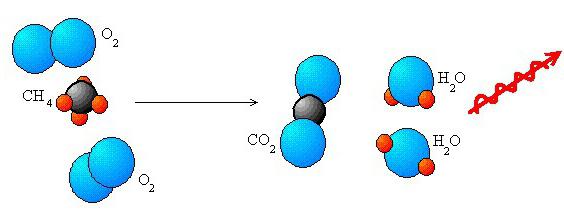
Vrste redoks reakcija
U skladu s formalnim značajkama razmatrane interakcije dijele se na intra - i intermolekularne. Ovo posljednje, na primjer, uključuje 2SO2 + 02> S03. Također, redoks reakcije klasificiraju se kao nesrazmjerne i repro-razmjerne. U prvom slučaju isti element ima različita svojstva. Prema tome, komponenta može istovremeno biti i redukcijsko sredstvo i oksidacijsko sredstvo:
Cl2 + H20 → HCl + HCl.
Druga vrsta - reproportacija ili proporcija - predstavlja nekoliko drugih interakcija. U takvim reakcijama jedan element dolazi iz dva različita oksidacijska stanja za jedan element:
NH4NO3 → N20 + 2H20
Katalitički procesi
Unutar tih interakcija pruža visoku sposobnost selektivnosti. Tako, na primjer, u skladu s katalizatorom i uvjetima, acetilenski ugljikovodici mogu se selektivno podvrgnuti hidrogenaciji do zasićenog ili etilena. A redukcija CO 2 u CO elektrokemijskog tipa u vodenom mediju u prisutnosti 1,4,8,11-tetraazacikotetradekana kompleksa nikla omogućuje da se proces provodi na nižim potencijalima i istovremeno suzbije. elektroliza vode tijekom stvaranja H2. Ova interakcija ima ključnu vrijednost u transformaciji CO CO 2 u različite organske tvari.
vrijednost
Redox katalitičke reakcije priroda obavlja važne zadatke u industriji. Vrlo su rasprostranjeni u prirodi i koriste se u inženjerstvu. Također, osnova života su redoks reakcije koje se javljaju tijekom transporta elektrona, respiratorne aktivnosti, fotosinteze. Ove interakcije pružaju većinu potrošnje energije ljudi spaljivanjem raznih fosilnih goriva. 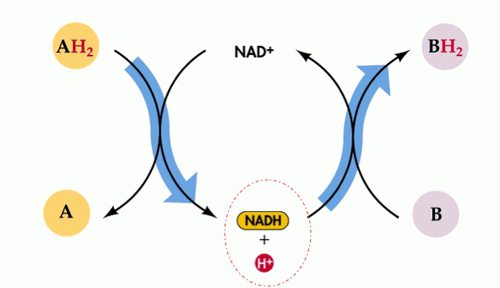
Protok interakcije
Redoks reakcije često prate povećano oslobađanje energije. To im omogućuje korištenje prilikom primanja, na primjer, struje. Najviše nasilnih interakcija događa se u odsutnosti otapala. Ako su prisutne, takve reakcije se možda neće pojaviti. To može biti zbog činjenice da jedna ili obje komponente reagiraju s otapalom. Možemo vam dati sljedeći primjer. U vodenoj otopini, reakcija 2Na + F 2 → 2NaF je nemoguća. To je upravo zbog činjenice da se fluor i natrij odlikuju snažnom interakcijom s H 2 O. Na formiranje kompleksa uvelike utječe svojstvo iona u redoks reakcijama. Tako se, na primjer, događa s [C0 2 + (CN) 6 ] 4 -. Ovaj kompleks se smatra jakim redukcijskim sredstvom, za razliku od CO 2 + hidratiranog iona.
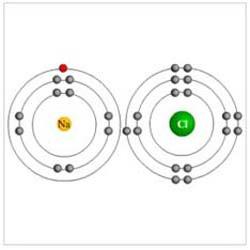
Organska kemija. Redoks reakcije
U ovom se disciplinskom području primjena generaliziranih pojmova i pojmova o tijeku i prirodi procesa smatra neproduktivnim. To je osobito istinito u prisutnosti laganog polariteta interatomske veze. U organskoj kemiji, uobičajeno je razmotriti oksidaciju kao proces povećanja učestalosti kiseline koja sadrži ili povećava broj veza koje sadrže vodik. U nekim slučajevima koristi se pristup koji pretpostavlja da se različiti stupnjevi oksidacije pripisuju C-atomima.

To, pak, ovisi o broju veza nastalih s komponentom koja ima veću elektronegativnost od vodika. U tom slučaju, položaj funkcionalnih derivata provodit će se u redoslijedu povećanja oksidacijskih stanja. Tako, na primjer, zasićene ugljikovodike treba pripisati nultoj skupini (Art. Oxid. - 4), ROH, RNH 2 , RCl - prema prvoj (-2), R2CCl2 i R 2 CO - do 2. (0), RCCl 3 i RCONH 2 - na 3. (+2), CO 2 i CCl 4 - na 4. (+4). U ovom slučaju, jasno je da je oksidacija proces u kojem se spojevi prenose na višu razinu, a redukcija je obrnuti postupak. U proučavanju interakcija, posebnu pozornost treba posvetiti mehanizmima po kojima se proces odvija. Treba napomenuti da su ti čimbenici vrlo raznoliki. Prema tome, reakcije se mogu odvijati putem homolitičkog ili heteroliznog mehanizma. Međutim, u mnogim slučajevima, postupak prijenosa jednog elektrona djeluje kao početna faza interakcije. Proces oksidacije, u pravilu, karakteriziran je strujanjem u položajima s najvećom gustoćom i redukcijom u položajima gdje je gustoća elektrona minimalna.