Što su halogeni u kemiji?
Razgovarajmo o tome što su halogeni. Nalaze se u sedmoj skupini (glavna podgrupa) periodnog sustava. Prevedeno s grčkog, "halogen" znači "rađanje soli". U članku će se govoriti o tome što čini kemijski halogen, koje tvari su kombinirane pod tim pojmom, koja su njihova svojstva i značajke proizvodnje.

Posebne značajke
Raspravljajući o tome što su halogeni, uočavamo specifičnost strukture njihovih atoma. Svi elementi na vanjskoj energetskoj razini imaju sedam elektrona, a jedan od njih je nesparen (slobodan). Stoga su izražena oksidacijska svojstva halogena, odnosno dodavanje jednog elektrona tijekom interakcije s različitim tvarima, što dovodi do potpunog završetka vanjske razine energije, formiranja stabilnih konfiguracija halogenida. Kod metala oni tvore krutinu ionske veze karakter.

Predstavnici halogena
One uključuju sljedeće elemente: fluor, klor, brom, jod. Astatis i tennesin imaju formalni odnos s njima. Da bismo razumjeli što su halogeni, treba napomenuti da klor, brom i jod imaju slobodnu orbitalu. Ona objašnjava razne stvari oksidacijska stanja za te stavke. Na primjer, klor ima sljedeće vrijednosti: -1, + 1, + 3, +5, +7. Kada se atomu klora daje dodatna energija, dolazi do postupnog prijelaza elektrona, što objašnjava promjene u stupnjevima oksidacije. Među najstabilnijim konfiguracijama klora su njegovi spojevi u kojima je stupanj oksidacije -1, kao i +7.

Biti u prirodi
Obilježja strukture objašnjavaju njihovu prevalenciju u prirodi. Halogeni spojevi u prirodi su predstavljeni kao halidi, visoko topljivi u vodi. S povećanjem atomskog radijusa halogena smanjuje se njihov kvantitativni sadržaj u zemljinoj kori. Primjerice, neki spojevi broma, klora i fluora koriste se u industrijskim volumenima.
Kalcij fluorid (fluorit) može se spomenuti kao glavni spoj fluora prisutan u prirodi.
Značajke primitka
Da bismo razumjeli što su halogeni, potrebno je saznati kako ih dobiti. Glavna opcija za izolaciju čistih halogena iz soli je elektroliza rastaljenih soli. Na primjer, kada ste izloženi natrijev klorid izravna električna struja kao reakcijski proizvodi mogu se smatrati ne samo plinovitim klorom, već i metalnim natrijem. Na katodi se reducira metal, a na anodi se formira halogen. Za dobivanje broma uporabom morske vode provodi se elektroliza ove otopine.
Fizička svojstva
Osvrnimo se na fizička svojstva predstavnika sedme skupine glavne podskupine. Fluor u normalnim uvjetima je plinovita tvar koja ima svijetlo žutu boju, oštar i iritantan miris. Plinoviti i žuto-zeleni klor, s oštrim zagušljivim jantarima. Brom je smeđa teška tekućina. Od svih halogena, samo jod je ljubičasta kristalna supstanca.
Fluor je najjači oksidirajući agens. U skupini, sposobnost vezanja elektrona tijekom kemijske reakcije postupno se smanjuje od fluora do astata. Razlog slabljenja ovog svojstva je povećanje atomskog radijusa.
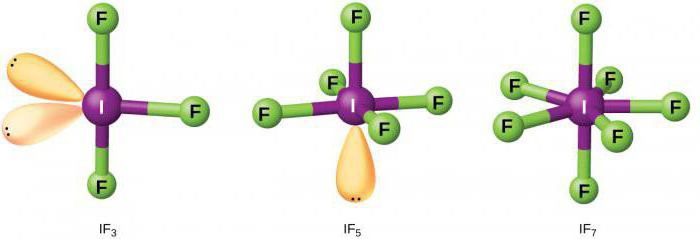
Značajke kemijskih svojstava
Fluor, kao najjači oksidirajući agens, može reagirati bez dodatnog zagrijavanja s gotovo svim nemetalima. Proces je popraćen oslobađanjem velike količine topline. Kod metala, proces je karakteriziran samozapaljivanjem fluora.
Budući da se ovaj halogen odlikuje visokom kemijskom aktivnošću, on je u stanju djelovati kada je izložen plemenitim plinovima.
Fluor reagira sa složenim tvarima. Aktivnost broma je značajno niža. Uglavnom se koristi u organskoj kemiji za provođenje kvalitativnih reakcija na nezasićene spojeve.
Jod je u interakciji s metalima samo kada se zagrijava, a proces karakterizira apsorpcija energije (egzotermna reakcija).
Značajke uporabe
Koja je vrijednost halogena? Da biste odgovorili na ovo pitanje, razmotrite glavna područja njihove primjene. Na primjer, prirodni mineral cryolite, koji je spoj aluminija, fluora, natrija, koristi se kao dodatak u pasti za zube kako bi se spriječilo propadanje zuba.
Klor u velikim količinama koristi se u proizvodnji klorovodične kiseline. Osim toga, ovaj halogen je tražen u proizvodnji plastike, otapala, boja, guma, sintetičkih vlakana. Velika količina spojeva koji sadrže klor služe za učinkovito suzbijanje raznih štetočina poljoprivrednih kultura. Klor, kao i njegovi spojevi, također su potrebni za izbjeljivanje pamučne i lanene tkanine, papira i dezinfekciju pitke vode. Brom i jod se koriste u kemijskoj i farmaceutskoj industriji.
U novije vrijeme se za čišćenje pitke vode umjesto klora koristi ozon.
Biološko djelovanje
Visoka reaktivnost halogena objašnjava činjenicu da su svi ti spojevi otrovi koji imaju gušenje i mogu oštetiti organska tkiva. Unatoč tim karakteristikama, ti su elementi nužni za vitalne procese ljudskog tijela.
Na primjer, fluor je uključen u metaboličke procese u živčanim stanicama, mišićima, žlijezdama. U svakodnevnom životu, teflonska jela sve su češća, a fluor je jedan od njegovih sastojaka.
Klor potiče rast kose, potiče metaboličke procese, daje tijelu snagu i snagu. Maksimalna količina u obliku natrijevog klorida dio je krvne plazme. Među spojevima ovog elementa od posebnog interesa s biološkog stajališta je klorovodična kiselina.
Da je osnova želučanog soka, uključen je u procese cijepanja hrane. Da bi tijelo funkcioniralo normalno, osoba mora konzumirati najmanje dvadeset grama dnevno. sol.
Svi halogeni su potrebni osobi za vitalnu aktivnost, a također ih koristi u različitim područjima djelovanja.