Metilni alkohol: svojstva, priprema i uporaba
uvod
Došli ste navečer s posla, presvukli se, a zatim, promatrajući vašu naviku, sjeli na stolicu ispred televizora i uključili kanal s vijestima u zraku. Spiker prvo emitira nešto nerazumljivo, a zatim daje nešto poput: "I konačno, glavna vijest dana. U takvom i takvom gradu došlo je do masovnog trovanja metilnim alkoholom. Nekoliko desetaka ljudi je poginulo, jer je još mnogo njih hospitalizirano." Vaš sluh odmah je uhvatio ime nepoznate tvari - "metil alkohol". Većina ljudi doznaje za njegovo postojanje na ovaj način. Neki će brzo zaboraviti ovu frazu, a neki će htjeti saznati više o tome. Ovdje ću im opisati sva svojstva metilnog alkohola.
definicija
Metil alkohol (formula CH3OH) je najjednostavniji monohidrični alkohol, prvi predstavlja homolognu seriju ovih posljednjih.
ime
U različitim izvorima može se nazivati različito: metil hidroksid, metanol, drveni alkohol, karbinol i metil hidrat.
Proizvodnja metilnog alkohola
Sve do 60-ih godina dvadesetog stoljeća za sintezu metilnog alkohola korištene su samo cink-kromne kemikalije, no kasnije se to iskustvo počelo provoditi na katalizatorima koji sadrže bakar. Ali danas se dobiva katalitičkom sintezom iz ugljikovog monoksida (II) i vodika pri temperaturi od 250 ° C, tlaku od 7 megapaskala i određenih katalizatora (cinkov oksid i bakar oksid). Prije toga je metilni alkohol dobiven suhom destilacijom drva. Ali danas je ova metoda sekundarna. U tu svrhu može se koristiti i otpad od rafiniranja i ugljen za koksiranje.
nekretnine 
Metanol je bezbojna tekućina bez mirisa. etil alkohol. Voda, etanol i eter mogu se pomiješati s njom u bilo kojem odnosu. Komprimira se i zagrijava kada se pomiješa s vodom. On također ima reputaciju snažnog otapala i često može zamijeniti etil alkohol. Ako se otopi u bezvodnom metanolu bakar sulfat, postaje plavkasto-zelena. Zbog toga se takav bezvodni vitriol ne može koristiti za otvaranje tragova vode u metilnom alkoholu. Metanol ne može oblikovati azeotropnu smjesu s vodom, zbog toga se smjese vode i metilnog alkohola mogu odvojiti destilacijskom destilacijom. Metanol se kombinira s mnogim solima kako bi nastao solvat. Kod reakcije s alkalnom lužinom mogu se dobiti alkoholati.
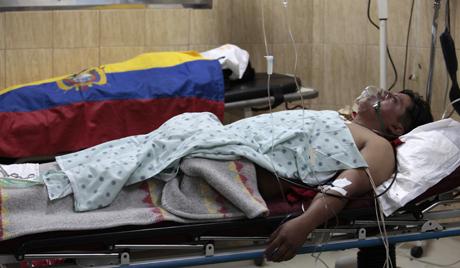 Metilni alkohol: trovanje
Metilni alkohol: trovanje
Metanol je najjači otrov, zahvaćen je njegov živčani i kardiovaskularni sustav. Trovanje je posljedica "smrtonosne sinteze" - metaboličke oksidacije u tijelu, čiji je proizvod vrlo otrovan formaldehid. Do teškog trovanja dolazi kada se proguta 5-10 ml metilnog alkohola, a ako je 30 ili više grama, sljepoća i / ili smrt su neizbježni. Simptomi blagog trovanja su glavobolja, opća slabost, slabost, zimica, mučnina i povraćanje. Zbog toga su životno opasni proizvodi čak i uz najmanju koncentraciju metanola. Antidot za trovanje ovom tvari je etil alkohol. Primjenjuje se intravenskim ili oralnim putem. Međutim, to ne bi trebalo raditi sam - s pogrešnom dijagnozom i doziranjem, situacija će se samo pogoršati. Dakle, ako sumnjate na trovanje metilnim alkoholom, hitnu potrebu nazvati liječnika.
primjena 
U plinskoj industriji, borba protiv stvaranja hidrata nije potpuna bez metilnog alkohola. Uz to se proizvode formaldehid, formalin, octena kiselina i brojni esteri. Metanol se koristi u proizvodnji otapala za lakove. Može poslužiti i kao dodatak tekućim gorivima za motore s unutarnjim izgaranjem i kao gorivo za motocikle i automobile. Od metilnog alkohola dobivate biodizel. Također u parfumeriji, on je denaturirajući dodatak etanolu. Gorive ćelije rade samo zbog oksidacije metanola u ugljikov monoksid (Iv) na katalizatoru.
zaključak
Sada znate sve o metilnom alkoholu. I, kao što možete vidjeti, unatoč toksičnosti, može biti vrlo korisno za osobu, samo uz pažljivo rukovanje s njom.