Dušikov oksid: formula, svojstva, primjena
Oksidi se nazivaju binarni spojevi kemijskih elemenata s atomom kisika, u kojem je oksidacijski stupanj 2-. Dušik, koji ima nižu elektronegativnu vrijednost, tvori razne kombinacije s kisikom. Ti spojevi pripadaju različitim klasama tvari. Dušikov oksid sadrži kisik u količini koja određuje valenciju elementa N. Ona se kreće od 1 do 5.
Što su oksidi
Postoji oko desetak dušikovih spojeva koji sadrže O-element. Od tih pet najčešće se susreću: monovalentni oksid, dvovalentni oksid, trovalentni oksid, tetravalentni oksid i pentavalentni oksid. 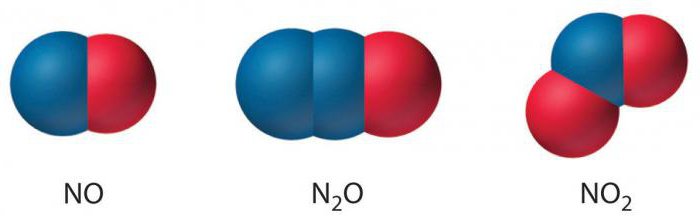
Preostali spojevi smatraju se manje uobičajenim. To uključuje tetravalentni dušikov oksid u obliku dimera, nestabilne molekule nitrilazida, nitrozil azida, trinitramida i nitratnog radikala.
Formula dušičnih oksida
U nastavku su prikazani simboli najznačajnijih spojeva elementa N.
To je prije svega dušikov oksid, čija se formula sastoji od dva kemijska znaka - N i O. Indeksi se stavljaju iza njih, ovisno o oksidacijska stanja atoma.
- Monovalentni dušikov oksid ima formulu N2O. U njemu je N atom napunjen +1.
- Dušikov oksid ima formulu NO. U njemu je N atom napunjen +2.
- Dušikov željezni oksid ima formulu N203. U njemu je N atom napunjen +3.
- Tetravalentni dušikov oksid, čija je formula NO2, ima naboj N + 4 atoma.
- Pentavalentni kisikov spoj je označen kao N205. U njemu se N atom napuni +5.
Opis monovalentnog dušikovog oksida
Također se naziva diazo, dušikov oksid i plin za smijeh. Prezime dolazi od djelovanja povezanog s intoksikacijom. 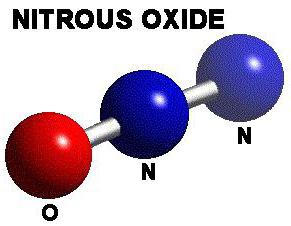
Dušikov oksid s valencijom I u normalnim temperaturnim uvjetima postoji u obliku nezapaljivog plina, bez boje, koji pokazuje ugodan slatkast okus i miris. Zrak je lakši od ovog spoja. Oksid je topljiv u vodenom mediju, etanolu, eterima i sumpornoj kiselini.
Vodene, alkalne i kiselinske otopine ne mogu reagirati s njim, ne stvaraju sol. Ne podliježe paljenju, ali je u stanju podržati proces izgaranja.
Amonijev dušikov oksid pretvara se u azid (N3NH4).
Kada se kombinira s molekulama etera, kloroetana i ciklopropana, stvara se eksplozivna smjesa.
Normalni uvjeti doprinose njegovoj inerciji. Pod djelovanjem zagrijavanja tvar se vraća.
Opis oksida dvovalentnog dušika
Također se naziva monoksid, oksid ili nitrosil radikal. Pod normalnim temperaturnim uvjetima, to je bezbojni, nezapaljivi plin, slabo topljiv u vodenoj sredini. Zrak se oksidira, ispada NO 2. Njegova tekuća i čvrsta forma postaje plava. 
Dušikov oksid može biti redukcijsko sredstvo u reakcijama interakcije s halogenima. Produkt njihovog dodavanja je nitrozil halid, koji ima formulu NOBr.
Sumporni dioksid i drugi jaki redukcijski agensi oksidiraju NO u obliku N2 molekula.
Opis željeznog oksida
Nazivaju se nitroznim anhidridom. U normalnom stanju može biti tekućina plave boje, a standardni parametri medija pretvaraju oksid u oblik plina koji nema boju. Ima stabilnost samo na niskim temperaturama.
N2O3 molekule disociraju tijekom zagrijavanja oslobađanjem mono- i bivalentnog oksida.
Kao anhidrid, dodaje vodu za proizvodnju dušične kiseline, a alkalijama tvori soli u obliku nitrita.
Opis oksida tetravalentnog dušika
Na drugi način to se naziva dioksid. Tu je u obliku smeđe-crvenog plina, koji ima oštar miris, a može također biti žućkasta tekućina. 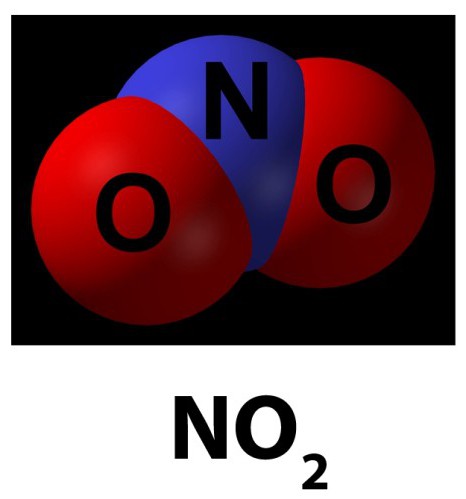
Odnosi se na kisele okside, koji imaju dobro razvijenu kemijsku aktivnost.
Njegove molekule oksidiraju ne-metale formiranjem spojeva koji sadržavaju kisik i slobodnog dušika.
Dioksid reagira s tetravalentnim i šestvalentnim sumpornim oksidom. Ispada sumporna kiselina. Metoda njegove sinteze naziva se nitroz.
Dušikov oksid se može otopiti u vodenom okolišu. Dušična kiselina je rezultat ove reakcije. Taj se proces naziva nesrazmjer. Intermedijarna komponenta se smatra dušičnom kiselinom, koja se brzo raspada.
Ako otopite dušik tetravalentnog oksida u lužinama, tada nastaje otopina nitrata i nitrita. Možete koristiti svoj tekući oblik za interakciju s metalom, zatim dobivate bezvodnu sol.
Opis pentavalentnog dušikovog oksida
Također se naziva diazotski pentoksid, nitronijum nitrat, nitril nitrat ili dušikov anhidrid. 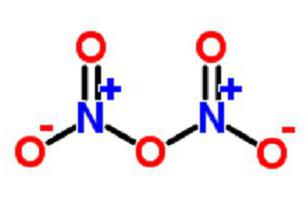
Ona je u obliku bezbojnih kristala koji su nestabilni i nestabilni. Njihova stabilnost je uočena na niskim temperaturama. Tu strukturu tvore nitrati i nitritni ioni.
U plinovitom obliku, tvar ima oblik anhidrida NO2-O-NO2.
Pentavalentni dušikov oksid ima kiselinska svojstva. Lako se razgrađuje oslobađanjem kisika.
Tvar reagira s vodom, što rezultira dušičnom kiselinom.
Alkali rastvaraju anhidrid oslobađanjem soli nitrata.
Kako dobiti dušične okside
Kada se u akutnom stanju koristi suhi amonijev nitrat, N 2 O oksid se formira, ali ova metoda može biti praćena eksplozijom.
Poželjna metoda dobivanja monovalentnog oksida je učinak dušične kiseline u koncentriranom obliku na sulfaminsku kiselinu. Glavni uvjet je grijanje.
Nitrosil, ili NO, je poseban dušikov oksid, koji se dobiva interakcijom molekula N2 i O2. Važan uvjet za ovaj proces je snažno zagrijavanje iznad 1000 ° C.
Prirodna metoda dobivanja povezana je s munjevitim ispuštanjem u atmosferskom zraku. Takav oksid brzo se spaja s molekulama kisika i nastaje dioksid.
Laboratorijska metoda za sintezu NO povezana je s reakcijom metala i nekoncentrirane dušične kiseline. Primjer takve reakcije je interakcija bakra s HNO3.
Druga metoda za stvaranje dušikovog monoksida je reakcija željeznog klorida s natrijevim nitritom i klorovodičnom kiselinom. Rezultat procesa je željezo i natrijevi kloridi, voda i sam oksid.
U industrijskom mjerilu, proizvodi se oksidacijom molekula amonijaka tijekom zagrijavanja i pod visokim tlakom. Akcelerator procesa je platina ili krom trovalentni oksid. 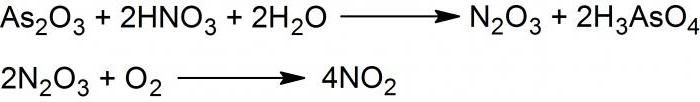
Dioksid, ili NO2 , dobiva se reakcijom arsena trovalentnog oksida s 50% dušične kiseline, koja se primjenjuje kap po kap na površinu čvrstog reagensa. Nastaje smjesa oksida dvovalentnog i tetravalentnog dušika.
Ako se ohladi na temperaturu od -30 ° C, tada se sintetizira dušikov anhidrid ili N203.
U obliku praha dobiva se u slučaju prolaska električne struje kroz plinoviti oblik.
Ako se na škrobni prah djeluje dušičnom kiselinom s koncentracijom od 50%, oslobađaju se oksidi dvovalentnog i tetravalentnog dušika, plin ugljikov dioksid i voda. Nakon toga, od prva dva dobivena spoja nastaje molekula N2O3.
Kao rezultat toplinske razgradnje spoja olova nitro, dušikov dioksid, slobodnog kisika i olovnog oksida.
Anhidrid, ili N2O5, nastaje zbog eliminacije molekule vode iz kiseline dušičnom reakcijom fosforni oksid pentavalent.
Drugi način da se sintetizira je proći suhi klor kroz bezvodni srebreni nitrat.
Ako na dušikov dioksid djeluju molekule ozona, stvara se N2O5 .