Natrijev bikarbonat: formula, sastav, uporaba
Pečenje ili soda za pečenje je spoj poznat u medicini, kuhanju i potrošnji u kućanstvu. To je kisela sol, čija je molekula formirana pozitivno nabijenim ionima natrija i vodika, anionom kiselinskog ostatka ugljične kiseline. Kemijski naziv soda je bikarbonat ili natrijev bikarbonat. Formula spoja prema Hill sustavu je: CHNaO 3 (bruto formula).
Razlika između kisele soli i medija
Ugljična kiselina tvori dvije skupine soli - karbonati (srednji) i bikarbonati (kiseli). Trivialno ime karbonata - soda - pojavilo se u antici. Potrebno je razlikovati srednje i kisele soli po nazivu, formuli i svojstvima.
Na2C03 - natrijev karbonat, dinatrijeva sol ugljične kiseline, natrijev karbonat. Služi kao sirovina za staklo, papir, sapun, koristi se kao deterdžent.

NaHC03 - natrijev bikarbonat. Sastav sugerira da je tvar mononatrijeva sol ugljične kiseline. Ovaj spoj karakterizira prisutnost dvaju različitih pozitivnih iona - Na + i H + . Vanjski kristalne bijele tvari su slične, teško ih je razlikovati.
Smatra se da je tvar NaHCO 3 soda bikarbona ne zato što se proguta kako bi se utažila žeđ. Iako s ovom supstancom možete napraviti gazirano piće. Otopina ovog bikarbonata uzima se oralno uz povećanu kiselost želučanog soka. Kada se to dogodi, neutralizira se višak protona H + , koji iritiraju zidove želuca, uzrokujući bol i paljenje.
Fizikalna svojstva sode bikarbone
Bikarbonat su bijeli monoklinski kristali. Sastav ovog spoja sadrži atome natrija (Na), vodika (H), ugljika (C) i kisika. Gustoća tvari je 2,16 g / cm3. Točka topljenja je 50–60 ° C. Natrijev bikarbonat - mliječno-bijeli prah - kruti kristalni spoj, topiv u vodi. Soda za piće ne gori, a pri zagrijavanju iznad 70 ° C razgrađuje se na natrijev karbonat, ugljični dioksid i vodu. U proizvodnim uvjetima, češće se koristi granulirani bikarbonat.

Sigurnost sode bikarbone za ljude
Spoj nema miris, okus mu je gorko-slan. Međutim, ne preporučuje se miris i okus tvari. Udisanje natrij bikarbonata može uzrokovati kihanje i kašljanje. Jedna primjena temelji se na sposobnosti sode bikarbone da neutralizira mirisne tvari. Puder se može obrađivati sportskom obućom kako bi se riješio neugodnog mirisa.
Soda za piće (natrijev bikarbonat) je bezopasna tvar u dodiru s kožom, ali u čvrstom obliku može uzrokovati iritaciju sluznice očiju i jednjaka. U niskim koncentracijama otopina nije otrovna, može se uzimati oralno.
Natrijev bikarbonat: spoj formule
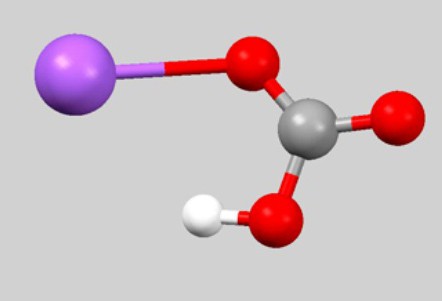
Bruto formula CHNaO 3 rijetko se nalazi u jednadžbama kemijske reakcije. Činjenica je da ne odražava vezu između čestica koje tvore natrijev bikarbonat. Formula koja se uobičajeno koristi za opisivanje fizikalnih i kemijskih svojstava tvari je NaHC03. Međusobni raspored atoma odražava model kuglične šipke molekule:
Ako iz periodičkog sustava izvučemo vrijednosti atomskih masa natrija, kisika, ugljika i vodika. možete izračunati molarnu masu tvari natrijevog bikarbonata (formula NaHCO3):
Ar (Na) - 23;
Ar (O) - 16;
Ar (C) - 12;
Ar (H) -1;
M (CHNaO3) = 84 g / mol.
Struktura tvari
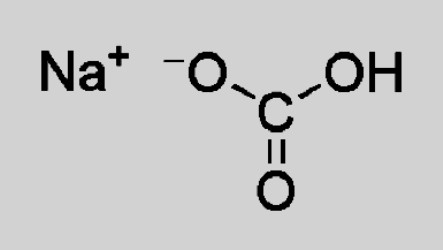
Natrijev bikarbonat je ionski spoj. Struktura kristalne rešetke uključuje natrijev kation Na + , zamjenjujući jedan ugljikov atom u ugljičnoj kiselini. Sastav i naboj aniona - HCO 3 - . Kada se otopi, dolazi do djelomične disocijacije na ione koji tvore natrijev bikarbonat. Formula koja odražava strukturne značajke izgleda ovako:
Topljivost pića u vodi
7.8 g natrijevog bikarbonata se otopi u 100 g vode. Tvar se podvrgava hidrolizi:
NaHC03 = Na + + HC03;
H20 = H + + HE - ;
HCO3 - + H + = H20 + CO2.
Pri sabiranju jednadžbi ispada da se u otopini akumuliraju hidroksidni ioni (slabo alkalna reakcija). Tekuće boje fenolftalein u ružičastoj boji. Boja univerzalnih indikatora u obliku papirnatih traka u otopini sode mijenja se od žuto-narančaste do sive ili plave.
Reakcija izmjene s drugim solima
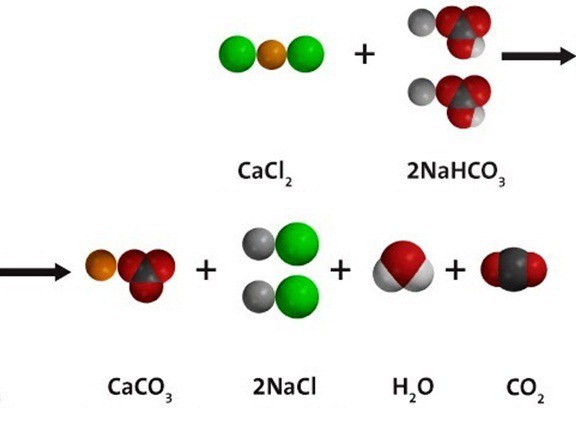
Vodena otopina natrijevog bikarbonata ulazi u reakciju ionske izmjene s drugim solima, pod uvjetom da je jedna od novootkrivenih tvari netopljiva; ili nastaje plin, koji se uklanja iz sfere reakcije. U interakciji s kalcijev klorid, Kao što je prikazano na donjem dijagramu, dobivaju se bijeli talog kalcijevog sarbonata i ugljikov dioksid. Natrij i klorni ioni ostaju u otopini. Jednadžba molekularne reakcije:
Interakcija sode bikarbone s kiselinama
Natrijev bikarbonat reagira s kiselinama. Reakciju ionske izmjene prati stvaranje soli i slaba ugljična kiselina. U vrijeme prijema, razgrađuje se u vodu i ugljični dioksid (isparava).
Ljudski želučani zidovi proizvode klorovodična kiselina postoje u obliku iona
H + i Cl-. Ako uzimate unutarnji natrij bikarbonat, reakcije se javljaju u otopini želučanog soka uz sudjelovanje iona:
NaHC03 = Na + + HC03;
HCl = H + + Cl-;
H20 = H + + HE - ;
HCO3 - + H + = H20 + CO2.
Doktori ne preporučuju trajnu uporabu kada visoka kiselost želučani natrij bikarbonat. Upute za lijekove navode različite nuspojave dnevnog i dugotrajnog unosa sokova za piće:
- povišeni krvni tlak;
- podrigivanje, mučnina i povraćanje;
- tjeskoba, loš san;
- smanjen apetit;
- bol u trbuhu.
Dobivanje sode bikarbone
U laboratoriju se natrijev bikarbonat može dobiti iz sode. Ista metoda korištena je ranije u kemijskoj industriji. Suvremena industrijska metoda temelji se na interakciji amonijaka s ugljičnim dioksidom i niskom topljivosti sode za piće u hladnoj vodi. Kroz rješenje natrijev klorid propuštaju se amonijak i ugljični dioksid (ugljični dioksid). Nastaju otopina amonijevog klorida i natrijevog bikarbonata. Kada se ohladi, topljivost sode za piće se smanjuje, zatim se tvar lako odvaja filtracijom.
Gdje se koristi natrijev bikarbonat? Upotreba sode bikarbone u medicini
Mnogi ljudi znaju da atomi metalnog natrija snažno reagiraju s vodom, čak i na paru u zraku. Reakcija počinje aktivno i popraćena je oslobađanjem velike količine topline (spaljivanja). Za razliku od atoma, natrijevi ioni su stabilne čestice koje ne štete živom organizmu. Naprotiv, oni su aktivno uključeni u reguliranje njegovih funkcija.
Kako se tvar netoksična za ljude koristi i korisna u mnogim aspektima - natrijev bikarbonat? Primjena se temelji na fizikalnim i kemijskim svojstvima sode za piće. Najvažnija područja su domaća potrošnja, prerada hrane, zdravstvena zaštita, tradicionalna medicina i piće.
Među glavnim svojstvima natrijevog bikarbonata je neutralizacija povišene kiselosti želučanog soka, kratkoročno uklanjanje boli kod hiperacidnosti želučanog soka, čira na želucu i 12 čira dvanaesnika. Antiseptički učinak otopine pića koristi se u liječenju upale grla, kašlja, intoksikacije, mučnine. Oni se peru usta i nos, sluznice očiju.

Različiti oblici doziranja natrijevog bikarbonata su široko korišteni, na primjer, prašci koji su otopljeni i korišteni za infuzije. Dodijeliti rješenja za pacijente za primanje iznutra, oprati s kiselim opeklinama. Natrijev bikarbonat se također koristi za izradu tableta i rektalnih supozitorija. Upute za pripravke sadrže detaljan opis farmakološkog djelovanja, indikacije. Popis kontraindikacija je vrlo kratak - individualna netolerancija na tvar.
Upotreba sode bikarbone u svakodnevnom životu
Natrijev bikarbonat je hitna pomoć za žgaravicu i trovanje. Uz pomoć pića kod kuće izbjeljivati zube, smanjiti upalu u slučaju akni, obrišite kožu kako biste uklonili višak masnog tkiva. Natrijev bikarbonat omekšava vodu, pomaže u čišćenju nečistoća s različitih površina.
Kada se voda za pranje ruku iz vune može dodati u bikarbonu. Ova tvar osvježava boju tkanine i uklanja miris znoja. Često se pri glačanju svilenih predmeta pojavljuju žute oznake s željeza. U ovom slučaju, gnojnica pića i vode pomoći će. Tvari treba što prije pomiješati i nanijeti na mrlju. Kada se kaša osuši, treba je očistiti četkom, a proizvod isprati hladnom vodom.
U reakciji s octenom kiselinom se dobije natrijev acetat i brzo se ispušta ugljični dioksid, pjenjenja cijele mase: NaHC03 + CH3COOH = Na + + CH3COO - + H20 + CO2. Ovaj proces se nastavlja kad god se peče soda za pečenje s octom u proizvodnji pjenušavih pića i slastica.

Okus pečenja bit će mekši ako koristite sintetički ocat koji nije kupljen u trgovini, već sok od limuna. U ekstremnom slučaju, možete ga zamijeniti mješavinom od 1/2 žličice. limunska kiselina u prahu i 1 žlica. l. voda. Pijenje sode s kiselinom dodaje se tijestu kao jedan od posljednjih sastojaka, tako da možete odmah staviti pecivo u pećnicu. Osim natrijevog bikarbonata, amonijev bikarbonat se ponekad koristi kao prašak za pecivo.